Свойства растворов силикатов четвертичных аммониевых оснований
Очевидно, что при одинаковом способе получения различие в свойствах растворов в системе М20—Si02—Н20 (где М — катион щелочного металла или органического основания) может определяться только видом катиона. Влиянию катиона на анионный состав растворов посвящены многие работы Хоббеля и др. [23]. Методами триметилсилирования и ядерного магнитного резонанса — ЯМР Si можно показать, что разбавленные высокощелочные растворы любых силикатов близки к истинным растворам и их анионный состав почти не зависит от типа катиона (табл. 17).
При увеличении концентрации силикатов с тем же модулем 2 Анионный состав раствора резко изменяется. Так, 1,64 М раствор ТМА на 65% состоит из ионов SigO®^, на 25% — из полимерных анионов и остальные ионные структуры не превышают 2%; 2,5 М раствор ТЭА составляют почти на 40% ионы Si60i5~, около 50% — полимерные анионы, 3% — SieOfo", каждый из остальных ионов — меньше 2%.
|
Иои |
0,6 М раствор ТБА содержит 50% полимерных анионов, около 20% моно-, ди-, тримерных линейных анионов, примерно 4% Si10O^-, других сдвоенных циклов нет. Все концентрированные
Таблица 17. Концентрация ионов в 0,1 М растворах силикатов с модулем 2
|
ТМА |
ТЭА |
ТБА |
Na |
|
58 |
56 |
59 |
48 |
|
14 |
14 |
16 |
14 |
|
4 |
7 |
6 |
7 |
|
1 |
3 |
1 |
2 |
|
3 |
3 |
4 |
3 |
|
2 |
4 |
2 |
3 |
|
2 |
2 |
2 |
6 |
|
16 |
11 |
10 |
17 |
|
% SiOj в растворе |
|
SinOST Si3O?0- suoir Si30|- Si40?r Другие определенные циклические анионы Полимерные анионы |
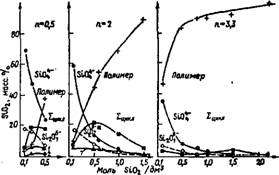
Растворы получены растворением кремнекислоти в соответствую, щей гидроокиси четвертичного аммония. Более подробно завися, мость концентрации анионов различной структуры в раствора;, силикатов ТБА разных модулей от общей концентрации кремнезе. ма в растворе представлена на рис. 39. Полимеры в данном случае представляют собой частицы, содержащие более десяти атомов кремния. При одном и том же модуле раствора увеличение кон - центрации не сопровождается изменением отношения числа катио - нов на 1 атом кремния. Поэтому резкое уменьшение доли моно - и димерных анионов с увеличением концентрации означает, что все большая часть катионов идет на стабилизацию полимерных частиц. Растворы силикатов ЧА представляют собой наглядный пример плавного перехода системы от истинных растворов к коллоидным системам (золям). Полимеризация кремнезема в растворе с увеличением его концентрации и модуля протекает так, что образуются блоки из частиц кремнезема, а не линейные структуры. Рост этих блоков и есть образование частиц золя.
В Технологическом институте были синтезированы и иссле дованы растворы полисиликатов ТЭА и ТБА силикатных модулей от 2 до 7, полученные растворением аэросила в концентрированных («30—35%) растворах соответствующих гидроокисей. В табл. 18 представлены составы и физико-химические характеристики полученных растворов при 20 °С.
При исследовании строения кремнезема в полисиликатных растворах представляли интерес распределение SiC>2 между растворенной (а-БіОг) и коллоидной составляющими, влияние модуля и концентрации на это распределение, динамика изменения его при приготовлении растворов. Учитывая, что граница между растворенным и коллоидным кремнеземом может быть проведена только условно, мы воспользовались методикой определения a-SiCb основанной на молибдатном методе анализа [26]. Найденный по этому методу a-Si02 полагали растворенным кремнеземом, а разницу между общим содержанием SiC>2 и a-SiC>2 считали коллоидным кремнеземом. Низкомодульные полисиликатные растворы можно было сопоставить с данными Хоббеля [23], а по известным константам скорости взаимодействия молибденовой кислоты с кремнеземом [2] представлялось возможным оценить, какие формы кремнезема могут превратиться в кремнемолибдат за время анализа. Оказалось, что а-БЮг включает все олигомерные формы кремнезема примерно до Si25- Помимо определения а-БіОг растворов полисиликатов ТЭА и ТБА, были исследованы их ИК-спектрЫ а методом ЯМР Si29 найдены доли кремнезема с различной связностью.
Как следует из табл. 18, один моль основания ЧА перевод^ в a-форму одно и то же количество кремнезема, начиная с модул' 4 и выше. Для гидроокиси тетраэтиламмония эта величина сколько выше, чем для тетрабутиламмония. Данные по ЯМР Si показывают практически полное отсутствие мономерной формь1
|
Рис. 39 |
Рис 39. Изменение анионного состава с концентрацией раствора силиката ТБА
Разных модулей
На кривых обозначены ионы-. • —мономеры; О —димеры; ▲ /, 2—соответственно
Тримерные и тетрамерные линейные ионы; ■ — различные циклические олигомеры; -)------------------
Полимеры [23]
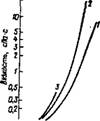
Рис. 40. Вязкость растворов силикатов ЧА в зависимости от их концентрации [11] Молярное отношение SiOj/NRc / — 12,5; 2 — 9,5; 3 — 4,5
Кремнезема. Об этом же свидетельствуют ИК-спектры растворов, так как поглощение в области 920—950 см-1, характерное для мономеров, отсутствует. Следовательно, растворы, исследованные нами, даже в области одних и тех же модулей заметно отличаются по анионному составу от растворов силикатов ТЭА и ТБА, исследованных в работе [23]. Это следует отнести за счет способа получения раствора, так как растворяя аэросил в растворе гидроокиси ЧА, шли от более полимерных к менее полимерным формам, в отличие от работ Хоббеля, где растворяли слабополимеризо - ванную кремнекислоту.
|
3B' Го
Fff1 ' ' ' ' ■ i i Ю 20 so w so a StOj,«occ. % Рис. 40 |
Очень мала в полученных нами растворах доля атомов кремния, связанных четырьмя силоксановыми связями, а наибольшую долю составляет кремнезем со связностью 2 и 3, причем с увеличением модуля доля Q=3 растет. Кремнезем со связностью 3 — это, главным образом, сочлененные трех-, четырех-, пятичленные циклы, у которых доля атомов кремния с тремя силоксановыми связями велика. Наглядной количественной характеристикой состояния кремнезема в растворе может служить средняя величина связности Qcp, рассчитанная по уравнению Qcp= где — доля кремнезема со связностью Q((Q;=0, 1, 2, 3, 4). Как видно из табл. 18, Qcp закономерно возрастает вместе с модулем раствора и не зависит в данном случае от вида катиона. Средняя связность характеризует полимерность кремнезема в растворе примерно так же, как средняя относительная молекулярная масса. Однако пара- Метр связности удачно отличается тем, что при изменении агрегатного состояния системы (высушивание, цементация) он продол-
И
^ает оставаться удобным для определения на любой стадии (по Si29) и отражает изменение состояния кремнезема в такого рода процессах.
Увеличение степени полимерности растворов с возрастанием модуля показывают также ИК-спектры. Если низкомодульные растворы имеют глубокий максимум поглощения в области 1020 см-1, то с увеличением модуля этот максимум сливается с максимумом поглощения при 1120 см-1, образуя сплошную зону поглощения. Возрастание частоты поглощаемых квантов связано с возрастанием доли силоксановых связей в исследуемой системе. Все полученные факты свидетельствуют, что стабилизирующая способность ионов четвертичного аммония велика и строение полисиликатов в растворе существеннейшим образом связано не только с модулем и концентрацией раствора, но также с видом катиона в растворе и способом получения раствора. Анализ на растворенный кремнезем (a-Si02), отличаясь простотой, может быть использован для определения окончания процесса взаимодействия раствора гидроокиси ЧА с кремнеземом. Если для приготовления раствора использовать кристаллические или малоактивные плотные формы кремнезема, то растворение протекает медленно, ограничивается переходом в раствор Si02 только в а-форме, высокомодульные полисиликатные растворы не образуются.
При получении растворов полисиликатов с использованием аэросила после достижения постоянного, не изменяющегося во времени содержания a-Si02 и образования прозрачного раствора еще долго (в течение нескольких недель) происходят процессы старения в системе, выражающиеся в том, что вязкость раствора падает. Так как полученные дисперсные системы близки к ньютоновским жидкостям, это означает, что в системе происходит структурирование, но не между коллоидными частицами, а внутри них, т. е. из более рыхлых образуются более плотные коллоидные частицы и, видимо, сокращается объем гидратных оболочек, движущихся вместе с коллоидной частицей.
На рис. 40 приведены данные Уэлдеса и Л анге по вязкости растворов силикатов ЧА разных модулей в зависимости от концентрации. При тех температурах и концентрациях кремнезема в растворах силикатов щелочных металлов, когда вязкость их становится недопустимо большой для различных транспортных операций, Растворы силикатов ЧА близки к вязкости воды, т. е. силикатный Модуль и концентрация последних может быть гораздо выше.
Наличие органической компоненты в растворе силикатов четвертичного аммония приводит к другому отличительному свойству этих растворов. Они способны смешиваться с водорастворимыми' °рганическими веществами, не вызывая ни фазового расслоения, ни коагуляции кремнезема. Концентрация кремнезема в смешанном водноорганическом растворе может превышать 40%, а органическая компонента в смешанном растворителе способна достигать 50%. Растворы силикатов калия и натрия (но не лития)
Невозможно смешать с органическими растворителями, не вызы. вая коагуляции или расслоения системы на две фазы, даже если концентрация кремнезема составляет 10—15%. В табл. 19 приве - дены данные, характеризующие способность растворов силикатов ЧА смешиваться с некоторыми водорастворимыми органическими растворителями. Предположительно речь идет о силикате тетрагидроксиэтиламмония, который имеет высокое сродство к низшим спиртам. В таблице указано максимально возможное количество кремнезема и органического растворителя (масс. %) в трехкомпонентной системе. Катионы ЧА, не включающие гид - роксильные группы в органические радикалы, должны иметь меньшую совместимость со спиртами.
Как видно из табл. 19, совместимость компонентов растворителя очень сильно возрастает с уменьшением концентрации кремнезема и снижается по мере увеличения длины органического радикала.
Способность растворов силикатов ЧА смешиваться с некоторыми органическими растворителями, помимо сродства органического катиона к органическим растворителям, определяется общей высокой устойчивостью лиофильной дисперсной системы, какой является высокомодульный водный раствор силикатов ЧА. При введении катионов ЧА высокая устойчивость силикатного раствора по отношению к коагуляции, гелеобразованию, т. е. к различным видам агрегации кремнезема, проявляется многообразно. Это прежде всего стабильность высокомодульных концентрированных водных растворов, не достижимая для растворов силикатов натрия или калия; это способность силикатов ЧА образовывать высокомодульные водорастворимые аморфные порошки. Сюда же следует отнести устойчивость растворов с высоким содержанием кремнезема по отношению к замерзанию. Многократное замораживание и оттаивание растворов силикатов ЧА не приводит к коагуляции кремнезема даже при наличии в системе неорганических катионов. Совместимость высокомодульных концентрированных растворов силикатов ЧА с органическими растворителями есть одна из форм проявления устойчивости кремнезема к гелеобразованию и коагуляции при частичной замене молекул воды в соль - ватных оболочках мицелл или полианионов на молекулы спирта
|
Модуль |
Si02 в исходном растворе, % |
СНзОН |
С2Н5ОН |
Изо-СзН/ОН |
(СНз)2СО |
|||
|
М20 |
Спирт, V /о |
Si02, /О |
Спирт, о/ /о |
Si02, О/ /О |
Спирт, % |
Si02, /о |
Ацетои, /о |
SiCh, % |
|
Таблица 19. Границы совместимости растворов силикатов ЧА со спиртами и ацетоном (11] |
|
6,5 6,5 6,5 9,0 |
|
50 30 15 40 |
|
37 50 60 39 |
|
31 15 50 24 |
|
28 44 54 25 |
|
40 16 6 29 |
|
23 37 54 21 |
|
43 18 6 31 |
|
23 37 44 21 |
|
43 18 8 31 |
|
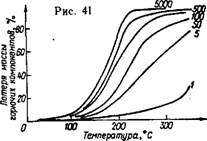
Рис. 41. Потери массы силиката ЧА (Si02/NR4= 12,5) в зависимости от температуры и времени сушки Числа у кривых — время сушки в минутах [11] |
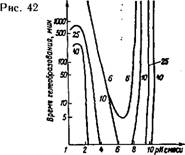
Рис. 42. Время гелеобразовання раствора силиката ЧА (Si02/NR4= 12,5) при
Различных рН [11] і
РН раствора создай добавлением H2SO4. Числами у кривых обозначен % SiC>2 в растворе
Или ацетона. Подобная стабильность дисперсной системы по отношению к замене части воды органическим растворителем характерна также для растворов силикатов лития, хотя в исходном состоянии в них органическая компонента отсутствует.
Безусловно, высокая стабильность полисиликатных растворов отчасти связана с геометрическими размерами катионов в роли противоионов, составляющих внешнюю обкладку двойного электрического слоя. Среди ионов щелочных металлов радиус гидратированного катиона лития наибольший. Однако в ассоциативных процессах коагуляции кремнезема или гелеобразовання большую роль играют поляризационные свойства коллоидных частиц вкупе с гидратными слоями и плотной частью двойного электрического слоя.
Различные виды гидратации положительных и отрицательных частиц в растворах полисиликатов ЧА резко изменяют поляризационные свойства дисперсной фазы и обусловливают ее высокую устойчивость к ассоциативным процессам. Известно [22], что для ионов четвертичного аммония характерна сильная гидрофобная гидратация, приводящая уже у ТБА к образованию клатратных структур и частиц, в противоположность положительной гидратации кремнезема. В целом это сочетание обусловливает низкую поляризуемость дисперсных частиц и тем самым высокую стабильность системы.
|
|
По отношению к нагреванию стабильность растворов силикатов "А определяется термической устойчивостью органических катио - н°в. Начало их медленной термической диссоциации относится к температуре 70—80 °С. Термогравиметрический анализ продукте воздушной сушки растворов силикатов ТБА и ТЭА дает температуру разложения 180—190 °С, куда относятся основные потери
Массы. На рис. 41 приведены кривые термического разложен^ силиката четвертичного аммония с силикатным модулем ЗО в зави симости от температуры и времени термической обработки.
В отношении протолитических реакций отличие растворов силикатов ЧА от растворов силикатов щелочных металлов невели - ко. Стабильность растворов силикатов ЧА в зависимости от рЦ среды (рис. 42) носит такой же характер, как у растворов силика - тов щелочных металлов. В кислой области максимум устойчивости около 2, а минимум — при рН, равном 6,5—7. При высоких рН растворы силикатов ЧА устойчивы неограниченно. Если сравнить концентрации кремнезема в растворах силикатов ЧА и щелочных металлов, имеющих при одном и том же рН среды одинаковое время гелеобразования, то у силикатов ЧА концентрация существенно выше. По нашим измерениям, при одинаковом силикатном модуле и концентрации кремнезема растворы полисиликатов ЧА имеют рН несколько более высокий, чем соответствующие растворы полисиликатов щелочных металлов. Это указыва-ет на неодинаковость распределения основания между раствором и коллоидными части цами или, что то же, на более глубокий гидролиз силикатов ЧА.
В табл. 20 по данным [11] приведены коммерческие рас творы силикатов четвертичного аммония, выпускаемые промышленностью за рубежом. В таблице прежде всего обращают на себя внимание высокие модули и концентрации SЮг в сочетании с низ кой вязкостью жидких стекол — показатели, не достижимые для натриевых или калиевых систем. По объему производства СЧА не могут сравниться с натриевыми силикатами, но заняли уже прочное место в общей номенклатуре жидких стекол. Хотя стоимость СЧА выше натриевых силикатов, использование СЧА дает возмож ность создавать новые ценные композиционные материалы или существенно совершенствовать качество известных композиций.
|
Содержание, % |
|
SiQg (NROsO |
|
Плотность, dil г/см3 |
|
SiOj |
|
РН |
|
• /о |
|
; мол |
|
(NR4)20 |
|
Si02 |
|
NR« |
Таблица 20. Характеристики коммерческих растворов СЧА
Вязкость прн 20 "С, Па с суТствии С02 они гидролизуются с образованием кремнезема и растворимого в воде карбоната ЧА. Ионы четвертичного аммония замещаются в силикатах ионами металлов (кроме щелочных) при 8заимодействии с растворимыми солями этих металлов.
Катионные поверхностно-активные вещества на основе четверочного аммония, обычно содержащие один из органических ради - калов с очень длинной цепью, иногда добавляют к растворам жидюго стекла. При этом образуются силикаты четвертичного аммония, и система способна вспениваться при взбивании. Добавление отвердителей или гелеобразователей дает возможность получать легкие прочные пенные структуры.