СВОЙСТВА АКРОЛЕИНА
Акролеин обладает следующими свойствами (см. также [3]):
Температура плавления, °С.......................................................... —86,95
Температура кипения, °С...................................................................... 52,69
Плотность р|о..................................................... >........................ 0,8389
Плотность пара по отношению к воздуху при 20 °С / . 0,8402
Показатель преломления............................................................... 1,4017
Вязкость при 20 °С, сП...................................................... ........ 0,393
Критическая температура, К......................................................... 510
Критическое давление, кгс/см2............................................................... '51,58
Критический объем, смз/моль...................................................... 189
Теплоты испарения
Кал/г....................................................................................... 129,5
Кал/моль. . ............................................................................. 7260
Теплота образования (газ) при 25 °С, ккал/моль. . . —17,79
Энергия образования (газ) при 25 °С, ккал/моль. . . ■—12,86
Теплота сгорания (жидкость) при 25 аС, ккал/г. . . 6,95 Удельная теплоемкость (жидкость) при 17—44 °С,
Ккал/(г • SC) .................................................................................... 0,511
Удельная теплоемкость (газ), кал/(моль • °С)
При 300 .................................................................................. 16,07
5Q0 ............................................................................... 22,97
700 ......................................................................................... 27,86
Коэффициент теплового расширения при 20 5С, 1/°С 0,00143 Пределы взрываемости в смеси с воздухом, объемн. %
Верхний................................................................................. 31
Нижний................................................................................... 2,8
Температура воспламенения в закрытом сосуде, 9С. . —25
Электропроводность при 10 °С, Ом-1........................................... 1,55 • 10"7
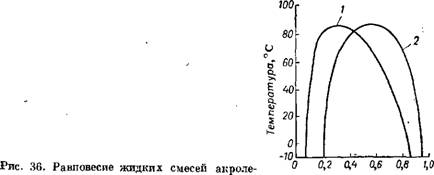
На рис. 36 показано равновесие жидких смесей акролеина и воды.
|
Ина и воды: Концентрация акролеина, І — мол. ч.; 2 — вес. ч. вес. или мол. ч. |
|
Катализаторы для окисления
|
|
Состав газа, % |
||
|
Пропилен |
Воздух (или Ог) |
Водяной пар |
|
Температура реакции °С |
|
Катализатор |
|
490/3,8 Кгс/см2, 467/3,5 кгс/см2 425 |
|
1 ч. (02) |
|
1 ч. |
Комбинация молибдата Bi (I система) и 80% Мо03-Р205, 6,2% Ві203, 3,8% МоОз+9,5% Si02 (II система) . . .
Фосфоромолибдат Bi
Молибдат Bi, молибдат Со, фосфат Си, ванадат Си, вольфрамат Си и др.
Молибдат Са—Bi.............................................
Молибдат щелочноземельных металлов Молибдат Bi + MgO, А1203 или Fe203
|
19 |
|
67 |
|
14 |
|
35 |
|
53 12 (02) |
|
10 |
|
40 26 |
|
50 66 |
|
50 |
|
25 |
|
25 |
Медьсодержащий катализатор (первый реактор) и вольфрамат или молибдат Bi, Ni, Со
Н8[Х(М0207)б] + Ві!!0з; X—редкоземельный металл, например додекамо-
Либдатоцериевой кислоты...........................
Фосфоромолибдат Bi + H2S04 или сульфаты, молибдат Bi+H2SC>4
Боромолибдат Со ..... ....
Фосфоро - или кремнемолибдат Си—Bi (Mo : Си : Р : Si= 1 : 0,5 : 0,1 + Ві203)
(Си, Ni, Cr)e(Si, Р)(Мо, W, V)l2- О40-бо, например Cu9PMoi2047,5 на SiC. . .
Ni0-20Coi0-i5Fei,0-7Bi0,i_4 •
• Po. i-2Moi2035-85, например
Ni10FeBiPMoi2O57 .......................................
CuO + кремнемолибденовая кислота. . Фосфоромолибдат Fe—Bi......
Молибдат Fe-fCr203 ............................. . . .
Молибдат Fe + Ті............................................
Фосфоромолибденовая кислота+As203
Фосфорованадат Cr— Bi, например
|
17 (02) |
|
50 |
|
33 Пропан |
Cr (VOs)3 • СгР04 • Ві203 ............................
450 500
350/7 кгс/см2; 375- -500/6-7 кгс/см2
450 430
380- 500
440 380
|
Продолжение табл. 12
|
Катализатор
Арсеномолпбдат Ві, ванадовольфрамат Ві, комбинации Bi— Sn—As— Мо—
-V-W-B........................................................
Bi (V03)3 ■ ВІРО4 ■ Bi2D3, фосфорована - дат Ві
Cu20 + молибдат или вольфрамат. . .
Молибдат Си...................................................
Фосфороборванадат........................................
Фосфорованадомолибдат...............................
Ванадат Ві, фосфорованадат Ві. . . Bil2PW12056,5
Ванадат Ag, Sn или Ві.....................................
Ві203+ кремневанадовольфрамовая кислота...
Те03.................................................................
Te03 + 5%Re20, ...............................................
С0М0О4 • Те02 ■ HRe04 (вместо С0М0О4 также молибдат или фосфат Ni и Си)
Молибдат Ві + Те02(Те) .................................
СиМо04+теллурат Си...................................
Молибдат Мп + Те02.......................................
Мп2Р20,.Мо03-Те02.........................................
Фосфоромолибдат Ві + Те02 на ТЮ2
Или силикагеле.............................................
Фосфоромолибдат Ві + Те02 ..........................
Те03+6Мо03 и Te03 + 6W03 и др. . . Мо03 + Сг203 или W03+Te02+окись
As, Sb или Bi.................................................
Фосфоромолибдат-)-1% Те или Те02 Фосфорованадиевая или фосфоровольф - рамомолибденовая кислота + Те03 Те02, активированная Cl2, Вг2 или 12
На бентоните................................................
(Bi, Те)0,5.18(Се, Th)(Mo, W, V)12037.84 Cu6-9(Te, Se)0l5-i, e(P. Si)0-i(Mo, W)12-
• O40-60......................................................
Теллуромолцбдат Ni.......................................
Sb204-^Sn02 = l : (3-50) .......
|
Состав газа, % |
Температура реакции, °С |
||
|
Пропилен |
Воздух (или Ог) |
Водяной пар |
|
|
440 |
|||
|
— |
— |
— |
475 |
|
— |
— |
— |
300-360 |
|
— |
— |
— |
475-650 |
|
13 |
13 (02) |
20 |
400-450 500 |
|
10 |
49 |
41 |
480 |
|
10,5 |
57 |
32,5 |
430 |
|
— |
— |
— |
345 |
|
10 10,6 16 (пропан) |
50 52,1 41 |
40 37,3 43 |
350-425 452 400 525 385 |
|
10,0 15 13 |
52,5 71 13 (02) |
37,5 14 20 |
- 480 480 485 |
|
12 |
18 (02) |
70 |
400 486 |
|
15 |
71 |
14 |
400 |
|
— |
— |
— |
400-600 |
|
11,7 |
48,2 |
40,1 |
360 |
|
Продолжение табл. 12
|
Катализатор
Sb204 ■ Sn02 на Si02.........................................
Sba04 • Sn02 на графите..................................
Sb2C>4 • Sn02 • на глине, фарфоре, стеклянных шариках
SbaC>4 • SnOa-f- Sb203 .....................................
Sb204 • Sn02 с добавлением солей Са, Fe (III) или Ва
Sb204 ■ Sn02 на Si02 (из этилсиликата) Sb204-Sn0a+окись Bi, Ni или Со. . Sb204 • SnOj, (3,26 : 1) .'
Sb2o4■Sno2 . . . ; ............................................
Sb204•SnOs.................................................
Sb204■SnOa.....................................................
Окись Sb — U + окись металла (например, CuO)
Sb203+окиси металлов побочных групп, например Sb203 • U808 ....
Sb20s+Fe203 ......................................................
Окись Sb —Mn.................................................
Ванадат Sb, фосфат Sb и Bi203 на SiC Молибдат Sb 4- окись Sn, Ті или W. .
Фосфорованадат Sn........................................
Окись As с добавкой окисей других металлов, например As205 • Fe203 . . Окись Mo или другого тяжелого ме - талла+В203+As205 на SiOa. . . . Молибдат Fe—С1 или молибдат С1+
+ As205 .......................................................
Вольфрамовая кислота + As205 . . . .
Арсенованадат Си на ТЮ2..............................
Фосфоромолибдат + As205 .............................
Титанат Sb + окись W, Mo или As. .
Фосфат Ag, Fe или Си......................................
Окись Си —Au на SiC.....................................
|
Состав газа, % |
Температура реакции, °С |
||
|
І К И Й И Вё |
Воздух (ИЛИ О г) |
Водяной пар |
|
|
10 |
70 |
20 |
452 |
|
10 |
56,5 |
33,5 |
497 |
|
10 |
50 |
40 |
400 |
|
10 |
50 |
40 |
480 |
|
10,6 |
49,6 |
39,8 |
411 |
|
_ |
_ |
_ |
439-524 |
|
440-519 |
|||
|
439-483 |
|||
|
10 |
50 |
40 |
467 |
|
— |
* |
-- |
|
|
5 |
55 |
34 |
480 |
|
8 |
62 |
30 |
480 |
|
20 |
' 20 |
60 |
475 |
|
9 |
77 |
14 |
390 |
|
10 |
45 |
45 |
370-380 |
|
10 . |
49 |
41 |
419 |
|
14 |
71 |
15 |
400 |
|
10 |
50 |
40 |
450 |
|
12 |
18(0,) |
70 |
640 |
|
24 |
46 |
30 |
300 |
|
Продолжение табл. 12
|