Получение и характеристика эпихлоргидрина
Получение эпихлоргидрина. Как видно из схемы (см. стр. 184), получение эпихлоргидрина является важной промежуточной ступенью при синтезе глицерина. Эпихлоргидрин впервые был
Синтезирован в 1854 г. [32] при взаимодействии глицерина с хлористым водородом:
СН2-СН-СНа+ 2НС1 100~120 СН2-СН—СН2+2Н20
TOC \o "1-3" \h \z I - I I III
ОН ОН ОН С1 ОН С1
СН2—CH—СН2 + NaOH 6°"8° CH2-CH-CH2 + NaCl + H,0
III І \/
С1 ОН С1 С1 о
Этот метод получил наибольшее распространение.
Эпихлоргидрин образуется из аллилхлорида после присоединения хлорноватистой ^ислоты через дихлоргидрин и дальнейшего отщепления соляной кислоты известковым молоком [33]:
СН2-СН-СН2 (30%)—
I I I,
С1 ОН С1
|
+Са(ОН)2 |
|
2СН2— СНСН2С1 .20_40 oCj рн=з - г - & |
|
-CaCl2i Н20 ' |
—* сн2-сн-сн2 (70%)- I I I CI CI он
—>- 2Н2С—CH—СН2С1
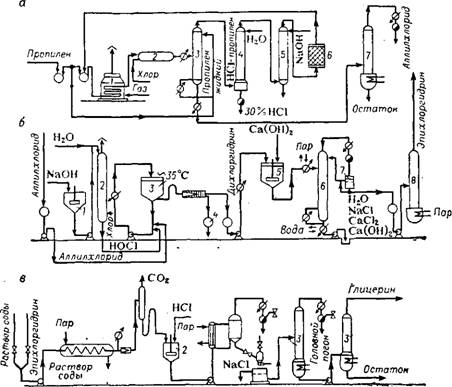
Технологическая схема промышленного метода получения эпи - хлоргидрина из аллилхлорида изображена на рис. 46. Для получения дихлоргидрина аллихлорид вводят в реакцию обмена с хлорноватистой кислотой в водной фазе. Поскольку аллилхлорид плохо растворяется в воде (при 20 °С в воде растворяется только 0,36 вес. % аллилхлорида), необходимо принимать особые меры, чтобы воспрепятствовать прямому контакту хлора и аллилхлорида. В противном случае в результате присоединения хлора образуется слишком большое количество трихлорпропана.
Чтобы не допустить непосредственного соприкосновения хлора с аллихлоридом, хлорноватистую кислоту получают в отдельной башне и работают с большим разбавлением и при низкой температуре. Это делается; для того, чтобы введенный хлор по возможности без остатка перешел в хлорноватистую кислоту:
С12 + Н20 —>- НОС1 + НС1
Хлорноватистую кислоту получают в башне с кислотоупорной облицовкой путем непрерывного введения 1—2%-ного раствора едкого натра и хлора. Образовавшаяся кислота выходит из верхней части башни, затем при тщательном смешении реагирует с аллил - хлоридом. При этом происходит хлоргидрирование. Из процесса постоянно выводится реакционная смесь в количестве, равном объему выходящей из башни хлорноватистой кислоты.
Реакционная смесь пропускается через термодиффузионное разделительное устройство, где отделяются трихлорпропан и тетра-
|
Рис. 46. Технологическая схема получения эпихлоргидрина и глицерина на Промышленной установке: а — хлорирование пропилена: 1 — нагреватель (от 20 до 400 °С); 2 — реактор; 3 — фракционная колонна; 4 — абсорбер; 5 — промывная колонна; в — сушильная башня; 7 — система из трех колонн для перегонки Аллилхлорида. б — хлоргидрирование аллилхлорида: I — растворитель щелочи; 2 — приготовление НОСІ; 3 — реактор; 4 — отбор трихлорпро - пена и тетрахлорпропилоного эфира; 5 — аппарат для отщепления НС1; в — колонна азео - ропной дистилляции; 7 — сепаратор; 8— система из дв^х колонн для обезвоживания и перегонки эпихлоргидрина; в — омыление эпихлоргидрина: 1 — подогреватель (Юо—180 °С, 10 кгс/см2); 2 — нейтрализатор; з — колонна для перегонки глицерина. |
Хлордиизопропиловый эфир. После смешения дихлОргидрина в аппарате с мешалкой с 15%-ным известковым молоком в реакционной колонне осуществляется превращение в эпихлоргидрин и отгоняется азеотропная смесь с водой. Водный слой возвращается в реакционную колонну, а сырой эпихлоргидрин дистиллируется в другой колонне. При такой технологии выход составляет более 90%.
Разработан метод непосредственного получения эпихлоргидрина из аллилхлорида, минуя промежуточную стадию образования гли - цериндихлоргидрина. Он состоит в окислении аллилхлорида пере - кисными соединениями. Однако этот метод до сих пор не внедрен в промышленность. В литературе указаны следующие окислители для этой цели: надуксусная или надпропионовая кислота [34], перекись водорода в присутствии W03 [35], кислород и ацетальдегид [36], пероксикарбоксиминокислота [37], ароматические нитро- «оединения [38], а также каталитическое окисление воздухом на окиси серебра. Окись серебра, нанесенная на губчатый алюминий, предварительно активируется пропусканием над ней водорода и азота [39].
Современное мировое производство эпихлоргидрина оценивается в 300 тыс. т. Исходным продуктом почти всегда служит аллихлорид.
Свойства и применение. Ниже приведены свойства эпихлоргидрина:
Температура плавления, °С,.............................................................. —57,2
Температура кипения, °С.................................................................. 116,11
Плотность
Р§ ................................................................ 1,2040
PS.............................................................................................. 1,2031
Р|5............................................................................................... 1,1732
РІ°о............................................................................................ 1,1633
Показатель преломления
П\о.............................................................................................. 1,43805
Им.................................................................................................. 1,43580
Вязкость, П
При 0°С...................................................................................... 0,0156
25° С................................................................................. 0,0103
Поверхностное натяжение, дин/см
TOC \o "1-3" \h \z при 12,5° С.................................................................................... 39,13
31,0° С................................................................................ 35,48
89,0° С............................................................................... 27,72
Теплота сгорания, кал/г.................................................................... 4524.4
Температура воспламенения, °С....................................................... 40,5
Диэлектрическая проницаемость
При 21,5° С........................................................................................ 20,8
Электропроводность
При 25° С, OM-1-CM-1.............................................................. . 34-Ю"9
О растворимости воды в эпихлоргидрине см. в работе [40], об азеотропных смесях с различными растворителями — в работе [41].
Эпихлоргидрин — химически очень активное соединение, высокой активностью обладают содержащиеся в нем эпоксигруппа и атом хлора. Поэтому эпихлоргидрин приобретает все большее значение, как промежуточный продукт органической химии. Наряду с применением для синтеза глицерина эпихлоргидрин употребляется в большом количестве для производства эпоксидных смол, которые получают взаимодействием дифенилолпропана, синтезируемого из ацетона и фенола, с эпихлоргидрином. Производство эпоксидных смол непрерывно увеличивается. Рассчитывают, что в 1980 г. в США выпуск их достигнет 80 тыс. т. Эпоксидные смолы производятся также в Англии, Голландии, ФРГ, Швейцарии, Бельгии, Франции, Японии, ЧССР и СССР. Кроме того, эпихлоргидрин находит применение в производстве ионообменных смол.
Недавно эпихлоргидрин стали применять для получения хлор - гидринового каучука:
Г-СН2-СН—О—1 I
СН2С1 J П,
С этой целью эпихлоргидрин полимеризуют с алкилалюминием в присутствии хелата металла, иногда вместе с окисью этилена [43, 44]., Хлоргидриновые каучуки разработаны фирмой Hercules Powder (США).
Гомополимер поступает в продажу под названием Гидрин 100, а сополимер с окисью этилена — под названием Гидрин 200 (с недавних пор Херклор X и Херклор Ц). По данным фирмы, эти типы гид - ринов должны обладать такой комбинацией свойств, какой до сих пор не было ни у одного из синтетических каучуков. По жаростойкости и сопротивлению действию озона и других окислителей Гидрин 100 и Гидрин 200 равны этилен-пропиленовым сополимерам. По мас - лостойкости они приближаются к нитрильному каучуку, а по газопроницаемости соответствуют бутилкаучуку.
При реакции эпихлоргидрина с фенолами или спиртами получаются простые глицидные эфиры, применяемые для различных целей в качестве активных растворителей или как стабилизаторы для галогенсодержащих полимеров.
Способность к поликонденсации продуктов взаимодействия эпихлоргидрина и аммиака используется для получения высокомолекулярных смол.