Получение и характеристика аллилхлорида
Метод горячего хлорирования. Как уже было сказано, при хлорировании олефинов с прямой цепью при температурах до 250 °С в результате присоединения хлора к двойной связи образуются преимущественно дихлориды.
|
СН2=С-СН3 + С12 I Сн» |
К совершенно иным продуктам приводит хлорирование олефинов с разветвленной цепью, например изобутилена, который содержит третичный углеродный атом. Здесь замещающее хлорирование происходит с сохранением двойной связи уже при —40 °С без заметного присоединения:
СН2=С—СН2С1 +НС1 I
СНя
Замещающее хлорирование неразветвленных олефинов с сохранением двойной связи впервые удалось осуществить Стюарту и Вей - денбауму [3] на пентене-2. Однако выход был очень низким.
Замещающее хлорирование олефинов с прямой цепью проходит успешно только при достаточно высоких температурах. Исследования Гролля [4—5] (Shell Development Co.), а также Флемминга [6] показали, что в этом случае осуществимо замещающее хлорирование с хорошим выходом и возможно использование этой реакции в промышленности. В 1942—1943 гг. в Германии (Оппау) были пущены полупромышленные установки, а в 1948 г. в Хьюстоне (Техас) введена в действие первая крупная промышленная установка по производству аллилхлорида, перерабатываемого далее в глицерин. При проведении горячего хлорирования в промышленных условиях необходим точный контроль температуры, давления и концентрации [7—9].
С повышением температуры реакция присоединения хлора постепенно сменяется реакцией замещения (табл. 18).
Таблица 18
Зависимость характера реакции хлорирования от температуры
|
210 |
3,44 |
1 |
74,7 |
25,3 |
0,081 |
|
320 |
6,03 |
1 |
22,5 |
77,5 |
0,200 |
|
400 |
6,34 |
1 |
3,8 |
96,2 |
0,550 |
|
510 |
6,32 |
1 |
1,3 |
98,7 |
4,060 |
|
590 |
6,60 |
1 |
0,3 |
99,7 |
10,900 |
|
Средняя температура реакции, °С |
|
Мольное соотношение пропилен : хлор |
|
Содержание хлора в продуктах присоединения, % |
|
Содержание хлора в продуктах замещения, % |
|
Конверсия, г С1 |
|
100 см3-мин |
|
12 Заказ 399 |
- і
|
|
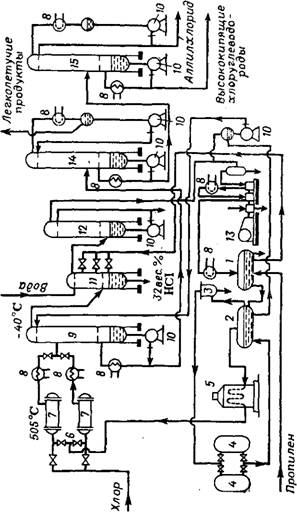
Циже кратко описывается промышленный метод хлорирования олефинов (рис. 44). В специальном смесительном сопле, помещенном в подогревательную печь, перемешивают до получения однородной смеси чистый пропилен, нагретый примерно до 350—400 °С, и чистый безводный, неподогретый хлор. Во избежание накопления хлора и связанного с этим избыточного хлорирования пропилен пропускают через два боковых отвода, а хлор — через главную трубу. Затем реакционная смесь, содержащая пропилен и хлор (лучше всего в отношении 5:1), поступает в реактор, представляющий собой стальной резервуар. Благодаря выделяющемуся при хлорировании теплу в реакторе устанавливается температура 500—530 °С:
С3Н6 + С12 ----- У С3Н5СІ + НС1 + 26 ккал
Время пребывания реакционной смеси в горячей зоне от 2 до 3 с. Увеличение времени пребывания нежелательно, так как аллилхло - рид заметно разлагается при повышенных температурах, а продукты разложения, особенно сажа, загрязняют установку.
Выделившийся при реакции клареновый углерод действует как катализатор хлорирования. Реактор долійен работать почти на максимальной мощности. Выходящая из реактора реакционная смесь содержит аллилхлорид, непрореагировавший пропилен, ненасыщенные моно - и дихлориды, хлористый водород и небольшое количество высоко хлорированных продуктов (табл. 19). При точном соблюдении - температурного режима насыщенные дихлориды образуются в небольших количествах, так как 1,2-дихлорпропан, например, снова разлагается уже при 500 °С.
После охлаждения этих продуктов до 50—120 °С можно\ проводить обработку. Для этого имеется два способа.
|
24,8 15,8 0,7 0,4 4,0 1,8 70,5 82,0 |
Экстракция.' Образовавшийся хлористый водород вымывается водой в выложенной кирпичом башне. При этом давление паров хлоридов настолько высоко, что конденсация еще не происходит. После водной промывки газ имеет в среднем следующий состав:
Вес. % Мол. %
Аллилхлорид.............................................
2-Хлорпропен-1.........................................
Дихлорпропан+дихлорпропилен. . Пропилен
В отделителе при 7—10 °С конденсируется до 50% хлоридов (сырой продукт I). Оставшиеся хлориды абсорбируются из пропилена углеводородами, например октаном (сырой продукт II), а затем отгоняются из абсорбционной жидкости. Насыщенный октаном неабсорбированный пропилен выходит из абсорбера и после проточного охлаждения рассолом снова возвращается в цикл. На трех - четырех специальных колоннах (лучше всего из никеля) из продуктов I и II периодически или непрерывно выделяется чистый аллилхлорид.
|
Таблица 19 Перечень возможных продуктов, образующихся при горячем (500—530 °С) хлорировании пропилена,
|
Конденсационный метод. Этот метод считается лучшим и потому внедрен в промышленность. Реакционные газы направляются прямо из реактора, где проводилось хлорирование, в так называемый форфракционатор, где в результате охлаждения жидким пропиленом при —40 °С конденсируются органические хлориды. Пропилен вместе с образовавшимся при реакции хлористым водородом поступает в HCl-абсорбер, где хлористый водород поглощается водой. Пропилен после щелочной промывки возвращается в цикл [10, И]. Зависимость среднего выхода продуктов (в расчете на израсходованный пропилен) от температуры показана на рис. 45.
Наиболее оптимальным оказалось соотношение пропилен : хлор = = 5 : І. При меньшем соотношении увеличивается содержание ненасыщенных дихлоридов, при более высоком соотношении, ХОТЯ и повышается выход аллилхлорида, но существенно увеличивается нагрузка на систему циркуляции, особенно на абсорбер, что приводит к росту эксплуатационных расходов.
Очень важно применять высокочистый пропилен и, особенноt очень чистый и безводный хлор. Любая органическая примесь хлорируется, что вызывает повышение расходов хлора в результате образования побочных продуктов. Также не следует использовать смеси пропана с пропиленом, так как это приводит к образованию трудно- отделяемых монохлоридов [12].
Подогреватель пропилена, смесительное сопло и реактор могут быть выполнены из обычной стали, так как в местах контакта с хлором образуется защитная пленка из кларенового углерода. НС1- Абсорбер лучше всего изготавливать из кирпича, пропитанного, силикатом натрия, или из стойкого к химическим воздействиям камня. Пригодны также игурит и керамика. Перегонная аппаратура может быть выполнена из материалов хастеллой А и дурихлор, но чаще употребляют монельметалл или никель. Метод горячего хлорирования за последние годы в основном не изменялся, но появилось множество вариантов конструкции реактора. При этом стремились снизить образование продуктов присоединения при смешении пропилена с хлором. Например, сконструирован реактор типа циклона, позволяющий работать с более низким соотношением пропилен: хлор (3 : 1) [13—15]. В этот реактор оба газа вводятся раздельно по касательной к противоположным сторонам циклона. Предложены также реакторы шарообразной, эллипсоидной и других форм, обеспечивающие хорошее смешение без мертвых пространств и выходы не менее 80% [16—18] .
Для улучшения теплового баланса предлагается реактор с двойными стенками, в котором отработанные газы быстро нагревают Свежий газ до оптимальной температуры 382—494 °С. В таком реакторе при 485 °С и времени контакта 2,13 с получается 79,8 мол. % аллилхлорида и 3,04 мол.% 1,2-дихлорпропана [19].
Следующая возможность улучшить смешение компонентов реакции состоит в том, чтобы впрыскивать в камеру для хлорирования хлор по оси, а пропилен по касательной [20]. Наконец, предлагается установка для хлорирования, на которой работает вертикальный реактор и применяются агенты теплопередачи [12].
|
J 00 АОО 500 |
|
Температура,°С |
|
Рис. 45. Влияние температуры реакции на выход продуктов горячего хлорирования пропилена при мольном соотношении пропилен : хлор=4 :1 (заштрихована область оптимальных температур). 1 — аллилхлорид; 2 — 1,2-дихлорпро - пан; S — высококипящие продукты; 4 — легкокипящие продукты. |
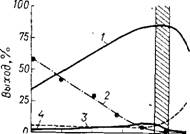 Были проведены расчеты по методу градиента с целью оптимизации температуры, давления, состава впрыскиваемого продукта и
Были проведены расчеты по методу градиента с целью оптимизации температуры, давления, состава впрыскиваемого продукта и
времени реакции. Если хлорирование проводится в присутствии 1,2-дихлорпропана, то увеличивается выход аллилхлорида [23].
Другие методы. Аллилхлорид получают также пиролизом 1,2- ди - хлорпропана [24]. При этом образуется 55—70% аллилхлорида, 3.0—40% смеси цис- и яграис-изомеров 1-хлорпропена-1 и 5% 2-хлор - пропена-1.
При 250—400 °С в присутствии различных катализаторов [25] преимущественного образования аллилхлорида не наблюдалось, при 560—640 °С выход аллилхлорида достигал примерно 60% [26]. В качестве катализаторов пиролиза 1,2-дихлорпропана в аллилхлорид предложены ВаС12, СоС12, NiCl2, ZnCl2, MnCl2, FeCl3 и CuCl2 на активированном угле, силикагеле или А1203 [27].
Можно осуществлять также хлорирование пропана или 1-хлор - пропана при 500—700 °С в присутствии катализатора [28]. Наконец, при горячем хлорировании пропилена можно использовать вместо С12 смесь HG1 и О 2 или воздуха (катализатор LiCl, благородные металлы, или соединения теллура на пемзе) [29].
Простой диаллиловый эфир, образующийся как побочный продукт при превращении аллилхлорида в аллиловый спирт, может быть снова переведен в аллилхлорид с 88%-ным выходом посредством пропускания с HG1 над CuCl при 15—40 °С и под давлением [30] или при 55 °С [31].
Свойства и применение аллилхлорида. Ниже приведены свойства аллилхлорида:
Температура плавления °С................................................................ —136,4
Температура кипения, °С
TOC \o "1-3" \h \z при 744 мм рт. ст....................................................................... 44,5
751 мм рт. ст..................................................................... 44,9
760 мм рт. ст.................................................................... 4-5,1
772,5 мм рт. ст........................................................................ 46,7
Плотность
Р2 ................................................................................................... 0,9637
РІ5 .............................................................................................. 0,9442
РІ0 .............................................................................................. 0,9379
Pf................................................................................................ 0,9311
Рзо............................................................................................... 0,9245
Показатель преломления
........................................................................................... 1,4188
Reg............................................................................................... 1,4154
. ng.................................................................................................. 1,4130
Дипольний момент, D............................................................................... 2,02
Вязкость при 30° С, П............................................................................ 0,00336
Критическая температура, °С.................................................................. 240,7
Теплота испарения, кал/моль................................................................... 6940
Теплота сгорания, ккал/моль................................................................... 440,8
Удельная теплоемкость (пара), кал/(г-°С)
При —17,8 °С................................................................................ 0,222
37,8 °С............................................................................. 0,230
93,3 °С.................................................................................. 0,224
149 °С............................................................................... 0,212
Пределы взрываемости в смеси с воздухом, объемн. %
Верхний........................................................................................ 11,51
Нижний......................................................................................... 3,28
Температура воспламенения, °С.............................................................. —26,7
Диэлектрическая проницаемость
Пар при 19° С и 760 мм рт. ст. ....................................................... 1,0128
Жидкость при 19,5° С....................................................... : . . 7,3
Растворимость при 20° С, вес. ч./ЮО вес. ч.
Воды в аллилхлориде '............................ '.................................... 0,08
А л ли л хлорида в воде................................................................. 0,36
Формула давления пара р (в мм рт. ст.) и значения давления пара при различных температурах приведены ниже:
|
2142 R P = 20,89279 - —у - - 4,4182 lg Т
|
Ниже приведены температуры кипения и содержание аллил - хлорида в двойных азеотропних смесях со следующими веществами::
|
Содержа |
Содержа |
||||
|
Т. |
Ние |
Т. |
Ние |
||
|
Кип., |
Алилхпо- |
Кип., |
Адил хло |
||
|
°С |
Рида, |
°С |
Рида, |
||
|
Вес, % |
Вес. % |
||||
|
Вода............................... |
43,0 |
97,8 ' |
Прошю нитрил |
....................... 44,95 |
80 |
|
Пентан........................... |
35,5 |
28 |
Метилаль. . |
....................... 41,4 |
20 |
|
Циклопентан . . . . |
44,3 |
63 |
Ацетон. . . |
....................... 44,6 |
90 |
|
Метиловый спирт. . |
39,85 |
90 |
Муравьиная |
Кислота 44,4 |
92,5 |
|
Этиловый спирт, . |
43,5 |
95 |
Этилформиат |
....................... 45,2 |
90 |
|
Изопропиловый спирт |
45,1 |
98 |
Сероуглерод. |
....................... 41,2 |
50 |
Аллилхлорид получил довольно большое значение благодаря легкости получения и высокой реакционной способности. Он является исходным продуктом при введении аллиловой группы в другие - соединения: сложные аллиловые эфиры (например, аллилфталат), аллиламины, аллилизотиоцианат (искусственное горчичное масло CH2=CHCH2NCS). В результате реакции обмена аллилхлорида с тиомочевиной образуется так называемый тиозинамин, применяемый в фотографии. Однако большая часть аллилхлорида используется для получения эпихлоргидрина и глицерина. Некоторое^
Количество аллилхлорида перерабатывается в аллиловый спирт, а также в аллиловый крахмал.
При реакции обмена аллилхлорида с аммиаком (целесообразно проводить эту реакцию в автоклаве с мешалкой при 100 °С под давлением) в зависимости от добавляемого количества аммиака получается моно-, ди - или триаллиламин [147]. Преимущественно получают моноаллиламин, и в этом случае избыток хлористого аммония оказывает самое благоприятное действие [148]. Моноаллиламин можно синтезировать также путем гидролиза соляной кислотой ал лилового горчичного масла, полученного из аллилхлорида под дейстЬием роданидов щелочных металлов или аммония [149]. Моно - и диаллиламины являются промежуточными продуктами для химических синтезов.
В последнее время приобрел значение аллиловый крахмал, образующийся при взаимодействии аллилхлорида или аллилбромида с крахмалом в присутствии щелочи [150]. Аллиловый крахмал, иногда вместе с каучуком, применяется для получения покрытий, клеев и пластмасс [151]. Аллилсахароза, являющаяся продуктом реакции сахарозы и аллилхлорида, после полимеризации тоже может быть использована для производства покрывных материалов [152].
Аллилхлорид используется для синтеза аллилсиликонов [153] и аллетрина — синтетического средства для борьбы с вредными насекомыми [154].
Аллилхлорид полимеризуется в присутствии катализаторов Фри - деля — Крафтса [155]. Полимеры применяются для пропитки бумаги, дерева и других материалов. В результате полимеризация в присутствии радикальных катализаторов (перекиси бензоила) получаются полимеры, прйменяемые в качестве пластификаторов, клеев и смазок, а также для получения лаков и пропиток [156]. При нагревании аллилхлорида с водорастворимым полисульфидом [157], а также 1,2,3-трихлорпропаном [158] образуются продукты подобные тиоколам.
Смесь из дихлорпропана и дихлорпропенов, получаемая как побочный продукт при горячем хлорировании пропилена, широко употребляется под названием «Д-Д» в качестве ценного средства для окуривания почвы с целью борьбы с нематодами. (250—500 кг/гектар) [159-160].
На схеме показаны различные пути синтеза эпихлоргидрина и глицерина из аллилхлорида.