ПОЛУЧЕНИЕ АЦЕТОНА
Самый старый метод промышленного производства ацетона заключался в сухой перегонке ацетата кальция, получающегося при нейтрализации известью древесного уксуса, который образуется при коксовании древесины [1]. Сейчас этот метод уже не находит применения, так как ацетон в этом случае содержит слишком много примесей, а исходный материал дефицитен.
Известны также способы получения ацетона путем бактериального расщепления углеводов (крахмала, Сахаров, мелассы), причем в качестве побочных продуктов образуются бутиловый или этиловый спирт [2—4]. Ацетон и бутиловый спирт получаются в мольном соотношении от 2 : 1 до 3 : 1.
В настоящее время этот метод в США еще занимает определенное положение для получения некоторого количества ацетона.
В Германии был разработан технологический процесс производства ацетона на основе уксусной кислоты [5]. При 400 °С через контакты из церия пропускали уксусную кислоту:
2Сн3соон 400°с' СН3С0СН3 + С02 + Н20
Такой ацетон отличается особой чистотой.
Ацетон производят также из ацетилена прямым синтезом:
2СН=СН + ЗН20 --------- ► СН3СОСН3+С02 + 2Н2 + 40 ккал/моль
Ацетилен вступает во взаимодействие с водяным паром при 450 °С в присутствии катализаторов (в частности ZnO или Fe203 — ZnO) [6].
В США фирма Celanese Corp. производит ацетон наряду с другими кислородсодержащими соединениями путем окисления смеси бутан — пропан небольшим количеством чистого кислорода при 330—370 °С и 7—10 кгс/см2. На долю ацетона приходится 5—7% общего количества оксидата [7]. Более высокий выход получают при использовании изобутана.
7.1.2. Получение из изопропилового спирта[2]
До настоящего времени основное количество ацетона получают все еще дегидрированием изопропилового спирта [13]:
СН3СН(ОН)СН3 —СН2СОСН3 + Н2-15,9 ккал/моль
Дегидрирование протекает при 35Q—400 °С в присутствии таких катализаторов, как сплав железо — медь — цинк [8], окись цинка или окись цинка с 4,5% углекислого натрия [9], медь, свинец и т. д. [10].
|
Водород
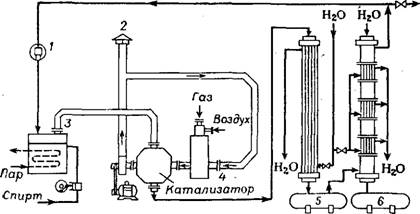
Рис. 38. Схема установки по производству ацетона: 1 — компрессор для водорода; 2 — система регенерации катализатора; 3 — испаритель; 4 — камера сгорания; 5 — емкость для сырого ацетона; 6 — емкость для раствора ацетона в воде. |
Упрощенная схема установки для производства ацетона из изопропилового спирта [11] приведена на рис.38. Изопропиловый спирт обрабатывается водородом при высоких температурах, причем 1 объем водорода поглощает примерно 1 объем паров изопропилового спирта. Смесь при 380 °С проходит через кожухотрубный реактор с трубами из хромоникелевой стали, в котором находится катализатор в виде кусочков пемзы, пропитанной ацетатом цинка (~7% ZnO). Максимальная конверсия изопропилового спирта составляет около 97% [12], время контакта 1 с. Реакционные газы охлаждают, образующийся 20%-ный ацетон концентрируют и очищают перегонкой. Водород промывают от ацетона в противотоке воды, концентрация водорода ~99%. Регенерацию катализатора проводят через 10 суток, выжигая загрязнения смесью азота с 2% кислорода. Срок службы катализатора около 6 месяцев.
В последнее время все чаще получают ацетон путем окисления изопропилового спирта воздухом; при этом образуется также перекись водорода:
СН3СН(0Н)СНз+02 —► СН3С0СНз + Н202
Этот метод играет определенную роль при производстве глицерина в отсутствие хлора.