ОКИСЬ ПРОПИЛЕНА
Окись пропилена была открыта Озером [1], когда он обрабатывал і-хлорпропанол-2 едким кали:
Т7лтт
C1CH2CH(0H)CHS НаС-------- CHCHs
О
Аналогичный результат получил Крассуский [2] при действии на 1-хлорпропанол-2 окиси свинца и воды. В литературе имеется ряд работ по синтезу окиси пропилена [3—9].
В настоящее время окись пропилена получают двумя путями: через пропиленхлоргидрин и прямым окислением пропилена в окись пропилена. В промышленном масштабе окись пропилена производили до сих пор только через хлоргидрин.
Данный метод остается пока наилучшим, т/ік как он дает хороший выход (85—90%); при прямом окислении выход пропилена достигает только ~35%. Кроме того, при переходе от хлоргидринного метода к прямому окислению при получении окиси этилена можно использовать освободившиеся установки для производства окиси пропилена.
4.1. ПОЛУЧЕНИЕ ОКИСИ ПРОПИЛЕНА ЧЕРЕЗ ПРОПИЛЕНХЛОРГИДРИН
Метод получения окиси пропилена путем присоединения хлорноватистой кислоты к пропилену, впервые подробно описанный Мар - ковниковым [10], до сих пор является самым распространенным. Протекающие при этом реакции можно записать следующим образом:
С12+Н20 НОС1 + НС1
,—>- С1СН2СН(ОН)СН,
2СН2=СНСН3 + 2НОС1—
1--- СН2(ОН)СНС1СН3
С1СН2СН(ОН)СНз + СН2(ОН)СНС1СН3+ Са(ОН)2 —► —► 2Н2С—СНСН3 + СаС12 + Н20 О
Мольное соотношение а - и p-пропиленхлоргидринов составляет 9 : 1..
В результате воздействия элементарного хлора на пропилен и хлоргидрин в качестве побочных продуктов образуются дихлор - пропан и дихлордиизопропиловый эфир:
СН2С1СН(ОН)СНа + С12 —► СН2С1СН(ОС1)СН3 сн2С1СН(ОС1)СН3+СН2=СНСН3 —► СН2С1СН(СН3)-0-СН(СН3)СН2С1 СН2=СНСН3 + С12—СН2С1СНС1СН3
Поскольку присоединение хлора идет значительно быстрее, чем присоединение хлорноватистой кислоты [11], нужно по возможности подавлять реакцию хлора с пропиленом. Для этого взаимодействие хлора с водой следует проводить в отдельной колонне. Собственно хлоргидринирование происходит в следующей второй колонне. Большое значение имеет хороший контакт между жидкой фазой и углеводородом. Целесообразно выбрать двухкамерную установку.
Недиссоциированная кислота всегда присоединяется по двойной связи. В присутствии буферного бората (рН = 10) хлоргидрин практически не образуется, между тем как в кислой среде (рН = = 4,7) наступает хлоргидринирование. Увеличение диссоциации равносильно уменьшению выхода хлоргидрина.
Так как степень диссоциации слабых кислот возрастает пропорционально температуре, то хлоргидринирование при повышенных температурах идет, в принципе, хуже.
Константа диссоциации НОСІ при 25 °С равняется 1,05-10'7. Если определить с помощью термодинамических характеристик показатель константы диссоциации для 65 °С, то можно установить изменение только на одну десятую степени, которое так мало, что не имеет практического значения.
По теории реакция взаимодействия должна проходить с образованием 1 моль хлоргидрина на 1 моль НС1. Однако аналитическое исследование процесса свидетельствует о избытке соляной кислоты, получающейся по следующему механизму:
СН2С1СН(ОН)СН3 + С12 —>- СН2С1СН(ОС1)СН3 + НС1
СН2С1СН(ОС1)СН3 + СН2=СНСН3------------- ► СН2С1СН(СН3)—О—СН(СН3)СН2С1
• Соотношение пропиленхлоргидрина и соляной кислоты зависит от температуры и концентрации хлоргидрина, соотношения пропилен: хлор, концентрации пропилена в исходном газе и от аппаратурного оформления процесса. С повышением температуры растет избыточное количество соляной кислоты, которое может достигнуть, например, при 75—80 °С примерно 50%. При 40 °С избыток колеблется в пределах 6—10% при концентрации пропиленхлоргидрина 50 г/л. Омыление пропиленхлоргидрина происходит так же, как омыление этиленхлоргидрина, однако оно протекает примерно в 20 раз быстрее.
Уменьшение констант скорости во время реакции обмена можно объяснить протеканием вторичных реакций. Действительно, окись пропилена реагирует с образованием промежуточного соединения, которое затем медленнее омыляется. Это нужно учитывать при промышленном производстве и быстро удалять образовавшуюся окись пропилена из реакционного раствора [12].
При промышленном получении процесс лучше всего идет в реакторе с двойной камерой, который применяется для превращения этиленхлоргидрина [13, 14]. При сравнимых рабочих условиях выход в таком реакторе составляет 87,5% пропиленхлоргидрина с одновременным образованием 11,0% пропилендихлорида и 1,5% ди - хлордиизопропилового эфира. В противоположность этому реактор с одной камерой дает только 69,2% продукта, одновременно 21,6% прореагировавшего пропилена высаждается в виде пропилендихлорида, а 9,2% превращается в дихлордиизопропиловый эфир. Это свидетельствует о несомненном превосходстве двухкамерной системы для процесса превращения пропилена в хлоргидрин. В первой камере такой установки хлор растворяется вместе с подаваемой свежей водой в циркулирующем пропиленхлоргидрине, разбавленном водой. После введения хлора- смесь подается во вторую камеру, где попадает в поток пропилена, и реакция заканчивается.
При хлоргйдринировании пропилена нельзя избежать образования побочных продуктов, так как в растворе хлоргидрина наряду со свободной НОСІ имеются еще свободные НС1 и С12. Реагируя с пропиленом, С12 вызывает образование 1,2-дихлорпропана, а в результате реакции с пропиленхлоридрином получается дихлордиизопропиловый эфир.
Как и в случае этиленхлоргидрина, для подавления побочных реакций желательно работать при температуре ниже 50—60 °С. При этих условиях этилендихлорид можно в значительной степени вывести из верха колонны газовым потоком и предотвратить образование второй фазы в реакторе. При реакции превращения пропилена более тяжелый дихлорид не позволяет работать с чистым пропиленом, что было бы выгодно. Тем не менее, дихлорид можно отогнать во время реакции обмена при 50—60 °С, использовав поток углеводорода, содержащий более 45% пропилена. Не вступивший в реакцию газ содержит инертные газы: метан, этан, пропан или азот. При начальном контакте с пропиленовым потоком водная фаза должна содержать не более 0,5 г/л хлора [12].
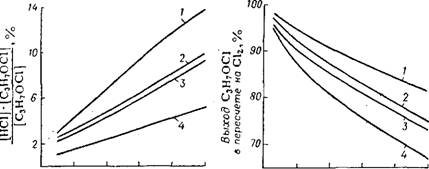
Концентрация самого раствора хлоргидрина также не должна значительно повышаться, так как это способствует протеканию побочных реакций (рис. 27, 28).
Из этого следует, что концентрацию продукта нельзя привести к экономическому показателю при однократном прохождении череэ
аппарат и приходится использовать вышеописанную циркуляционную систему.
|
0 20 40 60 80 100 Концентрация С3Н7ОС1, г/л |
|
Рис. 27. Влияние избытка НС1 на образование пропиленхлоргидрина: 1 — 1 г/л хлора, 45 °С; 2 — 0,15 г/л хлора, 45 "С; 3 — 1 г/л хлора, 35 "С; 4 — 0,15 г/л хлора, 35 °С. |
|
0 20 40 60 80 100 Концентраций С3Н7ОС1, г/л |
Концентрация пропиленхлоргидрина на выходе из реактора влияет на конечный результат в гораздо большей степени, чем при реакции обмена этилена. При 45 °С и концентрации хлора 0,15 г/л в случае с пропиленом получается 97% качественного продукта, если
Рис. 28. Зависимость выхода пропиленхлоргидрина в пересчете на С12 от конечной концентрации пропиленхлоргидрина:
1 — 0,15 г/л хлора, 35 °С; 2 — 0,15 г/л хлора, 45 °С; 3 — 1 г/л хлора, 35 °С; 4 — 1 г/л хлора, 45 °С.
Общая концентрация пропиленхлоргидрина ниже 5 г/л. При концентрации пропиленхлоргидрина 50 г/л выход снижается до 89,5%, а при 70 г/л выход примерно на 7%- ниже теоретически вычисленного (87%). Понижение, температуры до 35 °С приводит к незначительному увеличению выхода. Дальнейшее уменьшение температуры не повышает выхода, а рри 15 °С наблюдаются потери продукта из-за затруднений с аппаратурным оформлением.
При двухкамерной системе для производства хлоргидрина нужен реакционный объем порядка 1,2 м3/(т-сут).
Омыление пропиленхлоргидрина в окись пропилена происходит в основном анадогичцо образованию окиси этилена. Однако здесь можно использовать только известковое молоко, содержащее не более 1% MgO, иначе - будет преобладать образование пропионового альдегида.
Скорость образования окиси пропилена значительно ниже (примерно в 10 раз), чем при производстве окиси этилена. Однако пока^ зано, что образование пропилена в основном замедляется присутствием продукта в реакционной среде. Поэтому для ускорения
Реакции необходимо максимально быстро выделять продукт из системы по мере его образования.
Описан [16] двухколонный реактор для получения 93,5% про - пиленхлоргидрина и 6% 1,2-дихлорпропана. Предложено также вводить хлор и пропилен в водную хлорноватистую кислоту в различных местах колонного реактора [15, 17]. Рекомендуется и последовательное включение нескольких реакторов в каскад, причем в первый реактор загружают воду и хлор, а в последующие вводят реакционную смесь из предыдущего реактора и пропилен. Такой режим работы дает хороший выход [18]. Описан метод одновременного воздействия хлора, воды и пропилена друг на друга [19—21].
Обзор лабораторных опытов по получению пропиленхлоргидрина сделан Мейем и Франке [9]. Необязательно использовать чистый пропилен для хлоргидринирования, даже лучше разбавлять его пропаном [22—25]. Предложен способ проведения реакции пропилена с хлором даже в 20—80%-ной серной кислоте при 10—И °С [26].
Окись пропилена можно получать и совместным хлоргидриниро - ванием этилена и пропилена, так как образующийся пропиленхлор- гидрин омыляется в известковом молоке примерно в 20 раз быстрее, чем этиленхлоргидрин [27].
Показатель рН имеет решающее значение для направленного отщепления НС1 от пропиленхлоргидрина [28]. При рН = 9 - f - 12 образуется окись пропилена, при рН = 9 -4- 7 — пропиленгликоль, в очень кислой среде — ацетон. Увеличение мольного соотношения Са(ОН)2 : окись пропилена от 1 : 1 до 2 : 1 повышает выход пропи - ленгликоля, уменьшает выход окиси пропилена и не влияет на выход карбонильных соединений. Оптимальные параметры производства окиси пропилена приведены ниже [28] *
Температура, РС......................................
Концентрация Са(ОН)2, г/л. . .
РН. .....................................................
Подвод тепла, ккал/моль C3H7OCI Концентрация C3H7OCI
При этих условиях выход продуктов реакции составляет (в мол. %):
TOC \o "1-3" \h \z Окнсь пропилена................................................................. 91
П ропиленглнколь................................................................. 7
Карбонильные соединения.................................................... 2
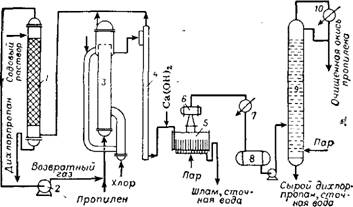
Схема установки для получения окиси пропилена методом хлор - гидрирования показана на рис. 29. Для получения хлорноватистой кислоты в нижнюю часть колонны 3 с кислотостойкой облицовкой вводят газообразный хлор.
Газообразный пропилен, смешанный в незначительном избытке с циркулирующим газом, подается в другом месте колонны 3. Из колонны часть реакционного раствора отводится для дальнейшей переработки в дегазационную колонну 4 с аналогичной кислотостойкой облицовкой. Большая часть однако циркулирует через перепускное устройство. В верхнюю часть перепускной трубы подается свежая вода в таком количестве, чтобы концентрация хлоргидрина в колонне не превышала 40 г/л, а содержание свободного хлора было
|
Рис. 29. Схема установки по производству окиси пропилена: 1 — промывная колонна с содовым раствором; г — компрессор; з — колонна для хлоргидрина; 4 — дегазационная колонна; 5 — гидролизер; в — дефлегматор; 7 — конденсатор для неочищенной окиси пропилена; 8 — емкость для неочищенной окиси пропилена; 9 — тарельчатая колонна; 10 -— конденсатор для очищенной окиси пропилена, ч |
Не выше 0,3 г/л. Температура реакции в колонне должна поддерживаться в пределах 40—45 °С. Отходящие с верха колонны 3 и дегазационной колонны 4 непрореагировавшие пропилен и пропан вместе с хлористым водородом, смешанным с дихлорпропаном, направляются под небольшим вакуумом в куб промывной колонны 1, заполнен? ной кольцами Рашига. Подаваемый в верхнюю часть промывной колонны раствор соды нейтрализует реакционную смесь и одновременно поглощает дихлорпропан. Нейтрализованная смесь пропан — пропилен возвращается через компрессор 2 в колонну 3.
Для предотвращения накопления инертных газов осуществляется постоянный сброс газа перед подачей циркулирующей газовой смеси на реакцию. Если содержание пропилена в газе, вводимом в колонну 3, не превышает 40 объемн. %, то получают оптимальный результат.
Из дегазационной колонны 4 реакционная смесь поступает в гидролизер 5 через перепускное устройство, где добавляется 10-20%- ное известковое молоко. Гидролизер представляет собой горизонт тальный стальной резервуар, снабженный перегородками. В каждую ячейку, образованную перегородками, подается пар и реакционная смесь нагревается до 60—80 °С. При этом происходит моментальное превращение пропиленгидрина в окись пропилена, которая испаряется и вместе с водяным паром и дихлорпропаном поступает в дефлегматор 6, где часть водяного пара конденсируется и возвращается в цикл. В холодильнике 7 дистиллят охлаждается, после чего направляется для хранения в промежуточную емкость 8.
В ректификационной колонне 9 с 50 теоретическими тарелками фракционируют сырую окись пропилена. Из верхней части выходит при 34 °С 98 %-ная окись пропилена, а в кубе колонны остаются вода, дихлорпропан с небольшими примесями дихлордиизопропилового эфира, прохшоновый альдегид и пропиленгликоль. Дихлорпропан из куба колонны периодически удаляют осушкой хлоридом кальция. Выход окиси пропилена составляет около 80% по отношению к исходному хлору. Установка работает непрерывно и, несмотря на небольшие размеры аппаратов, имеет высокую производительность.