ЛЕВОПИМАРОВАЯ КИСЛОТА
Левопимаровая кислота имеет следующие константы:
Темп. пл. 151,5—152° С [а}®— 288,0° (в спирте) 119); ее метиловый эфир темп. пл. 63—64° С: D™ 0,9981, п^5 1,5083, 1,5074, [а] —268° (в эфире) [154].
Продукт присоединения малеинового ангилрида, темп. пл. 226 -227"С, [а]с — 29,0° (в хлороформе), —28,9° (в метиловом спирте) 1154];
Метиловый эфир продукта присоединения, темп. пл. 214—215° С
[43J.
Впервые левопимаровая кислота была выделена А. Веетер- бергом в 1887 г. J158]. При исследовании маточных растворов, оставшихся после выделения натриевых солей декстропимаро - вой кислоты, он обнаружил левовраіцаюіцую кислоту, кристаллизующуюся в больших призматических кристаллах, темп. пл. 140—150°С и (a]D — 272° (в спирте). Эта кислота им была названа р-пимаровой, а впоследствии — левопимаровой из предположения, что она является оптическим антиподом декстропи - маровой кислоты, однако дальнейшие исследования этого не подтвердили. А. Вестерберг показал также, что левопимаровая кислота имеет эмпирическую формулу С20Н30О2.
В 1921 г. Г. Дюпон [121], исследуя состав галлипота P. maritime, показал, что основная трудность выделения из него левопимаровой кислоты заключалась в ее способности изомери - зоваться в абиетиновую кислоту под воздействием сильных минеральных кислот и ледяной уксусной кислоты. Он разработал методику разделения смоляных кислот через натриевые соли с последующим разложением их углекислым газом или разведенной уксусной кислотой. Способ выделения левопимаровой кислоты, предложенный Г. Дюпоном, позднее усовершенствовали С. И. Палкин и Т. X. Гаррис [140].
Левопимаровая кислота была получена из живицы P. siivc - stris В. Н. Кресгинеким, С. С. Малевской. Н. Ф. Комшиловым, Е. В. Казеевой [43], Б. А. Арбузовым {43], И. И. Бардышевмм и В. В. Кохомекой [4]. Кроме того, она была найдена в живице P. palustris [43, 126], P. caribaea [154], P. insignis [43], Pieea excelsa [43], P. Pallasina Lamb. [19]. Можно предположить наличие левопимаровой кислоты во многих других видах хвойных.
С. И. Палкин и Т. X. Гаррис (1934) [140] впервые обратили внимание исследователей на то, что очистка смоляных кислог при помощи солей аминов дает хорошие результаты. В 1948 г. Г. X. Гаррис и Т. Ф. Сандерсон [130] выделили чистую левопимаровую кислоту, темп. пл. 150—152° С и [а]^—275,0° (в спирте) путем перекристаллизации из ацетона бутаноламиновой соли левопимаровой кислоты с последующим разложением этой соли борной кислотой.
И. И. Бардышев с сотр. во многих случаях {4, 6, 10, 12, 13, 14, 19] для очистки и выделения смоляных кислот пользовались борниламиновьши солями. Особенно хорошие результаты были получены ими при выделении левопимаровой кислоты [4, 10, 14, 19]. И. И. Бардышев, X. А. Черчес и Л. И. Ухова [19] предложили следующий способ получения чистого образца левопимаровой кислоты: эфирный раствор живицы нейтрализовали эфирным раствором борниламина или смесью борниламина и нео - борниламина при молярном соотношении, равном 1:1. Смесь энергично перемешивали. Через некоторое время выпадали соли аминов, которые промывали на'фильтре большим количеством серного эфира. Далее тонкий порошок соли суспензировали в эфире и разлагали избыточным количеством водной суспензии борной кислоты или 1%-ным водным раствором уксусной кислоты. Эфирный раствор смоляных кислот промывали водой, эфир отгоняли, а левопимаровая кислота перекристаллизовыва - лась из спирта, темп. пл. 151,5—152° С, {a]20D—288° (в спирте). Положение максимума поглощения в ультрафиолетовом спектре 272,5 тц при коэффициенте удельного поглощения a 19,3.
Наличие двух двойных связей в молекуле левопимаровой кислоты доказано гидрированием ее до насыщенной тетрагидро - левопимаровой кислоты С2оН3402, темп. пл. 195—197° С, [а]ю+7° (в спирте), ее метиловый эфир темп. пл. 76—77°С, d491 0,9705, «о91 1, 4344, [а]х>+3° (в спирте). Гидрирование идет при использовании платинового катализатора в растворе уксусной кислоты.
Количественно протекающие при комнатной температуре реакции присоединения к левопимаровой кислоте малеинового ангидрида, я-бензохинона. a-нафтахинона, р-нафтахинона н чругих реагентов диенового синтеза [43] доказывают, что лево - ннмя'рог. аи кислота имеет конъюгированную систему двойных связей в одном кольце.
Наличие сопряженных двойных связен в одном кольце подтверждают и данные исследования спектра поглощения в ультрафиолетовой части для левопимаровой кислоты. Абсорбционный максимум поглощения по Крафту [43] 272,5 тц, по И. И. Бардышеву и В. В. Кохомской [43] 272,5 тц при коэффициенте удельного поглощения a 19,3.
Как уже выше указывалось, все кислоты типа абиетана (см. табл. 23) имеют строение, отвечающее формуле (XXIX), отличаются между собой только различным взаимным расположением двойных связей і молекуле кислоты.
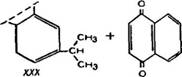
Л. Ружичка с сотр. [43] предложили две формулы строения для левопимаровой кислоты (XXX) и (XXXI).Эти формулы подтверждены другими исследователями [126].
НООС СН.
3
НООСч/СН3
|
/ч |
|
СН, |
|
СН3 |
|
С |
|
С |
|
/ —СН |
|
/ -СН |
|
Сна |
|
XXX |
|
XXXI |
|
Сня |
В 1940 г. С. С. Малевской [43, 59] предпринято обстоятельное изучение состава живицы и строения левопимаровой кислоты. Левопимаровая кислота озонировалась, озонид разлагался водой. В продуктах распада озонида обнаружены изо - масляная и диоксикетоальдегидрокарбоновая кислоты С15Н22О6
Количество летучих кислот составляло 57% от вычисленного, а количество изомасляной кислоты ■— 33% от летучих кислот.
Кислота СібНггОб (XXXII) при окислении влажной окисью серебра дала диоксикетодикарбоновую кислоту С15Н22О7
Наличие в продуктах расщепления левопимаровой кислоты больших количеств изомасляной кислоты, а также дикарбоно - вой кислоты (XXXIII) с 15 углеродными атомами показало, что левопимаровой кислоте принадлежит строение (XXX).
НООС. СН3
/
|
Ноос^ сн.: |
НООС СП
Ч / гч,
|
О |
|
СН., |
|
CHS |
CHJ
|
Ио/ хс |
НО/ЧСООН
Н
XXXII
XXXIII
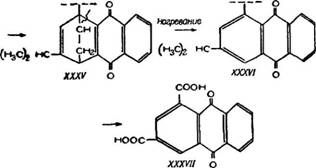
Б. А. Арбузов [43] получил продукт присоединения а-нафта - хинона к левопимаровой кислоте С30Н36О4 (XXXIV), темп. пл. 185° С, темп. пл. его метилового эфира 195° С. Далее, этот продукт (XXXIV) он дегидрировал (XXXV), подверг пиролизу (XXXVI) и затем окислил азотной кислотой. В результате окис
ления получена антрахинон-1,3-дикарбоновая кислота (XXXVII)., темп. пл. 339—340° С, которую затем синтезировал.
|
|
|
|
Описанные выше реакции являются убедительным подтверждением формулы строения левопимаровой кислоты (XXX).
В. Зандерман, изучая строение левопимаровой кислоты, также доказал, что ее строение отвечает формуле (XXX).