Электронный Парамагнитный резонанс в биологии
Исследование гемоглобина и его производных
|
|
|
А |
В предыдущей главе был приведен ряд примеров, показывающих, что в состав многих биологических молекул (например, перокеидазы, каталазы и цитохромов) входит гем, иными словами порфирин. Эта плоская структура (фиг. 85) характерна также-
|
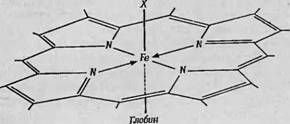
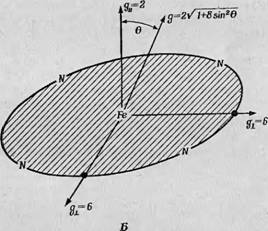
Фиг. 96. Структура гема. А — гем, т. е. порфириновое кольцо с атомом железа в центре; через пятую координационную связь к гему присоединяется глобин, через шестую — группа X (кислород, двуокись углерода и т. д.). Б — зависимость значения g-фактора у высокоспинового производного гемоглобина от направления (в плоскости гема G = 6,0 во всех направлениях). |
И для молекулы гемоглобина. В геме центральный атом железа окружен четырьмя атомами азота, а связь всей группы с белковой частью молекулы осуществляется через пятую координационную связь атома железа.
В гемоглобине — кислородпереносящем пигменте крови — имеются четыре гема и соответственно четыре атома железа на молекулу, тогда как в миоглобине — родственной гемоглобину молекуле, связывающей и переносящей кислород в мышцах,— имеется только один гем и соответственно один атом железа на молекулу. Таким образом, в первом приближении можно считать, что гемоглобин состоит из четырех молекул миоглобина. В обеих молекулах шестая координационная связь атома железа занята кислородом или двуокисью углерода и именно эта связь важна для процесса дыхания. В некоторых случаях шестая координационная связь бывает занята другими химическими группами; например, в условиях обычного хранения в буферных растворах в этом положении вместо кислорода или двуокиси углерода находится гидроксил (окисленный гемоглобин, или метгемоглобин, и окисленный миоглобин). Активность молекулы гемоглобина зависит от химической группы, присоединенной по шестой координационной связи. Так, в этом положении может находиться ион фтора, который отщепляется очень легко. Здесь может находиться также группа с более сильной связью, например цианид, но эту группу отщепить невозможно, и в результате молекула полностью теряет свою биологическую активность. На фиг. 96 показаны структура гема с атомом железа в центральном положении, пятая координационная связь, соединяющая железо с белком, и шестая координационная связь, занятая группой X. Вопрос о характере связи между атомом железа и группой X, естественно, имеет решающее значение. Дальнейшие исследования показали, что ЭПР-спектро - скопия не только дает более подробные сведения о природе этой связи, но и весьма полезна для установления структуры всей молекулы в целом.