ПИЩА И ПИТАНИЕ
|
V? у |
![]()
|
Уголь |
![]()
|
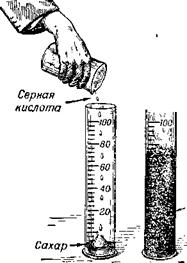
Рис. 14. Обугливание сахара кислотой» |
![]()
 Ото такое голод. Пища для живого организма служит
Ото такое голод. Пища для живого организма служит
* одновременно и топливом, и «строительным материалом», используемым на построение различных тканей. Если организм получает все необходимые для его роста и жизнедеятельности материалы—он сыт.
Если же пища длительное время содержит не все необходимые для организма вещества или содержит их в недостаточном количестве, жизнедеятельность организма становится всё более и более вялой — организм испытывает голод. Это относится к животным и растениям.
|
Серной |
![]() Для нормальной деятельности организма человека необходимо, чтобы пища содержала белки, жиры и углеводы (а кроме того некоторые соли и витамины). Познакомимся с ними подробнее.
Для нормальной деятельности организма человека необходимо, чтобы пища содержала белки, жиры и углеводы (а кроме того некоторые соли и витамины). Познакомимся с ними подробнее.
Углеводы. Истолчём в пудру обыкновенный сахар (свекловичный ИЛИ тростниковый С12Н22О11). Насыплем её в узкий стаканчик (рис. 14) и обольём небольшим количеством крепкой серной кислоты. Кислота очень быстро отнимет от сахара воду — он обуглится, вспухнет и превратится в объёмистую ноздреватую массу. Эта реакция идёт с выделением большого количества тепла. Поэтому выделяющаяся из сахара вода испа
Ряется, и над горлышком стаканчика хорошо видно образование мелких капелек воды. Точно так же ведут себя глюкоза или виноградный сахар СбН12Об, крахмал, а также вещество, из которого построены стенки клеток растений, — целлюлоза (клетчатка).
 Из-за лёгкости атом разложения на угле -
Из-за лёгкости атом разложения на угле -
Углерода род и воду и из-за
Того, что формулы атом этих веществ вы -
°~ водорода глядят так, как буд
То несколько атомов атом углерода соединены
Кислорода с несколькими моле
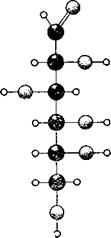
Кулами воды (ведь СбН^Об можно представить, как 6С +• +6Н20!), этот класс соединений получил название «углеводы». Строение простейшего углевода — глюкозы — изображено на рисунке 15.
Рис. 15. Строение молекулы глюкозы. Углеводы могут
Превращаться друг в друга, присоединяя или отщепляя при этом воду. Крахмал, например, можно превратить в простейший углевод — глюкозу. Тростниковый сахар С12Н22О11 также превращается в простейшие углеводы:
С12Н22О11+ Н20 >2С6Н1206.
Это превращение вызывают разбавленные кислоты и некоторые вещества, находящиеся в живых организмах. Замечательно, что такая реакция осахаривания идёт при
невысоких температурах — это имеет первостепенное значение для усвоения углеводов растениями и животными. Возможна и обратная реакция — превращение простых углеводов в сложные: 2СбН1206 —* С12Н220ц + Н20. Такие реакции идут при фотосинтезе в растениях и приводят к образованию крахмала и целлюлозы.
Окисляясь в живых организмах при дыхании, углеводы выделяют большое количество тепла.
Углеводы — не только пищевой материал, но и важное промышленное сырьё. Они используются для производства винного спирта, хлопчатобумажных тканей, искусственного шёлка, бумаги, бездымного пороха, пластмасс и т. п.
Жиры. Жиры — вторая необходимая часть нашей пищи. Это — сложные вещества, особенности которых удобнее всего пояснить на более простых примерах.
Если нагреть винный спирт с каким-либо водоотнимающим веществом, например с серной кислотой, то две его молекулы отщепляют воду и образуют простой
Э ф и р, в котором атом кислорода связывает остатки двух молекул спирта:
С2НзШ±1) ОС2Н5 С2Н6-0 —С2Н5+Н20.
Спирт спирт этиловый эфир
Ещё легче происходит отщепление ВОДЫ ОТ одной молекулы спирта и одной молекулы уксусной кислоты:
С2Н5ОН + НООССН3 ^ С2Н5ООССН3 + Н20.
Спирт уксусная кислота уксусноэтиловый
Эфир
При этой обратимой самопроизвольно идущей реакции получается сложный эфир, в котором атом кислорода связывает остаток молекулы спирта с остатком кислоты. Сложные эфиры дают любые кислоты и любые спирты, в том числе и трёхатомный спирт — глицерин. Трёхатомным он называется потому, что в его молекуле есть 3 спиртовые группы ОН; формула глицерина СН2ОН—СНОН—СН2ОН. Жиры и являются сложными эфирами, образованными глицерином и жирными кислотами, т. е. глицеридами жирных кислот. В состав жиров входят стеариновая кислота С17Н35СООН, пальмитиновая С15Н31СООН и менее богатые водородом (ненасыщенные) кислоты, например олеиновая кислота С17Н33СООН.
В образовании жиров участвуют все три спиртовые группы глицерина. Значит, одна молекула жира образуется из одной молекулы глицерина и трёх молекул жирной кислоты. Это и указывается в названиях жиров: три - стеарин — жир, образованный глицерином и стеариновой кислотой; триолеин — жир, получающийся из олеиновой кислоты и глицерина, и т. д.
О приблизительном составе некоторых натуральных жиров даёт представление следующая табличка:
|
Жир |
Процент тристеа - рина и трипаль - митина |
Процент три - олеина идругих ненасыщенных глицеридов |
Процент Прочих Глицери Дов |
|
Говяжье сало. * . |
75 |
25 |
0 |
|
Коровье масло. . |
53 |
39 |
8 |
|
Хлопковое масло. |
25 |
72 |
3 |
|
Льняное масло. . |
8 |
78 |
14 |
Мы видим, что в жирах животного происхождения преобладают насыщенные глицериды, а в растительных маслах — ненасыщенные.
Триолеин, как и другие ненасыщенные глицериды и соединения, можно перевести в насыщенные (тристеарии), действуя водородом в присутствии катализаторов — веществ-посредников, облегчающих и направляющих реакцию. В промышленности такой процесс проводится с растительными маслами и носит название «гидрогенизация жиров». Получаемые при этом насыщенные продукты используются для мыловарения, изготовления маргарина и т. п.
Как и все сложные эфиры, жиры гидролизуются, омыляются водой, ещё лучше — кислотами и особенно хорошо — щелочами. При действии щёлочи на жиры получаются мыла (отсюда и название реакции —> «омыление»):
Тристегрин + едкий натр глицерин + мыло.
Обыкновенное мыло и есть натриевая соль стеариновой кислоты.
Жиры в организмах составляют запас пищевых материалов. При сгорании они выделяют много тепла.
Белки. Белки — тот сложный материал, из которого состоит вещество живой клетки — протоплазма. Кроме углерода, водорода и кислорода, молекулы белков всегда содержат азот, а в ряде случаев — ещё серу, фосфор и некоторые другие элементы.
Состав и строение белков узнают с помощью гидро* лиза — расщепления белков водой под влиянием кислот. При продолжительном гидролизе белки дают соединения, называемые аминокислотами. Примером их может служить аминоуксусная кислота ЫН2—СН2—СООН, отличающаяся от уксусной тем, что вместо одного атома Н она содержит остаток аммиака — аминогруппу ЫНг. Аммиак — слабая щёлочь. Поэтому аминокислоты проявляют одновременно и свойства кислот, и свойства щелочей. Но ведь кислоты и щёлочи обязательно взаимодействуют друг с другом! Значит, одна молекула аминокислоты может сразу образовать соединение с двумя другими такими же молекулами, реагируя с одной из них как с кислотой, а со второй — как со щёлочью. При этом на одном конце новой, втрое большей молекулы опять окажется аминогруппа, а на другом — группа СООН. Эта молекула может образовать с двумя другими ещё большую молекулу. В действительности так и происходит: образующиеся в природе белки имеют очень большие молекулы, в 2000—10 000 раз более тяжёлые, чем молекулы воды. Так, яичный белок имеет молекулярный вес 34 000, белок гемоглобина — около 66 000, а желатина — 150 000.
Белки делятся на растворимые (в воде, в слабых растворах солей, в водно-спиртовых смесях) и нерастворимые. Растворимые белки при нагревании свёртываются. Такой переход совершается, например, при варке яиц.
Кожа, волос и шерсть — тоже белки. Хотя они и не растворяются ни в каких растворителях, их можно гидролизовать кипячением с кислотами и таким образом узнать их состав. Молекулы нерастворимых белков ещё крупнее, чем молекулы растворимых белков. При гидролизе многих из них сначала образуется желатин, а затем клей, то-есть растворимые белки, а уже потом гидролиз идёт дальше, до образования аминокислот.
Организмы животных, особенно — высших, не обладают способностью «синтезировать», то-есть строить ами
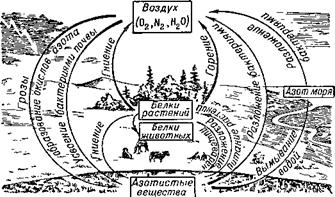
Нокислоты и белки из простейших веществ. Они получают белки в готовом виде из пищи и только перестраивают их. Растения же синтезируют аминокислоты и белки из углекислоты, воды и минеральных азотистых соединений— солей азотной кислоты, аммиака. В сельском хозяйстве азотистые удобрения применяют именно для усиления питания растений азотом, который идёт для синтеза белков. Таким образом, азот, подобно углероду и кислороду, тоже совершает в природе «круговорот», переходя от простых минеральных соединений к очень сложным органическим соединениям — белкам. При распаде,
|
Почвы Рис. 16. Круговорот азота в природе. |
Гниении белков азот опять выделяется в виде простых соединений — аммиака и его солей, а частью — в виде свободного азота. Этот круговорот азота в природе изображён на рисунке 16.
Катализаторы в живых организмах. Почему в винограде накапливается сахар состава СбН^Об, в свёкле — сахар С12Н22О11, а в картофеле — более сложный углевод— крахмал? Почему у коровы — травоядного животного — накапливается сало, а не растительное масло? Конечно, это отчасти объясняется различием условий, при которых протекают химические процессы в том или другом организме: различной температурой, разным освещением и т. п. Но главное здесь — присутствие в организмах тех или иных «ферментов» или, как их ещё называют, «энзимов». Это — биологические катализаторы, особые вещества, ускоряющие и направляющие биохимические процессы. Многие процессы в природе протекают избирательно, то-есть в определённом направлении, и это помогает организмам растений и животных перерабатывать пищу в вещества, свойственные именно данному виду организма. Поэтому нет ничего удивительного в том, что в картофеле накапливается именно крахмал, а в свёкле — сахар. Всё это — результаты реакций, направляемых ферментами.
В таблице на стр. 56 мы видели, что в растительных маслах содержится тристеарин, составляющий основу говяжьего сала. Мы отметили также, что триолеин при известных условиях может присоединять водород и превращаться в тристеарин. Установлено, что эта реакция происходит и в живых организмах под влиянием восстановительных ферментов. Жир триолеин перерабатывается в организмах травоядных животных в сало.
Наши примеры показывают, что белки, жиры и углеводы не просто включаются из пищи в состав тканей и клеток организма, а проходят соответствующую «кухню». Они гидролизуются, окисляются, восстанавливаются, расщепляются и снова образуют сложные вещества — белки, жиры и углеводы, но уже иного состава и строения, нужного для данного вида организма.
В качестве примеров ферментов, направляющих такие реакции в организмах, можно привести «диастаз», содержащийся в слюне, вызывающий осахаривание крахмала, «пепсин» желудка, «трипсин» поджелудочной железы и «эрепсин» кишечника — гидролизующие белки, «липазу» печени, омыляющую жиры.
Почему в тесто нужно добавлять дрожжи или питьевую соду? Не всегда белки, жиры и углеводы пищевых продуктов находятся в удобной для усвоения форме. Хлебные злаки богаты питательными веществами, но непосредственно в пищу они не идут, а подвергаются предварительной обработке — помолу, варке, выпечке. Для чего это нужно?
Размеры растительных клеток очень малы: отдельные клетки можно рассмотреть только в микроскоп. Даже самый тонкий помол не доводит измельчение зерна до отдельных клеток. А ведь белковые вещества и крахмал
Находятся внутри растительной клетки, стенки которой состоят из целлюлозы, стойкого вещества, почти не поддающегося перевариванию в желудке. Чтобы организм мог извлечь питательные вещества из такой растительной клетки, необходимо разрушить её стенки. Это разрушение и происходит под действием воды и высокой температуры при выпечке хлеба или при варке картофеля.
При варке злаков зёрна крахмала разбухают и образуют клейкую массу. Если к тесту не прибавлены дрожжи, то после выпечки получается твёрдая, непористая масса (галеты), тоже не легко перевариваемая. Под влиянием же дрожжей, содержащих фермент кислотного брожения, тесто «скисает» — из содержащихся в нём углеводов образуются в небольших количествах уксусная и молочная кислоты. Это брожение сопровождается выделением углекислоты. Углекислота придаёт тесту ноздреватость, разрыхляет его, особенно сильно — при нагревании во время выпечки. Это делает хлеб несравненно более удобоваримым.
Такого же результата можно добиться и без дрожжей, воспользовавшись веществами, которые разлагаются при температуре выпечки хлеба и выделяют углекислоту (например, углекислым аммонием (МН^СОз или питьевой содой КГаНСОз):
Нагревание
2НаНС03->Ка2С03 + С02 + Н20.
При замене дрожжей этими веществами тесто уже не нужно оставлять «подходить», так как в этом случае углекислота образуется не за счёт медленной реакции брожения углеводов, а за счёт быстрого разложения соли, идущего только при нагревании.
Что общего имеется в скисании теста, образовании уксуса из винограда, простокваши из молока, спирта из крахмала? Общим во всех этих случаях является то, чта все эти превращения — реакции с участием ферментов. Как и образование уксусной и молочной кислот в тесте, так и превращение виноградного вина в уксус при стоянии на воздухе происходит под влиянием бактерий. Они попадают в вино из воздуха, выделяют ферменты кислотного брожения и вызывают реакцию:
СН3СН2ОН + Оа5™?СН3СООН + н20.
Спирт уксусная кислота
Таким же образом из молока при стоянии на воздухе получается простокваша; она содержит молочную кислоту, образующуюся из молочного сахара.
Брожение под влиянием бактерий может происходить только у таких веществ, которые являются подходящей для бактерий питательной средой. В виноградном вине винного спирта немного и бактерии в нём хорошо развиваются. Но если эти же бактерии поместить в чистый спирт (96-процентный), то они погибнут. Поэтому спирт не превращается в уксусную кислоту, когда в него попадают бактерии, вызывающие кислотное брожение.
Однако для многих бактерий сам уксус — плохая среда. Поэтому его применяют для консервирования (маринования) пищевых продуктов.
Производство винного спирта — пример искусственно осуществляемого ферментативного процесса. Исходные материалы для него (картофель, зерно) богаты углеводами, в частности — крахмалом. Однако не все углеводы способны бродить. Бродят только простейшие углеводы; более сложные углеводы, например крахмал, должны быть предварительно «осахарены» — превращены в простейшие углеводы. Образование винного спирта из крахмала — сложный процесс, Каждая его стадия идёт под влиянием специального фермента, как это показывает следующая схема:
Фермент диастаз Крахмал + вода („ал£Тоза)
Фермент мальтаза
Мальтоза + вода —----------------------- > глюкоза
(дрожжи)
Фермент зимаза
Глюкоза---------------------- > спирт + углекислота;
(дрожжи)
Необходимый для осахариваыия крахмала фермент диастаз содержится в солоде — проросших зёрнах ячменя. Образование же и брожение глюкозы происходит под влиянием ферментов, вырабатываемых дрожжевыми грибками, — мальтазы и зимазы.
Протекающие в живых организмах процессы ещё более сложны. Но и здесь наблюдается такое же строгое «разделение труда» — каждый из ферментов «заведует» каким-либо одним направлением превращения веществ.
|
В |
нашем кратком очерке мы осветили лишь некоторые интересные явления, происходящие в природе и в технике. Но нельзя забывать, что современная химия проникла во все области народного хозяйства. На предприятиях и заводах создаются в настоящее время материалы, не встречающиеся в природе в готовом виде. Наряду с природным сырьём они стали основой современной техники. Это нетрудно показать на нескольких примерах.
Авиация требует топлива высокого качества. Химия открыла пути улучшения качества и увеличения количества бензинов, выделяемых из нефти. Химия дала также способы искусственного получения углеводородов и важных добавок для составления наиболее высококачественных авиабензинов; эти углеводороды и добавки получаются теперь сотнями тысяч тонн. Новый этап в развитии авиации — применение реактивных двигателей — также оказался возможным потому, что химия нашла для этой цели ряд новых материалов, в том числе и новые виды топлива.
Шины, камеры и множество других частей самолётов и автомашин изготовляются из каучука и резины. Однако природа не слишком щедро наделила земной шар каучуконосными растениями, да и произрастают они далеко не везде. Химии пришлось разрешить вопрос о синтезе каучука из простых и доступных видов сырья. В настоящее время синтетический каучук получается в количествах, в несколько раз превышающих количества добываемого натурального каучука. Родина синтетического каучука — СССР. Первый промышленный способ синтеза каучука разработал академик С. В. Лебедев. По этому способу советская химическая промышленность выпустила первый в мире синтетический каучук. Организация этого важнейшего производства проходила при личном содействии товарищей И. В. Сталина и С. М. Кирова. В настоящее время вырабатывается уже много сортов синтетического каучука, не только не уступающих натуральным каучу - кам, но и превосходящих их. Сырьём для этих производств служат спирт, ацетилен, а также некоторые газы, получаемые при переработке нефти.
Химия дала текстильной промышленности ряд новых синтетических материалов, из которых вырабатываются прочные красивые шёлковые ткани и другие изделия.
Новые созданные химией материалы — пластмассы — заменили для многих технических целей металлы я стекло. Различные детали автомобилей, самолётов и других машин, а также множество предметов домашнего обихода изготовляется теперь из пластмасс.
Не так уж давно красители для тканей добывались только из растений и животных. Число этих красителей было невелико, а способы их выделения из сырья очень сложны и трудоёмки. Химия создала тысячи сортов красителей самых разнообразных цветов и оттенков, совершенно вытеснивших из употребления красители естественного происхождения.
Взрывчатые вещества — соединения с громадным запасом внутренней, химической энергии. Они неустойчивы и в природе не существуют. Все они являются исключительно продуктами производства химической промышленности и находят применение в оборонном деле, при горных, земляных и т. п. работах.
Немало жизней спасли синтетические лекарственные препараты — стрептоцид, сульфидин, сульфазол и множество других. Некоторые синтетические препараты действуют не только на человека и животных. Разработаны способы получения ряда соединений, получивших название «ростовых веществ». Они приобрели большое значение в садоводстве и других отраслях сельского хозяйства, влияя на рост и созревание растений. Напомним, кстати, что сельское хозяйство требует огромных количеств удобрений, вырабатываемых химической промышленностью.
Ни производство красителей, взрывчатых веществ, лекарственных препаратов и пр., ни производство искусственного волокна, пластмасс или каучука невозможны без кислот, щелочей и солей. Поэтому-то производство кислот, щелочей и солей составляет «основную» химическую промышленность.
Добавим к сказанному, что и металлургия многое черпает из химии: способы переработки руд, составление новых сплавов, защита металлов от коррозии — всё это тесно связано с химией.
Значение химии в народном хозяйстве было особенно подчёркнуто при рассмотрении 3-го пятилетнего плана развития народного хозяйства СССР на XVIII съезде партии, происходившем в 1939 году. В этом плане
Особенное внимание уделялось развитию химической промышленности. Поэтому 3-я сталинская пятилетка вошла в историю под названием «пятилетка химии».
Химия как наука стояла на очень высоком уровне и в дореволюционной России. Работы М. В. Ломоносова, Д. И. Менделеева, А. М. Бутлерова, В. В. Марковникова,
А. Е. Фаворского, Н. Д. Зелинского и многих других русских учёных заложили основы современной химии и сделали русскую химию самой передовой. Достижения русской химии широко использовались за границей, но в России до Октябрьской революции химической промышленности почти не существовало; страна была в полной зависимости от английской, французской и особенно германской химической промышленности.
После Великой Октябрьской социалистической революции положение коренным образом изменилось. В СССР, создана мощная передовая химическая промышленность, освободившая страну от иностранной зависимости. Эта промышленность с честью выдержала такую строгую проверку, какой была Великая Отечественная война 1941— 1945 годов, потребовавшая невиданных в истории человечества количеств взрывчатых веществ, моторного топлива, каучука и всех других видов химической продукции.
В СССР созданы десятки крупных превосходно оснащённых научно-исследовательских институтов, в которых тысячи советских химиков разрабатывают научные и народнохозяйственные проблемы.
Наши химическая наука и химическая промышленность идут и развиваются своими, независимыми от капиталистических стран, путями и активно участвуют в решении общенародной задачи, поставленной перед трудящимися нашей Родины товарищем Сталиным — в построении экономического фундамента для перехода к коммунизму.