Флокуляция под действием катионных поверхностно-активных веществ
Взаимодействие гидрофобных групп, адсорбированных на поверхности кремнезема, влечет за собой образование «гидрофобной связи». Тэнфорд [291] подробно описал этот эффект. Для
8 Заказ № 250 коллоидного кремнезема сильнодействующими флокулирующими агентами являются амины с длинными цепями, в частности ал - килзамещенные четвертичные соли аммония с длинными цепями. Так, Смит и Турнбул [292] добавляли четвертичную соль аммония, чтобы вызвать частичную флокуляцию коллоидного кремнезема и придать ему тиксотропность для использования в качестве связующего вещества в тугоплавких порошковых шламах.
Авторы работы [293] при обсуждении вопроса о мицелляр - ной адсорбции описали ход адсорбционного процесса поверхностно-активного вещества на частицах коллоидного кремнезема. Полярная поверхность покрывается адсорбированным поверхностно-активным веществом, ориентированным по отношению к ней таким образом, что частицы кремнезема становятся гидрофобными. При немного более высокой концентрации ПАВ на первичном адсорбированном слое происходит дополнительная адсорбция, и на поверхности формируется конденсированный сдвоенный слой ПАВ. При этом оказывается, что полярные группы ПАВ во втором слое ориентируются уже наружу, сообщая поверхности гидрофильные свойства. Авторы представили экспериментальное доказательство того, что по мере добавления к системе дополнительного количества ПАВ его концентрация в растворе начинает понижаться после некоторой концентрационной точки, в которой стремительно развивается агрегация адсорбированного вещества вплоть до формирования двойного слоя на поверхности мицелл.
Хорошо известно, что гидрофобные частицы в воде прилипают друг к другу, как только приходят в соприкосновение. Поэтому не удивительно, что частицы кремнезема становятся гидрофобными, едва только на некоторых ограниченных участках на частицах кремнезема начинается флокуляция. Следовательно, при низких концентрациях такие ионы, как додециламмоний, влияют на электрокинетический потенциал частиц кварца точно так же, как и ионы натрия. При более высоких концентрациях наблюдается критическая точка, в которой электрокинетический потенциал резко изменяется, и ионы аммония с длинной цепью, несомненно, собираются в отдельные ассоциаты на поверхности раздела во многом подобно тому, как это происходит при формировании мицелл в объеме раствора [294].
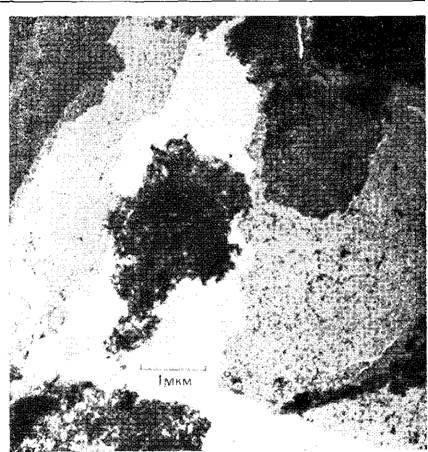
Мощное флокулирующее действие небольших добавок хлорида цетилтриметиламмония на золи кремнезема было использовано Александером и Айлером [295], чтобы сгруппировать частицы кремнезема при таких условиях, когда они способны формироваться в агрегаты, подобные листочкам или пленкам. Электронно-микроскопический снимок плоских агрегатов представлен на рис. 4.21. Механизм формирования таких агрегатов
|
Рис. 4.21. Электронно-микроскопический снимок листоподобных агрегатов, сформировавшихся из коллоидного кремнезема в присутствии катионных поверхностно-активных веществ. |
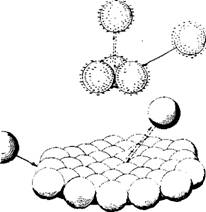
Схематически показан на рис. 4.22. Частицы кремнезема удерживаются вместе благодаря действию мицелл катионного ПАВ. Требуемое количество ПАВ составило только ~5 % от оцененного теоретически количества, необходимого для образования одного монослоя ПАВ на всей суммарной поверхности кремнезема. Мицеллы, вероятно, размещаются на кремнеземной поверхности только в точках контакта между частицами. Такой особый тип плоскостной флокуляции протекает в щелочном растворе, когда частицы кремнезема заряжены отрицательно и, следовательно, взаимно отталкиваются, но тем не менее при наличии достаточной силы, способной преодолевать мицеллярные связи.
8*
При этих условиях агрегаты будут расти в тонком слое, подобно листочку толщиной всего лишь в одну кремнеземную частицу. Так происходит потому, что частицы кремнезема способны сближаться и присоединяться друг к другу только по краям растущего листочка, поскольку' в этой области оказывается наименьшим ионное отталкивание. Как только формирование подобных листочков или «плоскостных агрегатов» заканчивается,, на них начинает осаждаться избыточный кремнезем. Это приводит к прочному связыванию Частиц вместе и заполнению пустот между ними, так что в результате получается непроницаемая слоистая частица кремнезема, имеющая толщину частицы коллоидного размера.
|
|
|
Рис. 4.22. Схема формирования агрегатов в виде листочков из частиц кремнезема. Частицы имеют возможность приближаться к краям листочка, где энергетический барьер за счет сил отталкивания оказывается меньшим, чем на поверхности. Внизу показано поперечное сечеиие листочка из слипшихся между собой частиц кремнезема. |
О'Коннор и Сандерс [296] исследовали гидрофобный н гидрофильный характер поверхности кремнезема при адсорбции на ней ионов цетилтриметил аммония. Когда кремнезем или очищенная стеклянная поверхность вступают в контакт с 10_7М водным раствором бромида цетилтри - метиламмония, то поверхность кремнезема начинает адсорбировать органический агент и адсорбция идет до тех пор, пока не образуется монослой этого вещества. При этом поверхность оказывается гидрофобной. Однако, если в растворе присутствует дополнительное количество этого агента, поверхность полностью не высыхает, когда ее извлекают из раствора, и в действительности остается влажной при условии, что концентрация агента составляет более чем 10"4 моль/л. Критическая концентрация мицелл в системе равна ~ 10~3 моль/л, поэтому очевидно, что при очень низких концентрациях на кремнеземе будет адсорбироваться■ один монослой этого агента с гидрофобными группами, направленными наружу. Это придает поверхности гидрофобные свойства, если
В растворе отсутствует избыток агента. Но если при концентрации мицелл 10_3 моль/л агента содержится больше, то тогда формируется двойной адсорбированный слой и катионы располагаются снаружи, снова превращая поверхность кремнезема в гидрофильную, которая при этом оказывается способной к смачиванию.
Коллоидный кремнезем, подвергшийся флокуляции благодаря образованию «гидрофобных связей» между гидрофобными участками на поверхности кремнеземных частиц, имеет следующую характерную особенность: при добавлении смешиваемого с водой спирта, например пропилового, наблюдается повторное диспергирование флокулята за счет «смачивания» поверхности. Гидрофобные группы пропилового спирта ориентируются по направлению к гидрофобной поверхности частиц кремнезема так, что спиртовые гидроксильные группы, направленные наружу, превращают поверхность в гидрофильную. При повторной регенерации и высушивании кремнезема спирт испаряется, и поверхность снова становится полностью гидрофобной.
Как отмечали Матиевич и Оттевилл [297], для адсорбции катионного ПАВ на поверхности коллоидных частиц необходимо, чтобы частицы по крайней мере имели определенный наименьший размер. Когда ПАВ в системе присутствует только в необходимом для флокуляции количестве, поверхность коллоидных частиц становится гидрофобной и происходит коагуляция. Но когда вводится избыточное количество ПАВ, происходит формирование второго слоя вследствие вандерваальсо - вого притяжения между углеводородными цепочками. Тогда ионизированные группы второго наружного слоя ориентируются по направлению к раствору, и частицы начинают разделяться и пептизировать с переменой знака заряда на поверхности.
Природа «гидрофобной связи» в водных растворах между гидрофобными участками молекулярных размеров была выявлена Клоцем [298]; затем этот вопрос обсудил Шерага [299] в связи с исследованиями белков; дальнейшее тщательное изучение было выполнено Немети и Шерага [300]. Козман [301] определил «гидрофобную связь» как стремление неполярных групп сцепляться друг с другом в водных средах. Это похоже на образование мицелл с внутримолекулярной связью, подобно тем, что существуют в водных растворах моющих веществ. Козман [302] представил общее обсуждение вопроса о «гидрофобных связях».
Исследования показывают, что ионы четвертичных аммоние-' вых оснований с длинными цепями, таких, как цетилпиридин, адсорбируются на поверхности кремнезема примерно при критической концентрации мицелл [303]. Ион алкиламмония занимает на поверхности кремнезема площадь, пршмерно равную 33—
45 А2 [304]. Фактически эти ионы адсорбируются на кремнеземной поверхности в виде димеров [305].
В результате флокуляции под воздействием катионного ПАВ, такого, как бромид цетилтриметиламмония, золь кремнезема может стать высоко тиксотропным, что полезно при его применении в качестве связующего вещества [306].
Для изучения флокуляции кремнезема, вызванной действием поверхностно-активных веществ, оказывается интересным то, что избыточное количество катионного ПАВ может быть оттитровано анионным ПАВ с применением в качестве индикатора бромфенолового синего [307].