Катализаторы синтеза метанола
Синтез метанола из СО и Н2 в промышленных условиях проводят на оксидных цинк-хромовых, цинк-хром-медных и цинк - алюмомедных катализаторах [51].
К исходному сырью предъявляют жесткие требования, так как примеси щелочных металлов вызывают образование высших спиртов, а в присутствии примесей никеля и железа ускоряются реакции, идущие с образованием метана. В синтез-газе не допускается содержание карбонила железа и соединений серы.
Высокоактивные и селективные катализаторы синтеза метанола» позволяющие осуществлять процесс при 200—300 °С, содержат медь.
Низкотемпературные катализаторы синтеза метанола представляют собой тройные и более сложные оксидные системы, в состав которых помимо оксида меди входят в различных сочетаниях трудновосстанавливаемые, более тугоплавкие по сравнению с СиО оксиды таких металлов, как Cr, Al, Zn, Mg, Мп. Высокую активность Gu—Zn—Cr-катализаторов объясняют способностью СиО образовывать с ZnO и Сг203 тонкодисперсную систему. Образованию и сохранению дисперсной формы Си способствует, по мнению авторов [145], образующаяся цинкхромовая шпинель с дефектной структурой. Дефекты вызваны внедрением меди в между - узлия решетки. Введение в состав катализатора хрома повышает его термоустойчивость.
Алюминий необходим для стабилизации каталитической активности. Известно [145], что металлическая медь и оксид цинка растворяются в аммиачно-карбонатном растворе с образованием аммиакатов по реакциям:
2Cu + С02 + 8NH3 + Н20 + 02 = [Си (NH3)4 С03] [Си (NH3)4 (ОН),], (1)' ZnO + (NH4)2 С03 + 2NH4OH = [Zn (NHS)«] C03 + 3H20. (2>
При 65—85 °С происходит разложение аммиачно-карбонатных комплексов Си и Zn по единому механизму, связанному с образованием осадка солей основных карбонатов меди и цинка по реакциям:
[Си (NH3)4 С03] [Си (NH3)4 (ОН)2] -U СиС03-Си (ОН)2 + 8NH3) 5 [Zn (NH3)4] С03 + 3H20 - U 2ZnC03.3Zn (ОН)2 + 20NH3 + 3C02.
Осадок основных карбонатов меди и цинка не нуждается в промывке. Заданное соотношение Си и Zn легко обеспечивается на. стадии приготовления исходных растворов.
Состав катализатора, % (масс.):
СиО 52 Cr2Os 17
ZnO 26 А1203 5
Основные характеристики:
Насыпная плотность, г/см3............................ 1,5
Пористость, %............................................... 18
Удельная площадь поверхности, м2/г . . Примерно 10
Аммиачно-карбонатные растворы (АКР) меди и цинка готовят в реакторах 2, 3 (рис. 3.23) растворением металлической меди и оксида цинка в аммиачно-карбонатном растворе при 25—40 °С
|
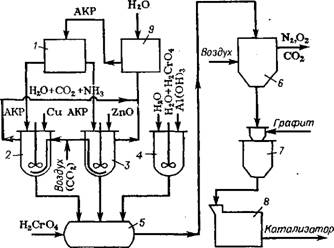
Рис. 3.23. Схема производства медьсодержащего катализатора синтеза метанола: 3 — мерник; 2—4 — реакторы; 5 — сушилка; 6 — электропечь; 7 — протирочное устройство; 8 — таблеточная машина; 9 — система улавливания |
По реакциям (1), (2). Там же происходит разложение аммиачно - карбонатных комплексов при 80—90 °С. Завышение температуры раствора свыше 90 °С приводит к разложению образовавшихся основных карбонатов меди и цинка до их оксидов.
В реакторе 4 получают суспензию гидроксида алюминия в растворе хромовой кислоты при 70—80 °С. Хромовая кислота частично растворяет гидроксид алюминия, а оставшуюся часть разрушает и диспергирует. Суспензию соосажденных основных солей меди и цинка и суспензию гидроксида алюминия в растворе хромовой кислоты из реакторов 2—4 с помощью воздуха продавливают в вакуумную сушилку 5, где ее перемешивают при 80 °С. Туда же порциями поступает порошок щавелевой кислоты. При этом имеют место реакции:
СиСОз-Си (ОН)2 + 2Н2Сг04 —> 2СиСг04 + ЗН20 + С02 2ZnC03.3Zn (ОН)2 + 5Н2Сг04 —> 5ZnCr04 + 8Н20 + 2С02 СиСОз-Си (ОН)2 + 2Н2Сг04-2Н20—> 2СиСг04-Н20 + 4Н20 + С02
2ZnCOs-3Zn (ОН)2 + 5H2Cr04-2H20 5ZnCr04-2H20 + 8Н20 + 2СОа
Получающийся продукт представляет смесь карбонатов основных солей, оксалатов и хроматов меди и цинка, гидроксида алюминия и воды.
Массу сушат при перемешивании под вакуумом до остаточной влажности 8—10 % и прокаливают в электропечи 6 на воздухе при температуре примерно 300 °С. Прокаленную массу перемешивают с графитом [2 % (масс.) ] и формуют в таблетки размером 4X6 мм. Выделяющиеся в процессе приготовления катализаторов NH3, С02 и пар с помощью системы улавливания 9 возвращают в технологический процесс, обеспечивая безотходность производства, близкую к полной.