Цеолитные катализаторы
Цеолитные катализаторы в различных поливалентных ка - тионных (или декатонированных) формах используют для проведения реакций органического и неорганического цикла: крекинг, гидрокрекинг, изомеризация, алкилирование, гидрирование, дегидрирование, окисление и т. д. В некоторых случаях они проявляют высокую активность без добавок промоторов, а в других — при нанесении на них активных компонентов. Цеолитные катализаторы термически стабильны, устойчивы по отношению к таким контактным ядам, как сернистые и азотсодержащие соединения, металлы, не вызывают коррозии аппаратуры. Развитая поверхность (до 800 м2/г), способность к катионообмену и высокая механическая прочность цеолитов позволяют использовать их в качестве носителей каталитически активной массы.
Все природные и большинство синтетических цеолитов представляют собой кристаллические алюмосиликаты, содержащие оксиды щелочных и щелочноземельных металлов, отличающиеся строго регулярной структурой пор, заполненных в обычных температурных условиях молекулами воды. При осторожном нагревании цеолиты выделяют водяной пар, при этом сами не разрушаются. Отсюда их название, состоящее из греческих слов «цео» и «лит» — «кипящие камни».
Скелет цеолитов имеет каркасную структуру с относительно большими сотообразными полостями, которые сообщаются окнами малых размеров, так что все полости связаны между собой. В 1 г цеолита имеется около 3-Ю20 полостей.
Наибольшее значение в катализе имеют кристаллические алю - мосиликатные цеолиты типа А, X, Y с прочным трехмерным скелетом. Общую формулу цеолитов можно представить в виде Мег in О. Al203-xSi02-г/Н20, где п — валентность катиона металла Me; х — число молей Si02; у — число молей воды. Величина х в значительной степени определяет структуру и свойства цеолитов. В цеолите типа А значение х близко к 2; в цеолитах типа X — изменяется от 2,2 до 3; в цеолитах типа Y — от 3,1 до 5,0; в синтетическом мордените достигает 10. Для каталитических процессов используют цеолиты с х = 2,8- -г6,0[156]. При различных условиях синтеза цеолитных катализаторов (химический состав кристаллизуемой массы, параметры кристаллизации, природа катиона) можно в широких пределах изменять значение х [157]. Так, низкокремнистые катализаторы (х = l,9-f-2,8) синтезируют в сильнощелочной среде, а в качестве источника кремнезема используют силикат натрия. Для получения высококремнистых цеолитов применяют более реакционноспособные золи или гели кремниевой кислоты, а синтез проводят в менее щелочной среде.
При синтезе цеолиты получают обычно в №+-форме. Эти катионы могут быть обменены на эквивалентные количества других с образованием различных ионообменных модификаций, имеющих разнообразные каталитические свойства. Для каждого типа цеолита сечения пор и их входные отверстия (окна) имеют молекулярные размеры и являются строго постоянными [158]. Это позволяет достичь высокой селективности катализатора. Так, с помощью цеолитов удается дегидрировать бутиловый спирт из его смеси с изобутиловым или гидрировать олефины из их смеси с изоолефинами. Ниже приведена характеристика пористой структуры некоторых цеолитов:
Цеолит.................... LiA NaA КА СаА NaX (NaY) СаХ (CaY)
Диаметр полости,
Им. ........................ 1,2 1,1-1,2 1,1 1,1 1,1-1,3 1,1-1,3
Размер окон, нм 0,4 0,4 0,3 0,5 Примерно 0,9 Примерно 0,8
Синтетические цеолиты можно получить гидротермальным синтезом в виде кристаллов с размерами порядка микрона. Синтез цеолитов в №+-форме сводится к осаждению щелочного алю - мокремнегеля с последующей его кристаллизацией [112].
Принципиальная схема приготовления гранулированных цеолитов сводится к следующим операциям: приготовление рабочих растворов (кремнезема, алюмината натрия, NaOH, КОН и др.), осаждение алюмосиликагидрогеля, кристаллизация гидрогелей в щелочной среде, промывка, формовка, термообработка.
В качестве сырья используют силикат-глыбу, А1(ОН)3 и NaOH. Гидроксид алюминия растворяют в кипящем растворе NaOH. Полученный алюминат натрия доводят до рабочей концентрации водой. Силикат-глыбу разваривают в автоклаве острым паром (см. стр. 106), раствор жидкого стекла разбавляют водой для получения требуемой концентрации.
Смесь растворов силиката и алюмината натрия поступает в смеситель 1 (рис. 3.27), где при интенсивном перемешивании коагулирует с образованием рыхлого гелеобразного осадка алюмосиликагидрогеля. Гидрогель кристаллизуют в кристаллизаторе 2.
|
|
|
NaAlC |
|
Na,0-nSi0j |
|
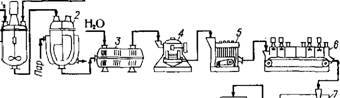
Рис. 3.27. Схема производства гранулированных цеолитов: • |
|
С □ 1 |
|
□ |
|
І — смеситель жидких фаз; 2 — кристаллизатор; 3 — фильтр-пресс; 4 — бегуны; 5 — таблеточная машина; б — ленточная сушилка; 7 — барабанное сито; 8 — шахтная печь |
|
|
|
С □ 3 С □ 1 |
Катализатор
При получении цеолита типа А температура в кристаллизаторе составляет 80—90 °С, а время — 6 ч; для цеолита типа X требуются температура порядка 95—100°С и время — 12 ч. Кристаллизатор обогревают глухим или острым паром. Важнейшими факторами в процессе кристаллизации при получении Na-цеолита являются следующие: концентрация щелочи (NaOH или КОН) в реакционной среде, молярные отношения реагирующих компонентов и формула состава алюмосиликагидрогеля, которую принято выражать оксидами: aNa20-А1203-nSi02-л:Н20. Осадок отделяют от маточного раствора в фильтр-прессе 3, отмывают от избытка щелочи водой. Частицы осадка имеют размер от 1 до 15 мкм.
В бегунах 4 цеолит замешивают с каолинитовой или бентонитовой глиной, взятой в количестве 15—20 % от массы осадка. Время замеса колеблется в пределах 30—40 мин. Требуемая для грануляции консистенция пасты, получающейся в бегунах, должна соответствовать примерно 35 %-й влажности.
В таблеточной машине 5 получают гранулы требуемых размеров, сушат в ленточной сушилке 6 при 120—150 °С. Мелочь и пыль, отсеянную от сухих гранул в барабанном вращающемся сите 7, направляют на повторный замес. Гранулы прокаливают во вращающейся или шахтной печи 8 при 575—650 °С в течение 6—24 ч. В процессе прокаливания цеолит приобретает требуемую механическую прочность и термическую устойчивость.
Введение связующего ухудшает кинетические характеристики цеолита, вследствие сокращения доли полезного объема пор. В связи с этим разработана технология цеолитов без связующего [112], по которой кристаллы сращивают в агломераты; промежутки между последними образуют вторичную пористую структуру. Порошкообразный каолин и гидрокарбонат натрия поступают через дозаторы в бегуны 1 (рис. 3.28), где смешиваются с одновременным увлажнением в течение 30—40 мин до получения однородной массы.
Смесь из бегунов направляют на вальцы 2 для окончательного перетирания и далее в формовочную машину 3. Наилучшее гранулирование достигается при влажности массы 33—34 %. Сырые гранулы высушивают на ленточной сушилке 4 до остаточной влажности 15—17%, прокаливают примерно при 600 °С в течение 12—24 ч в шахтной печи 5 и отсеивают от крошки и пыли на барабанном сите 6.
Содержащиеся в исходном каолине минералы в результате термической амортизации образуют алюмосиликат — метакаолин. Соотношение SiOa к А1203 в метакаолине соответствует соотношению этих компонентов в цеолитах типа А.
После смешения метакаолина с NaHC03 образуется алюмосиликат натрия, почти полностью переходящий при кристаллизации во вращающемся кристаллизаторе 7 в цеолит А. Вращение кристаллизатора улучшает обработку гранул и уменьшает опасность их слипания или старения. Через кристаллизатор циркулирует горячий щелочной раствор алюмината натрия. Температура процесса кристаллизации 95—100 °С. Далее гранулы промывают до значения рН отходящей воды около 11,5, выгружают в бункер - сушилку 8, где избыток воды стекает через сетчатое внутреннее днище, а цеолит высушивают, продувая горячий воздух или топочные газы.
Цеолит типа Y, используемый в качестве компонента катализатора крекинга, получают на основе концентрированного золя Si02, раствора силиката натрия или мелкодисперсного кремнезема [20]. Последний осаждают из раствора силиката натрия раствором аммонийных солей [NH4N03 или (NH4)2S04]. Полученную суспензию кремнезема промывают пятикратным (в рас
чете на SЮ2) количеством воды, отжимают на вакуум-фильтре до влажности 70+-75 % (масс.), смешивают со щелочным раствором алюмината натрия с целью получения реакционной массы с молярным отношением Si02 : А1203 == 6 — 8; NaaO : Si02 = = 0,28 — 0,4. Приготовленный щелочной алюмокремнегель гомогенизируют и подвергают низкотемпературной (95—100 °С) гидротермальной кристаллизации. Кристаллы цеолита отделяют от маточного раствора, промывают от избытка щелочи до рН промывных вод, равного 10,5 и высушивают.
Методы нанесения активных компонентов. Для введения в полости или нанесения на поверхность кристаллов цеолитов каталитически активных компонентов используют методы ионного обмена, пропитки, соосаждения, адсорбции из газовой фазы, внесения соединений в процессе синтеза (кристаллизации) цеолитов, адсорбцию паров металлов и др. [159].
Поскольку поры цеолитов имеют молекулярные размеры, они вмещают ограниченное число молекул, зависящее от природы соединения и условий его введения, поэтому можно получать более дисперсное распределение активных компонентов.
Ионный обмен (пат. США 3013982). Обменом катионов Na+ на ионы других элементов или Н+ можно ввести в цеолит - ную структуру металлы, например Ni и Pt. Никель-обменный цеолит (или цеолит, содержащий комплексные катионы) может быть восстановлен водородом примерно при 500 °С до металлического никеля. При этом наряду с атомами никеля образуются протоны, которые компенсируют вместо ионов Ni2+ отрицательные заряды алюмосиликатного скелета:
[ А104]|—Ni2+ + н2 = 2Ni° + 2 [А104р Н+.
Наилучшее распределение металла достигается в том случае, когда перед стадией восстановления из цеолита удаляется практически вся вода. При прочих равных условиях легкость восстановления катионов зависит от состава цеолита, степени его кислотности. Чем выше кислотность, тем меньше степень восстановления катионов.
Каталитическую систему Pt на цеолите используют в реакциях дегидрирования циклогексана и деметилирования толуола. Исходный цеолит типа Y имеет состав, % (масс.):
Si02 63,5 Na20 13,0
А120з 23,5 Fe 0,05
Цеолит промывают деионизированной водой, обрабатывают водным 0,0Ш раствором [Pt(NH3)4]Cla при 98—100 °С. После обмена цеолит отмывают до отсутствия ионов хлора в фильтрате, сушат при 110 °С, а перед использованием восстанавливают в токе водорода при 500 °С, получая при этом металлическую Pt на цеолитном носителе.
При восстановлении образцов наблюдается миграция металлов из объема кристаллов цеолитов на их внешнюю поверхность и образование фазы массивных металлов. Интенсивность ее образования зависит от структуры цеолита, его Состава и природы металла [159 ]. По легкости миграции в цеолитах металлы располагаются в ряд:
Ag>Pd>Cu>Ni>Pt.
На практике чаще всего необходимо получить катализаторы с небольшими количествами [0,1—1 % (масс.)] благородных металлов (Pt, Pd). Однако при ионном обмене распределение малого количества катионов во всей массе катализатора не всегда равномерно, особенно, если цеолиты гранулировайные. В этом случае лучше всего обмен на катион благородного металла вести в присутствии ионов, содержащихся в применяемой форме цеолита: Na+ для натриевой формы, Са2+ для кальциевой и т. д. Это позволяет получать катализаторы с равномерным распределением металлов во всем объеме отдельных гранул и всей массе цеолита.
Пропитка. Обезвоженный цеолит пропитывают некоторыми растворимыми органическими или неорганическими соединениями металлов с последующей термической обработкой. Соединения должны разлагаться с выделением металлов при температурах ниже порога стабильности кристаллической решетки цеолита. Для этой цели можно использовать карбонилы или гидрокарбо - нилы Fe, Со, Ni, Cr, Mo, W, Mn, Re, ацетилацетонаты Сг, Си, Ag, Аи, галогениды Ті, Hf, Zr и другие соединения [160].
Введение соединений в процессе синтеза (кристаллизации) цеолита [161]. Метод используют в тех случаях, когда введение каталитической добавки в готовые кристаллы цеолита невозможно. Так, ввести Pt методом ионного обмена в цеолит СаА с размером окон 0,5 нм практически невозможно, поскольку доступные соединения Pt имеют низкие значения рН и могут разрушить структуру цеолита, а катионы нейтральных аминокомплексов Pt имеют размеры больше 0,5 нм. В этом случае пригоден способ введения каталитически активного компонента на стадии синтеза (кристаллизации) цеолита. Например, на стадии кристаллизации цеолита NaA из раствора, содержащего комплексы Pt, идет захват последних в полости кристаллов. Захваченные катионы прочно удерживаются в порах цеолита и не извлекаются в процессе обмена Na+ на Са2+. Таким образом получают высокоселективный катализатор гидрирования олефинов.