Кооперирование производства карбамида с производством аммиака
Одно из перспективных направлений повышения эффективности современных химико-технологических систем заключается в создании объединенных схем различных, но взаимосвязанных производств. При этом упрощается технология, уменьшается общее число технологических операций и потребность в оборудовании, сокращается численность обслуживающего персонала, более рационально используются энергетические средства [1]. Кроме того считается [2], что объединение двух процессов представляет собой важное средство обеспечения для одного из них, в случае небольшой его мощности, технико-экономических характеристик, сопоставимых с аналогичными показателями многотоннажного производства.
Известно множество вариантов кооперирования производства карбамида с другими производствами. Отметим, в частности, предложение [3] о совмещении с синтезом алкандиолов и с получением многочисленных продуктов на основе парового крекирования углеводородов, а также объединенный процесс получения метанола— карбамида—аммиака—водорода [2]. Подавляющее же большинство технических решений относится к интегральному процессу синтеза карбамида и аммиака. Поскольку оба сырьевых потока для синтеза карбамида (NH3 и С02) поступают с установки синтеза аммиака, эти два производства неизбежно всегда взаимосвязаны; только обычно связь их весьма ограничена.
Из анализа схем раздельного производства NH3 и CO(NH3)2 следует, что существует немало объективных недостатков такой технологии, которые могут быть устранены только путем глубокого кооперирования. Например, на установку синтеза карбамида С02 поступает при давлении, близком к атмосферному, а жидкий NH3 10* 291
F
Под давлением примерно 1,5 МПа, тогда как в технологической линии синтеза аммиака С02 получают при Р» 3 МПа, a NH3 при Р ^ 20 МПа и выше. Далее отметим, что для очистки конвертированного газа от примеси С03 в аммиачном производстве применяют специальные абсорбенты, для регенерации которых требуются большие энергозатраты. В то же время в производстве карбамида рециркулируемые потоки являются эффективными поглотителями С02. В качестве одной из существенных предпосылок объединения схем укажем также на то, что производство карбамида отличается высокой энергоемкостью, а современные многотоннажные установки аммиака обладают сравнительно дешевыми энергетическими ресурсами. Наконец, различные газовые потоки из агрегата синтеза аммиака могли бы служить стриппинг-агентами в узле дистилляции плава синтеза карбамида.
Перейдем к рассмотрению конкретных предложений по комбинированию производств карбамида и аммиака.
Идея глубокого кооперирования была запатентована в Германии почти одновременно с пуском первой установки промышленного получения карбамида еще в двадцатых годах [4]. По этому способу в зону синтеза карбамида в качестве одного из исходных реагентов подают после предварительного охлаждения газовую смесь, выводимую из колонны синтеза аммиака, либо жидкий NH3 непосредственно после синтеза. Поскольку в этом случае NH3 содержит примеси Н2, N2, Аг и др., предусматривают [5] окисление Н2 кислородом, который вводят в реактор карбамида совместно с С02. Причем, после выделения из плава синтеза карбамида жидкий аммиак не рециркулируют, а отгружают в виде товарного продукта.
Диоксид углерода из синтез-газа для производства аммиака предлагают выделять конденсацией при глубоком охлаждении [6] либо абсорбцией в одну или несколько ступеней водой, аммиачной водой, водными растворами УАС и карбамида [6,7],насыщенными углеводородами, жидким аммиаком в сочетании с безводным плавом карбамида или с каким-либо растворителем карбамата аммония [8]. Процесс абсорбции проводится при низком или высоком (вплоть до давления синтеза карбамида) давлениях. После поглощения С02, согласно одному из вариантов [8], СО, содержащийся в синтез-газе, подвергают каталитическому окислению и вновь абсорбируют С02. Чтобы исключить загрязнение синтез - газа аммиаком, при поглощении С02 используют [9] раствор с минимальной концентрацией NH3.
Для разделения смеси N2, Н2 и NH3, выводимой из реактора синтеза аммиака, NH3 сорбируют водой, водным РУАС или раствором карбамида; абсорбат передают в зону синтеза карбамида либо используют его для поглощения С02 из синтез-газа. Существует вариант, по которому предусмотрена регенерация абсорбента путем отдувки NH3 из раствора инертным газом с последующим использованием газовой смеси в качестве стриппинг-агента в зоне дистилляции плава синтеза карбамида. В другом случае часть NH3 выделяют ректификацией аммиачной воды и ожижают [7, 10].
В некоторых патентах рекомендуется связывание С02 из синтез-газа осуществлять непосредственно в зоне синтеза карбамида, куда наряду с аммиаком вводят рециркулируемый РУАС. Если общее содержание С02 в синтез-газе превышает потребность в нем производства карбамида, излишек С02 предварительно абсорбируют раствором К2С03 (либо К2С03 с добавкой диэтаноламина) [7, 11,].
Безусловно, весьма притягательно выглядит замысел [12] получения карбамида взаимодействием С02 из синтез-газа и NH3 из смеси N2, Н2 и NH3, выводимой из реактора аммиака, при подаче обоих потоков непосредсгвенно в колонну синтеза карбамида. Но не исключено, что низкая степень превращения (вследствие присутствия в зоне синтеза большого количества инертных по отношению к про - цессу веществ) не позволит осуществить рассматриваемое предложение [12] на практике.
Энергию дросселирования продукционной смеси из реактора NH3 (с целью выделения непрореагировавших Na и Н2) используют [13] для сжатия жидкого NH3, направляемого в реактор карбамида.
В ряде патентов [7, 14] предусматривают утилизацию тепла синтез-газа, например, для нагревания плава синтеза карбамида в зоне дистилляции.
При совмещении производств МН3 и CO(NH2)2 появляются дополнительные возможности применения различных газовых потоков в качестве стриппинг - агентов на стадии дистилляции. Продувают плав очищенным от С02 синтез-газом при давлении синтеза карбамида или при пониженном давлении с последующей абсорбцией отогнанных NH3 и С02 из газовой смеси с образованием раствора карбамата аммония, рециркулируемого в зону синтеза карбамида. Синтез-газ предназначают для продувки плава и без очистки от С02. По схеме, созданной японскими специалистами, сырой синтез-газ подвергают контактированию с РУАС при Я > 12 МПа. При этом из газа частично абсорбируется С02. Оставшимся газовым потоком отдувают С02 и NH3 из плава синтеза карбамида, после чего смешанный газовый поток подают на вторичное контактирование с раствором из первой зоны абсорбции и образующийся абсорбат возвращают в колонну синтеза карбамида. Один из запатентованных способов предусматривает двухступенчатую продувку плава синтеза карбамида сначала синтез-газом, а затем газовым потоком с предыдущей ступени после абсорбции из него NH3 и С02 [7, 10, 14, 151.
До настоящего времени ни одна из интегральных схем производства CO(NH2)2 и NH3 не внедрена в промышленных условиях. Наиболее изучены в опытно-промышленном масштабе и практически подготовлены к промышленному использованию способы фирм «Мицуи Тоацу» и «Снам Проджетти». Схемы этих фирм и будут подробно рассмотрены ниже.
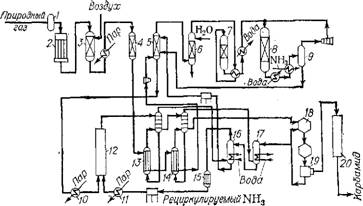
Объединенный процесс «Мицуи Тоацу». Способ совмещенного производства CO(NH2)2 и NH3 запатентован фирмой «Мицуи Тоацу» в нескольких вариантах, в основном отличающихся техникой абсорбции С02 из сырого синтез-газа и составом применяемого абсорбента. Принципиальная технологическая схема одного из вариантов [7] приведена на рис. Х.1.
Синтез-газ для производства NH3 получают известными методами, например, конверсией углеводородного сырья. Конвертированный газ сжимают компрессором 1 до давления синтеза карбамида. Это давление варьируется в зависимости от мольного соотношения NH3 : С02, но обычно оно выше 15 МПа (предпочтительно от 20 до 30 МПа). Сжатый газ вводят в аппарат, представляющий собой реактор синтеза карбамида, объединенный с абсорбером С02. Газ поступает в нижнюю часть абсорбера 2. В верхнюю часть абсорбера подают растворитель карбамата аммония — воду, водный раствор аммиака, водный раствор карбамида. В качестве абсорбента также может быть использован метиловый спирт. Абсорбенты могут содержать небольшие количества примесей других веществ.
Абсорбер оборудован насадкой в виде колец Рашига или кол - пачковыми тарелками. Высоту зоны абсорбции устанавливают из расчета предотвращения возможности проскока С02. В верхнюю часть абсорбционной зоны вводят жидкий NH3 и сжимаемый плун-
Nh3;n"2:h2;co co(nh2)2;nh3;h2o
Жерным насосом 11 раствор карбамида (например, маточный раствор из узла кристаллизации и центрифугирования). Выводимый из зоны абсорбции раствор направляют в зону синтеза карбамида 4. В случае необходимости этот поток можно подогреть в теплообменнике 3. В реакторе синтеза карбамида температуру поддерживают в интервале 160—200 °С.
Плав синтеза карбамида выводят из нижней части реактора через вентиль 13 и обрабатывают известными способами (например, дистилляцией) для выделения карбамида. Раствор неконвертированных NH3 и С02 с примесью карбамида рециркулируют насосом 12.
|
C0(NH2)2;C02;NH3;H20 h20;c02;nh3;c0(nh2)2 |
|
Рис. X. l. Схема объединенного производства CO(NH2)2 и NH3 фирмы «Мицуи Тоацу»: 1,8 — компрессоры; 2 — абсорбер С02; 3 — теплообменник; 4 — реактор синтеза карбамида; 5 — холодильник; 6 — сепаратор; 7 — узел очистки газа от СО; 9 — реактор синтеза NH3; 10 — сепаратор NH3; 11, 12 — насосы; 13 — вентиль. |
Выходящий из абсорбционной зоны газ полностью свободен от примеси С02. Этот газ подают через холодильник 5 в сепаратор 6, где отделяют NH3, возвращаемый в абсорбционную зону, а оставшийся газовый поток направляют на установку 7 очистки от СО. Если применяется медно-аммиачная очистка, то в газе допустимо небольшое содержание NH3. Но в случае, если с этой целью осуществляется отмывка жидким азотом или метанирование, необходимо предварительное полное удаление NH3. 294
|
|
Рис. Х.2. Схема пилотной установки объединенного производства NHa и CO(NH2)2:
1 — узел очистки от соединений серы; 2,3 — конверторы i и ii ступеней; 4 — конвертор СО; 5 — абсорбер С02; 6 — скруббер NH3; 7 — метанатор; 8 — реактор синтеза NH3; 9 — сепаратор NH3; 10, 11 — подогреватели; 12 — реактор синтеза карбамида; 13, 14 — аппараты i и ii ступеней дистилляции; 15 — конденсатор nh3; 16 — абсорбер высокого давления; 17 — абсорбер низкого давления; 18 — кристаллизатор; 19 — центрифуга; 20 — грануляционная башня.
В установке 7 устанавливают мольное соотношение Н2 : Na, требуемое для проведения реакции синтеза NH3. Очищенный газ компрессором 8 сжимают до 40—50 МПа и подают в реактор синтеза аммиака 9. Полученный NH3 выделяют из реакционной смеси известными способами и в жидком виде направляют в аппарат 2. Непрореагировавшие газы возвращают в реактор синтеза NH3.
В 1966 г. фирмой была пущена пилотная установка мощностью 5 т CO(NH2)2 в сутки [16—18]. Схема установки [18] (рис. Х.2) соответствует способу [7 ] и отличается от изложенного выше варианта тем, что абсорбцию С02 под высоким давлением из j
Синтез-газа (для производства NH3) осуществляют карбаматный ]
Раствором и жидким NH3, а теплоту потока синтез-газа исполь - j
Зуют для дистилляции плава синтеза карбамида.
В соответствии с приведенной на рис. Х.2 схемой газ, полученный конверсией углеводородов и последующей конверсией СО, пэд давлением около 3 МГІа и при температуре 200 °С подаюг через теплообменники-кипятильники I и II ступени дистилляции плава синтеза карбамида в компрессор, сжимающий газовый поток до 30 МПа. При таком давлении С02 из газа поглощают в абсорбере карбаматный раствором (полученным абсорбцией газов дистилляции из цикла синтеза карбамида) и свежим NH3 из цикла синтеза NH3. Выводимый из абсорбера раствор, содержащий NH3, карбамат аммония и некоторое количество обр» зовавшегося карбамида, направляют в реактор синтеза карбамида под давлением 25 МПа. С учетом частичного образования карбамида в абсорбере С02 объел реактора в этом случае меньше, чем в обычном процессе. Наряду с раствором из абсорбера С02, в реактор подают рециркулируемый жидкий NH3. Плав синтеза карбамида подвергают двухступенчатой дистилляции; полученный раствор карбамида Подают в кристаллизатор; кристаллы отделяют в центрифуге, расплавляют и гранулируют в башне. Синтез-газ, очищенный в абсорбере от С02,
F-
Промывают в скруббере водой для удаления NH3, затем освобождают от примесей СО и С02 метанированием и под давлением 27 МПа подают в реактор синтеза аммиака [16, 18]. Установка работала 400 суток, в том числе 30 суток непрерывно [18].
Объединенный процесс обладает целым рядом преимуществ [2, 16—19].
1. В контуре синтеза карбамида исключается компрессор С02 и соответственно сокращаются затраты электроэнергии. При этом, разумеется, нельзя не учитывать, что возрастает количество сжимаемого синтез-газа, содержащего 20% С02. Поскольку за счет примеси С02 плотность синтез-газа возрастает, для сжатия содержащего С02 газа можно применять наиболее экономичное устройство — турбокомпрессор при мощности установки для синтеза NH3 400 т/сутки, тогда как минимальная мощность установки при газе, не содержащем С02, 500 т/сутки NH3.
2. Исключаются аммиачные насосы и примерно на 56% снижаются затраты энергии на сжатие NH3, поскольку свежий жидкий NH3 из контура синтеза NH3 непосредственно передают в реактор синтеза карбамида. Сохраняется лишь насос для рециркулируемого возвратного NH3.
3. Упрощается стадия очистки синтез-газа от примеси С02: исключаются затраты энергии на регенерацию абсорбента, полностью ликвидируется регенерационная аппаратура (колонны и теплообменники). Абсорберы С02, работающие под высоким давлением, более компактны и эффективны.
4. Исключается установка для регенерации NH3 из аммиачной воды, полученной при улавливании NH3 из продувочных газов синтеза NH3, в связи с использованием ее в производстве карбамида.
5. Так как в абсорбере С02 частично протекает реакция образования карбамида, размеры колонны синтеза карбамида могут быть уменьшены.
6. В результате упрощения технологии и сокращения общего числа стадий снижается требуемая численность обслуживающего персонала.
7. Стоимость интегральной установки на 5—10% ниже капитальных затрат на автономные агрегаты синтеза NH3 и CO(NH2)3 117].
8. Снижаются энергетические затраты, что иллюстрируется табл. Х.1 и Х.2.
9. За счет экономии капиталовложений и снижения энергозатрат ожидаемое снижение себестоимости карбамида составит [17 ] 6—7%.
Объединенный процесс при всех перечисленных достоинствах не лишен и недостатков. Основным из них является снижение гибкости и невозможность (или сложность) обеспечения отдельной работы одной из частей комбинированного агрегата. В этой связи уместно напомнить, что в свое время полузамкнутые схемы полу - 296
|
Таблица Х.1. Снижение энергетических затрат (из расчета на 1 т Карбамида) при использовании объединенной схемы по сравнению с производством иа раздельных установках [17]
|
|
Примечание. Принято, что в производстве NH3 затраты остаются неизменными, и вся экономия имеет место в производстве карбамида. |
|
Таблица Х.2. Энергетические и сырьевые затраты в процессах производства карбамида и аммиака [18] [в расчете иа 1 т CO(NH2)2 и 0,580 т NH3]
|
Чения карбамида оказались неконкурентоспособными именно из-за жесткой связи производств карбамида и солей аммония и были вытеснены полностью замкнутыми схемами.
Некоторое усложнение объединенного метода может вызвать дебаланс сырья. Если сырьем служит нафта, то С02 избыточен по отношению к мощности производства CO(NH2)2, рассчитанного, исходя из ресурсов NH3. В этом случае необходимо устанавливать вспомогательную установку абсорбции С02. Если же С02 недостаточно, например, при конверсии метана, необходимо предусматривать [19] сбыт избыточного NH3.
Объединенный процесс «Снам Проджетти». В основу процесса положены следующие новейшие разработки специалистов фирмы [7, 20]: выделение NH3 из продукционной газовой смеси после реактора синтеза NH3 водной абсорбцией; обезвоживание влажного рециркулнруемого в контуре синтеза NH3 газа впрыском жидкого NH3; стриппинг-процесс производства карбамида.
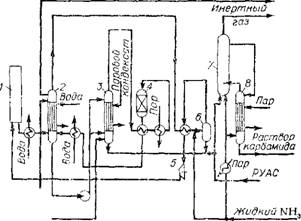
Принципиальная технологическая схема интегрального процесса приведена на рис. Х. З и Х.4. На этих рисунках не показаны ступени получения конвертированного газа, так как они ничем
Конвертированный газ
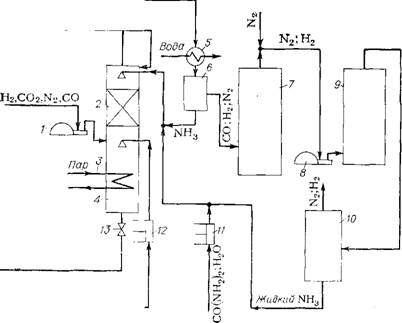
Рис. Х. З. Схема отделений синтеза СО(МН2)2 и NH3 в интегральном процессе их производства:
|
Продувочный газ |
|
Деминерализоу-, ванная воаа |
I — реактор синтеза NH3; 2 — пленочный абсорбер NH3; 3 — пленочный абсорбер С02; 4 — метанатор; 5 — компрессор; 6 — влагоотделитель; 7 — реактор синтеза карбамида; 8 — дистиллятор.
|
Жидкий NH. |
|
РУАС~<—^Ь -1 |
|
Плав синтеза карбамида^ |
|
Ко нвер тирован Иый газ |
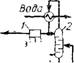
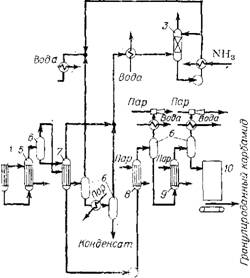
Рис. Х.4. Схема отделений дистилляции плава синтеза и выделения карбамида в твердом виде по интегральному процессу:
1 — иасос; 2 — промывная колонна; 3 — абсорбер-конденсатор; 4,5 — аппараты дистилляции i и ii ступеней; 6 — сепаратор; 7 — аппарат дистилляции III ступени; 8, 9 — выпарные аппараты i и ii ступеней; 10 — грануляционная башия.
Не отличаются от аналогичных ступеней при автономном производстве NH3. Однако следует отметить, что теплоту охлаждения конвертированного газа используют для дистилляции плава синтеза CO(NH2)2 и предварительного подогрева рециркулнруемого жидкого NH3.
Конвертированный газ сжимают от 3—3,5 МПа до 18—20 МПа и подают в абсорбер с падающей пленкой, где С02 поглощают концентрированным раствором NH3 с образованием карбамата аммония. Большая часть теплоты абсорбции может быть регенерирована (предварительный нагрев котельной питательной воды). Содержание NH3 в поглотительном растворе составляет около 80% (масс.), что обеспечивает получение высококонцентрированного карбаматного раствора при 130—140 °С с массовым соотношением С02 : Н20 » 3,0—3,5.
Освобожденный от С02 конвертированный газ с примесью испаренного в абсорбере С02 аммиака [14—15% (об.)] подают в метанатор на окончательную очистку от СО и С02. Затем соединяют с газовым потоком, выводимым из реактора синтеза NH3, и направляют в пленочный абсорбер для поглощения NH3. (По другому варианту процесса, газ отмывают водой от аммиака до подачи на метанирование). Остаточное содержание NH3 в газе снижается до 0,5% (об.), и из абсорбера выводят высококонцентрированный раствор NH3, а также побочный поток сдувочного газа и основной газовый поток. Абсорбер сконструирован таким образом, чтобы избежать смещения рециклового и свежего газа перед сдувкой. Далее основной поток газа обезвоживают путем охлаждения и промывки жидким аммиаком. С этой целью в него впрыскивают часть NH3, рециркулнруемого в реактор синтеза CO(NH2)2. После регенерации тепла обезвоженный газ подают компрессором в реактор синтеза NH3.
Свежий карбаматный раствор из абсорбера С02 совместно с ре - циркулируемыми потоками NH3 и УАС поступает в нижнюю часть реактора синтеза CO(NH2)2, куда вводят также газовую смесь NH3 и С02 из стриппинг-дистиллятора. За счет теплоты конденсации этой смеси поддерживается тепловой баланс реактора.
Плав синтеза из верхней части реактора CO(NH2)2 поступает самотеком в стриппинг-дистиллятор, где он нагревается конденсирующимся паром. Часть непрореагировавших NH3 и С02 отпаривают в токе NH3 и возвращают в реактор. Оставшийся плав синтеза дросселируется и поступает на окончательную переработку.
Плав дистиллируют на трех ступенях (под давлением 1,8; 0,55 и 0,08 МПа) для выделения остаточных NH3 и С02 и после вакуум - испарения воды подают в грануляционную башню.
Дефицит тепла в I и II дистилляторах плава синтеза покрывают за счет охлаждения конвертированного газа из отделения получения синтез-газа. Тепло для III дистиллятора обеспечивают за счет конденсации паров из II дистиллятора. Водный конденсат из III дистиллятора (РУАС, полученный за счет конденсации части паров из II дистиллятора) после газожидкостной сепарации, дросселирования жидкости до давления 0,08 МПа и отпарки в кипятильнике остаточного NH3 сливается в канализацию. После отделения воды пары под давлением 0,08 МПа совместно, с газами из III дистиллятора поступают в абсорбционную колонну, где NH3 и С02 подвергают конденсации-абсорбции. Несконденсированные газы дистилляции под давлением 0,55 МПа, соединившись с холодным аммиачным раствором из абсорбера, работающего под давлением 0,08 МПа, конденсируются и поступают в качестве абсорбента в ректификационную колонну, работающую под давлением 1,8 МГІа, в которую снизу входят пары из I дистиллятора, а сверху — жидкая аммиачная флегма.
Отходящий сверху газовый поток представляет собой чистый (99,9%) NH3, а отводимый снизу жидкостный поток — РУАС. Оба эти потока рециркулируют в узел синтеза CO(NH2)2. Избыточный жидкий NH3 отводят за пределы установки.
Изложенный интегральный метод отличается следующими характерными особенностями [7, 20].
1. По сравнению с раздельным производством NH3 и CO(NH2)2 исключены узел отмывки С02 из конвертированного газа и узел конденсации NH3 из продукционной газовой смеси после реактора синтеза NH3.
2. Большая часть теплоты образования карбамата аммония утилизируется путем предварительного подогрева котельной питательной воды, проходящей по межтрубной зоне в том же направлении, что и поток аммиачной воды. В результате температура реакционной смеси превышает температуру кристаллизации карбамата аммония.
3. Влажный синтез-газ подвергается обезвоживанию под действием части NH3, рециркулнруемого в реактор синтеза CO(NH2)2, что дает экономию энергии.
4. Реактор синтеза карбамида работает в автотермичных условиях. Из-за отсутствия экзотермической реакции образования карбамата аммония из свежего сырья тепловой баланс реактора должен поддерживаться средствами извне. В интегральном процессе принят наиболее целесообразный способ подведения тепла: подача горячих паров из дистиллятора непосредственно в реактор. Это позволяет обойтись без карбаматного конденсатора и существенно упростить контур синтеза CO(NH2)2, сведя его до реактора и дистиллятора.
5. Во избежание отрицательного влияния рециркулируемой воды на ха в реакторе синтеза CO(NH2)2 создают большой избыток NH3.
Тепловой баланс реактора и дистиллятора определяет оптимальное значение хв, которое выбирают с таким расчетом, чтобы полностью конденсировать в реакторе пары, поступающие из раз - лагателя. 300
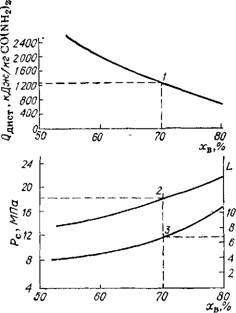
На рис. Х.5 показано, как идет процесс при разных значениях хв. Тепловой баланс замыкается при хв я» 70%. При более низкой хв пришлось бы отводить тепло из системы, например, за счет дополнительного конденсатора; ха^70% при 180°С достигается при L— 6,9 и под давлением 18—19 МПа.
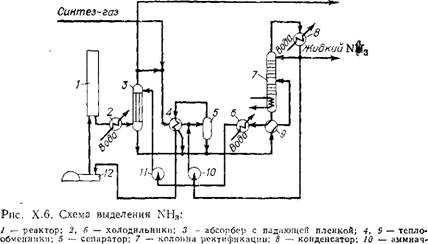
Результаты экспериментов наопытно-промыш - ленной установке. Один пз основных технологических элементов интегральной схемы «Сиам Проджетти» — новый процесс выделения NH3 из продукционной смеси после реактора синтеза NH3. Принципиальная схема процесса [21 ] выделения NH3 показана на рис. Х.6 и заключается в следующем (рассматривается вариант отдельной установки синтеза NH3). Газовый поток из реактора синтеза NH3 под давлением около 12 МПа охлаждают до 40 °С и направляют в узел абсорбции NH3. Абсорбцию осуществляют в теплообменнике с падающей пленкой, в котором поднимающиеся по трубам газы контактируют с нисходящей пленкой жидкости — воды или слабого раствора NH3. Теплоту абсорбции отводят охлаждающей водой снаружи труб. Благодаря эффективному охлаждению и мас - сообмену получается очень концентрированный раствор NH3 [50% (масс.) и выше], а содержание NH3 в газах снижается приблизительно до 0,5% (об.). Промытый газ, насыщенный водой, поступает в следующий узел осушки.
После удаления продувочных газов промытый газ смещивают со свежей N2—Н2-смесью и подают в регенеративный теплообменник, в котором он охлаждается высушенным газом до —15 ч—20 °С Здесь большая часть воды из влажного газа конденсируется до остаточного содержания 50 мг/л, а конденсат отводят в виде раствора аммиака.
|
Рис. Х.5. Зависимости (2Дист— хв (/), Рс — хв (2), L—x в (3) при tc= 180 °С и W = = 1,2 для блока синтеза и стриппинг-дистил - ляции. |
|
.Пунктиром обозначена величина фдист, соответствующая автотермическому режиму процесса синтеза. |
Затем по ходу потока в газ впрыскивают жидкий NH3. Часть этого NH3 адиабатически испаряется, вызывая дальнейшее пере-
|
Сдувочный газ
Ный насос; 11 — насос для раствора аммиака; 12 — компрессор. |
Охлаждение, а оставшийся жидкий NH3 отделяют от газа в конечном сепараторе; в жидком NH3 содержится практически вся Н20, которая была в газе до впрыскивания. За счет регулирования количества избыточного NH3 в конечном сепараторе получают в итоге раствор NH3 достаточной концентрации 185—90% (масс.) NH3], а остаточное содержание водяных паров в высушенном газе не превышает 1—3 мг/л. Жидкий аммиак впрыскивают не столько для охлаждения газа за счет испарения NH3, сколько для промывки газа избыточным жидким аммиаком и абсорбции последних следов воды. Время контакта между жидкостью и газом в системе осушки ограничено. Это дает возможность поддерживать в высушенном газе содержание NH3 ниже насыщения, т. е. абсорбция воды происходит быстрее испарения NH3. В результате содержание NH3 в газе возрастает от 0,5 всего лишь до 1,5—2% (об.), что приемлемо для нормальной работы реактора синтеза.
Полученный раствор NH3 ректифицируют, после чего получают жидкий NH3 (99,9%) и слабый раствор NH3 (5—10% (масс.) ]. Как уже ранее отмечалось, в объединенной схеме раствор NH3 используют для абсорбции С02 из конвертированного газа.
Процесс водной абсорбции NH3 был испытан на опытно-про - мышленной установке 1211. Экспериментальный пленочный абсорбер состоял из двух поставленных друг на друга одинаковых элементов длиной 5 м каждый с 19 трубами внутренним диаметром 20 мм (рис. Х.7). Аммиак и газ-носитель перед смешиванием подогревали до 150—180 °С, затем охлаждали до 40 °С и однородный по составу газовый поток направляли в абсорбер. Дозировочным насосом подавали абсорбент (воду или слабый раствор NH3) на верх абсорбера. Скорости потоков измеряли мембранными из - 302
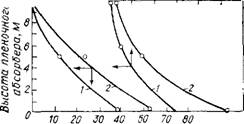
мерителями или ротаметрами. На входе, выходе и в середине абсорбера отбирали пробы и проводили полный химический анализ газов и жидкостей. Было проведено более 30 циклов под давлением 12,5 МПа с использованием азота и стехиометрической смеси синтеза (N2 Н - ЗН2). Экспериментально полученные кривые абсорбции (по двум полным испытаниям) приведены на рис. Х.8.
В результате проведенных испытаний пленочного абсорбера установлено [21]:
1) абсорбция NH3 водой (или слабым раствором NH3) до очень низких остаточных содержаний в теплообменниках с падающей пленкой практически осуществима и экономически целесообразна;
2) затопление происходит, лишь если в газовой фазе Re л*
300 ООО;
3) достигается высокий к. п. д. массообмена;
4) концентрация NH3 в слабом растворе не должна превышать 5—10% (масс.);
5) увеличив рабочее давление до 15 МПа, легко получить концентрированный раствор NH3 [75—80% (масс.) ].

|
Инертный газ |
|
Инертный газ |
|
Жидкий Nlio |
|
Аммиачная вода |
|
Вода- Рис. Х.7. Схема узла абсорбции NH;i ИТ, ИД, ИР, ИУ — измерители температуры, давления, расхода, уровня; Р—регулятор. 303 |
Полученные экспериментальные данные позволили уточнить математическую модель пленочного абсорбера, ранее составленную теоретически. Такая модель позволяет надежнее и быстрее конструировать пленочный абсорбер [21 ].
На той же опытно - промышленной установке были проведены опыты [20] по изучению процесса получения раствора карбамата аммония в массообмен - ном аппарате с падающей пленкой путем абсорбции С02 из газовой смеси с использованием высококонцентрированного раствора NH3.
Абсорбер С02 состоял из нижнего бар- ботажного отделения и двух верхних отделений типа падающей пленки. В каждом пленочном отделении высотой 5 метров — 7 труб внутренним диаметром 20 мм. Барботажная зона работает в адиабатических условиях, пленочные отделения охлаждаются за счет интенсивной циркуляции охлаждающей воды через межтрубное пространство. Испытания проводились под давлением 15 МПа при содержании С02 в синтез-газе в пределах 18—25% (об.).
Для обеспечения однородного состава газовой смеси и воспроизведения промышленных параметров смесь С02 и синтез-газа подогревали до 150—160 °С. Расходы газа и аммиачного раствора, наряду с температурой, регистрировали в нижней, средней и верхней частях абсорбера. В каждом опыте определяли химическим анализом: содержание С02 в газе на входе, концентрацию карбамата аммония в растворе в промежуточной и в выходной секциях, содержание NH3 в аммиачной воде, содержание NH3 и С02 в потоке отходящего газа.
Основные результаты экспериментов следующие. Работа узла абсорбции вполне надежна и остаточное содержание С02 незначительно. Забивок на выходе из абсорбера не наблюдалось. Получается очень концентрированный карбаматный раствор, в котором массовое соотношение С02 : Н20 = 3. При увеличении избытка NH3 в карбаматном растворе это соотношение увеличивалось до 5,5—6. Часть NH3 из раствора испаряется и переходит в газовую фазу. Содержание NH3 в отходящем газовом потоке составляет 10—30% (об.). Количество испаренного NH3 зависит как от избытка NH3, так и от Р и t в абсорбере. Давление в промышленных условиях составляет 18—20 МПа; при этом "в очищенном от С02 газе будет содержаться 14—15% (об.) NH3.
|
Концентрация аммиака 3 инертном газе %(о6.) w 0 2 4 б в К 1? |
|
Концентрации раствора аммиака, %(масс) |
|
Рис. Х.8. Экспериментальные кривые по результатам двух полных испытаний. |
Аммиачный раствор вводили двумя потоками: в нижнюю и верхнюю части абсорбера. При подаче одного потока только в верхнюю часть результаты испытаний оказались неудовлетворительными. Наиболее благоприятные результаты были получены 304
Таблица Х. З. Затраты энергоресурсов и сырья в процессах производства аммиака и карбамида (в расчете иа 1 т гранулированного карбамида) [22]
|
Раздельные установки мощностью |
|
Объединенная установка мощностью 1700 т/сутки CO(NH,)a |
|
1000 т/сутки NH3 и 1700 т/сутки CO(NH2)2 |
|
Статьи затрат |
|
24,87 |
|
20,89 0,35 |
|
0,35 0,05 |
Природный газ, включая затраты для
Технологических целей, X 106 кДж
Стоимость, долл. катализаторов химикатов
З
Расход, м3
|
1,3 |
|
1,3 |
|
265 |
|
210 |
Деминерализованная вода. . . . охлаждающая вода
При подаче безводного жидкого NH3 в нижнюю часть абсорбера и воды в его верхнюю часть. Хорошие результаты были достигнуты при температуре охлаждающей воды 110—140 °С в нижнем отделении и 60—90 °С в верхнем. Снизить температуру воды, циркулирующей в верхнем отделении, было невозможно из-за опасности выпадения кристаллов твердого карбамата аммония.
Эти испытания подтвердили техническую осуществимость двух основных стадий нового интегрального процесса — выделения NH3 и С02 из газовых смесей с получением высококонцентрированного карбаматного раствора. Исходя из этих экспериментальных данных и опыта проектирования производств NH3 и CO(NH2)2, фирма «Снам Проджетти» выполнила комплексный проект объединенной установки NH3 и CO(NH2)2.
Экономические преимущества интегрального процесса «Снам Проджетти». Создатели процесса указывают на следующие достоинства объединенной схемы [20, 22, 23]:
Экономия тепловой энергии, потребляемой при обычном методе удаления С02 из конвертированного газа;
Экономия тепловой и/или механической энергии, требуемой для отделения NH3 от непрореагировавших N2 и Н2;
Экономия механической энергии на сжатие С02 до давления синтеза CO(NH2)2;
Экономия капиталовложений за счет отказа от традиционного узла поглощения С02 и ступени отделения NH3 (в контуре синтеза NH3), сжатия С02 и карбаматного конденсатора (в контуре синтеза карбамида). В интегральном процессе требуются только воздушный компрессор и компрессор для сырого конвертированного газа, который, благодаря сравнительно высокой плотности последнего по сравнению с синтез-газом, имеет меньше ступеней сжатия и/или меньшее число оборотов.
С целью количественной оценки технико-экономических преимуществ применения объединенного процесса были сопостав
лены [20 ] показатели обычных современных раздельных установок NH3 и CO(NH2)2 и объединенной установки NH3—CO(NH2)2 по схеме «Снам Проджетти». Производительность установки по NH3 — 1000 т/сутки, гранулированного CO(NH2)2 — 1700 т/сутки; сырье — природный газ. Сравниваемые установки состоят из следующих узлов.
Установка с раздельными
Производствами NH3 Объединенная установка
И CO(NH2)2 NH3-CO(NH2)2
Паровая конверсия природного Паровая конверсия природного газа, конверсия СО, удале - газа и конверсия СО под да - ние С02, метанирование (все влением —3 МПа эти стадии под давлением —3 МПа)
Компримирование синтез-газа Компримирование конвертиро - от 3 до 24 МПа центробеж - ванного газа до —20 МПа ным компрессором центробежным компрессором
Синтез NH3 под давлением Синтез NH3, получение
24 МПа в реакторе типа NH2COONH4, дегидратация «1<венчинг»-аппарат (реактор последнего с получением с охлаждением) СО (NH,)2 под давлением 19—
20 МПа"
Синтез CO(NH2)2 под давле - Система пароснабжения (пара - нием 15 МПа по стриппинг- метры пара 11 МПа и 510 °С) процессу «Снам Проджетти» с бойлером отработанного теп-
Общая энергоустановка для ла на линии топливного газа агрегатов синтеза NH3 и с установки конверсии при - CO(NH2)2 с получением пара родного газа; технологический под давлением 11 МПа и пар предварительно подается с температурой 510 °С для на турбины рабочих турбин
Для обоих сравниваемых случаев электроэнергию, необходимую для технологических целей, обеспечивает генератор с приводом от турбины, поэтому расходы пара и электроэнергии не входят в статьи затрат.
В табл. Х. З сопоставлены удельные затраты энергоресурсов и сырья для обоих случаев. Анализ капитальных затрат этих двух вариантов показал, что для объединенного процесса стоимость капиталовложений на 20% ниже. Кроме того, в случае объединенной установки за счет более низких расходных коэффициентов снижение себестоимости CO(NH2)2, по сравнению с обычными процессами, составит 16% [22].
Факторы, определяющие целесообразность практического применения интегральной схемы. Создатели интегральной схемы «Снам Проджетти» проанализировали факторы, определяющие целесообразность ее практического применения, и пришли к следующему заключению [22].
Главный недостаток объединения двух процессов — недостаточная эксплуатационная гибкость технологического процесса, обусловленная строгой зависимостью двух производств. Однако, и при производстве NH3 и CO(NH2)2 на раздельных установках между ними существует определенная взаимосвязь. Действи - 306 тельно, в случае прекращения производства NH3 необходимо останавливать установку получения CO(NH2)2, вследствие отсутствия С02, образующегося при синтезе NH3. Напротив, отключение установки синтеза CO(NH2)2 не влечет за собой остановку производства NH3 при наличии соответствующего склада для продукта. В случае объединения отключение одной из двух установок влечет за собой отключение другой установки. При этом должны учитываться следующие факторы:
1) опыт свидетельствует о том, что степень надежности аммиачной линии бывает ниже, чем степень надежности производства CO(NH.2)2. Иными словами, остановки в основном будут иметь место в агрегате NH3; поэтому тот факт, что агрегат NH3 в интегральном процессе связан с агрегатом CO(NH2)2, не обязательно означает значительное снижение рабочей гибкости;
2) цель объединения двух установок заключается не только в усовершенствовании их, но и в упрощении процесса и повышении его надежности за счет уменьшения числа машин и аппаратов, входящих в интегральную схему производства NH3 и CO(NH2)2. В этом отношении интегральная установка более надежна, чем раздельное производство.
Поэтому, с одной стороны, объединение производств NH3 и CO(NH2)2 несколько снижает эксплуатационную гибкость, так как установка очистки конвертированного газа от С02 является в то же время установкой синтеза CO(NH2)2, которая на первый взгляд значительно сложнее, чем обычная установка отмывки С02. Но, с другой стороны, такое объединение означает более высокую потенциальную надежность, обусловленную упрощением установки в части процессов синтеза и NH3, и CO(NH2)2 на базе интеграции. Только опыт покажет, какой из этих противоположных эффектов будет иметь большее влияние на надежность всего производства.
Экономичность и простота новой технологии, разработанной итальянской фирмой, позволяют считать ее перспективной.
Мы рассмотрели достоинства и недостатки прогрессивных интегральных схем. Остается разобрать последний вопрос: при каких условиях станет возможным их практическое применение. По нашему мнению, для этого необходимо:
1) ослабить жесткую связь объединяемых производств; для этого, вероятно, следует предусматривать частичное использование производственных мощностей по выпуску одного из продуктов при вынужденной остановке линии по выпуску другого продукта;
2) обеспечить полную автоматизацию управления производством на основе АСУТП с применением УВМ;
3) за счет технического усовершенствования технологии и оборудования, а также высокой культуры обслуживания и эксплуатации снизить до минимума возможность аварийных остановок;
4) располагать персоналом высокой квалификации.