Физико-химические особенности получения сварных, паяных и клеевых соединений
МЕХАНИЗМ ОБРАЗОВАНИЯ МОНОЛИТНЫХ
СОЕДИНЕНИЙ ТВЕРДЫХ ТЕЛ
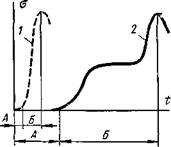
На первый взгляд кажется, что образование монолитного соединения двух одинаковых монокристаллов с идеально гладкими и чистыми поверхностями возможно при любой температуре и без приложения внешней энергии. Для этого достаточно сблизить их поверхности на расстояние, соизмеримое с параметрами кристаллической решетки (порядка долей нанометра). Тогда между сопряженными атомами возникнут связи, граница раздела Д (рис. 1.1) исчезнет и произойдет сварка. Такой процесс кажется вероятным и не противоречит второму началу термодинамики, так как свободная энергия системы при этом должна уменьшиться на величину энергии двух исчезнувших поверхностей раздела.
|
|
|
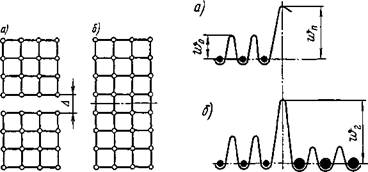
Рис. 1.2. Энергетический барьер потенциальной энергии системы атомов у поверхности кристалла (а) и иа границе твердой и жидкой фаз в начальный период их контакта (б) |
|
Рис. 1.1. Схема образования соединения двух монокристаллов с идеально чистыми н гладкими поверхностями: |
|
кристаллы до (о) и после (б) соединения |
В действительности даже в идеальном случае для соединения поверхностей требуется затрата энергии. Дело в том, что любому
устойчивому состоянию системы соответствует определенный минимум энергии атома. Каждый атом находится как бы в потенциальной лунке и переход из одного устойчивого состояния в другое возможен только путем преодоления энергетического барьера (рис. 1.2).
Внутри кристалла каждый атом удерживается симметрично направленными силами связи. На свободной поверхности кристалла или жидкости атом неуравновешен вследствие отсутствия связи с одной стороны (вакуум) или из-за ее ослабления. Это вызывает повышение энергии поверхностного слоя кристалла ш„. Если для перемещения внутри тела атому необходима энергия wo (см. рис. 1.2), то для выхода в окружающую среду ш„, причем w„>wо. Поэтому для соединения двух монокристаллов в один требуется деформационная, или тепловая, энергия извне, превышающая граничную энергию wr.
Внешняя энергия деформации будет затрачиваться на преодоление сил отталкивания, возникающих между сближаемыми поверхностными атомами. Когда расстояния между ними будут равны межатомному расстоянию в решетке кристаллов, возникают квантовые процессы взаимодействия электронных оболочек атомов. После этого общая энергия системы начнет снижаться до уровня, соответствующего энергии атомов в решетке целого кристалла, и появится выигрыш энергии, равный избыточной энергии поверхностных атомов кристаллов до их соединения — энергии активации.
Тепловая энергия, сообщенная поверхностным атомам при повышении температуры, увеличивает вероятность развития квантовых процессов электронного взаимодействия в соединении.
Стадийность процесса сварки. Опытный материал и теоретический анализ показызают, что сварку и пайку можно отнести
|
Рис 1.3. Кинетика изменения прочности соединения а в зависимости от длительности сварки t (топохимические кривые) при быстром (/) и медленном (2) развитии стадий образования физического контакта А и химического взаимодействия Б |
|
|
к классу так называемых топохими - ческих реакций, которые отличаются двухстадийностью процесса образования прочных связей между атомами соединяемых веществ (рис. 1.3). Двухстадийность характерна только для микроучастков соединяемых поверхностей.
На первой стадии А развивается физический контакт, т. е. осуществляется сближение соединяемых веществ на расстояния, требуемые для межатомного взаимодействия, а также происходит подготовка поверхностей к взаимодействию. На второй стадии Б — стадии химического взаимодействия — заканчивается процесс образования прочного соединения.
Практически получение монолитных соединений осложняется двумя факторами:
свариваемые поверхности имеют микронеровности (даже при тщательной обработке), высота которых измеряется микрометрами. Поэтому при совмещении поверхностей контакт возможен лишь в отдельных точках;
свариваемые поверхности имеют загрязнения, так как на любой поверхности твердого тела адсорбируются атомы внешней среды.
Для качественного соединения материалов необходимо обеспечить контакт по большей части стыкуемой поверхности и активизировать ее.
Энергия активации. Активация поверхности заключается в том, что поверхностным атомам твердого тела сообщается некоторая энергия, необходимая:
а) для обрыва связей между атомами тела и атомами внешней среды, насыщающими их свободные связи;
б) для повышения энергии поверхностных атомов до уровня энергетического барьера охватывания, т. е. для перехода их в активное состояние.
Такая энергия активации может в общем случае сообщаться в виде теплоты (термическая активация), упругопластической деформации (механическая активация), электронного, ионного и других видов облучения (радиационная активация).
СВАРКА ПЛАВЛЕНИЕМ И ДАВЛЕНИЕМ
При сварке плавлением и пайке сближение атомов твердых тел осуществляется вследствие смачивания поверхностей тел жидким металлом (припоем, расплавом), а активация поверхности твердого металла — путем сообщения ее частицам тепловой энергии. Жидкий металл может растекаться по всей поверхности тела и обеспечивать соприкосновение и прилипание (или адгезию) его молекул и поверхностного слоя твердых тел.
При затвердевании расплавленного материала слабые адгезионные связи заменяются прочными химическими связями, соответствующими природе соединяемых материалов и типу их кристаллической решетки. При сварке плавлением вводимая энергия (обычно тепловая) должна обеспечивать расплавление основного и присадочного материалов, оплавление стыка, нагрев кромки и т. д. При этом происходит усиленная диффузия компонентов в расплавленном и твердом материалах, их взаимное растворение. Эти процессы, а также кристаллизация расплавленного металла сварочной ванны (или припоя) обеспечивают объемное строение зоны сварки, что обычно повышает прочность сварного соединения.
Сварка плавлением происходит без приложения осадочного давления путем спонтанного слияния объемов жидкого металла.
Она обычно не требует тщательной подготовки и зачистки соединяемых поверхностей.
При сварке плавлением обе стадии процесса соединения — физический адгезионный контакт и химическое взаимодействие, сопровождаемое диффузией, — протекают достаточно быстро (см. рис. 1.3, кривая 1). Для однородных металлов это не опасно. Но в случае разнородных материалов с ограниченной взаимной растворимостью практически трудно получить соединения без хрупких интерметаллических прослоек в контакте.
При быстром образовании физического контакта твердого тела с расплавом, например при сварке путем расплавления одного из соединяемых материалов, сначала на границе твердой и жидкой фаз будет наблюдаться пик межфазной энергии wr, аналогичный шп (см. рис. 1.2,6), так как переход атомной системы в новое состояние происходит не мгновенно, а за некоторый конечный промежуток времени. Длительность ретардации (задержки) пика поверхности раздела, как называют этот период, может быть приближенно рассчитана как время жизни атома перед потенциальным барьером или определена опытным путем. На основании этих данных можно определить допустимую длительность контакта твердой и жидкой фаз и оптимальную температуру сварки или пайки.
При сварке давлением (в твердом состоянии) сближение атомов и активация (очистка) поверхностей достигаются в результате совместной упругопластической деформации соединяемых материалов в контакте, часто одновременно с дополнительным нагревом.
Длительность стадий образования физического контакта А и химического взаимодействия Б здесь существенно больше, чем при сварке плавлением, и зависит от ряда факторов: физикохимических и механических свойств соединяемых материалов, состояния их поверхности, состава внешней среды, характера приложения давления н других средств активации (ультразвук, трение и т. д.).
В последнее время предложены методы приближенного расчета параметров режима сварки статическим давлением, которые подтверждаются опытом. Длительность процесса образования физического контакта, заключающегося в смятии микронеровностей, рассчитывают по скорости ползучести. Длительность второй стадии — химического взаимодействия — оценивают по уравнению Больцмана как длительность периода активации.
Расчеты основаны на представлениях о схватывании материалов в результате ползучести на контактных поверхностях и образовании прочных химических связей в местах выхода и перемещения вакансий, дислокаций и скоплений. Выход дислокаций на контактную поверхность активирует ее путем разрыва насыщенных связей, что приводит к образованию активных центров.
Однако принято считать, что при соединении металлов в твердом состоянии имеет значение не только схватывание, но и спекание. Спекание — комплекс диффузионных процессов, протекающих во времени при повышенных температурах. Схватывание — бездиффузионное явление — объединение кристаллических решеток, находящихся в контакте тел в результате их совместного пластического деформирования. Относительная роль схватывания и спекания в разных методах соединения металлов различна и определяется в основном температурой, временем и давлением в контакте. Например, диффузионную сварку при большом времени выдержки можно считать основанной на явлении спекания. Во всех остальных случаях схватывание первично, а диффузионные и рекристаллизационные процессы, если они вообще происходят, вторичны.
ПАЙКА И СКЛЕИВАНИЕ
Пайкой обычно называют процесс соединения материалов с помощью припоя без их расплавления. Процессы сварки и пайки часто бывает трудно разграничить, например при сварке разнородных металлов в сочетаниях сталь и медь, вольфрам и молибден и др., когда расплавляется только один, более легкоплавкий металл. Поэтому в дальнейшем при анализе источников энергии целесообразно объединять сварку и пайку одним термином — сварка. Пайку можно выполнить с использованием тех же энергетических процессов, что и сварку.
Образование непрерывной межатомной связи при пайке происходит в процессе смачивания припоем поверхности соединяемых деталей. Смачивание и связь твердого тела с жидкостью может определяться электростатическими силами Ван-дер-Вааль - са и силами химического взаимодействия.
Подобно физической адсорбции, первый тип контакта называют физическим (обратимым) смачиванием. Второй тип контакта, подобно хемосорбции, называют химическим (необратимым) смачиванием. Работа адгезии во втором случае в тысячи раз больше, чем в первом, и составляет около 5 • 102... ...5- 103 Дж/моль.
Для осуществления химического смачивания при пайке необходим нагрев деталей и припоя, а также активация в специальных средах при обработке поверхности флюсом.
Склеивание может происходить практически без введения энергии в месте соединения благодаря силам адгезии (прилипания) между жидким клеем и молекулами поверхностных слоев твердого тела, а также химическим реакциям. Способность клея соединять изделия объясняется силами остаточного химического сродства между находящимися на поверхности молекулами клея и склеиваемого материала. Эти силы примерно в Ю...100 раз меньше основных сил химической связи в простых молекулах.
Они, например, порождают у жидкостей явление поверхностного натяжения, способность смачивать или не смачивать поверхности различных материалов.
В случае высокомолекулярных соединений, когда мономерная молекула, повторяясь в полимере тысячи раз, образует макромолекулу, силы адгезии возрастают пропорционально росту молекулярной массы. Эти силы, имея электрическую природу, в значительной степени зависят от химической структуры клея и склеиваемого материала.
Полярные группы — карбоксильные, спиртовые, амино-, эпоксидные и другие — значительно увеличивают адгезию клея к полярным материалам. Для увеличения адгезионных сил при склеивании некоторых неполярных материалов последние подвергают термической или химической обработке в целях получения на их поверхности некоторого количества полярных групп. Наличие или отсутствие адгезии клея к склеиваемому материалу легко определить по смачиваемости клеем этого материала.
Для улучшения адгезии во всех случаях склеиваемая поверхность подвергается тщательной очистке и обезжириванию (иногда искусственно повышается степень ее шероховатости).
Однако прочность клеевого соединения определяется не только адгезией, но и когезией, т. е. силами взаимодействия между молекулами самого клея. Силы когезии термопластических клеев имеют ту же природу, что и силы адгезии. У клеев на основе термореактивных связующих когезионные силы внутри клеевого шва после его отвердевания будут усиливаться также благодаря образованию обычных химических связей.
Таким образом, прочность клеевых соединений определяется химическими и межмолекулярными силами притяжения элементарных частиц клея и склеиваемого материала. В начальной стадии процесса, когда силы взаимодействия, обусловленные смачиванием и межмолекулярным взаимодействием частиц, в основном слабы, прочность клеевого соединения мала. Далее при возникновении химических связей прочность увеличивается.
Например, при контакте полиамидного клея со сталью возникают химические соединения, где атом азота (полиамида) делит свои два электрона с атомами железа (стали). Одновременно между атомами кетогруппы С=0 и атомом кислорода в оксиде железа возникает дополнительная ионная связь. Таким образом, возникает так называемое хелатное соединение. Другие клеи (на основе толуилендиизоцианитов) при взаимодействии с атомами кремния (стекла) образуют ковалентные связи.
Существенное отличие склеивания от большинства процессов сварки и пайки — то, что при затвердевании клея вследствие охлаждения, полимеризации и других физико-химических явлений взаимное растворение и диффузия соединяемых материалов, как правило, полностью отсутствуют.