СКОРОСТЬ АДСОРБЦИИ
Гыстро несутся поезда и автомашины, с сверхзвуко - вой скоростью прочерчивают небо реактивные самолеты, как молния летит стружка из-под резца токаря-скоростника — вся соврехменная техника стремится овладеть большими скоростями. Даже такой, казалось бы, узако - ненно медленный процесс, как выращивание больших кристаллов из раствора солей, и тот переведен на большие скорости, чтобы успевать удовлетворять потребности техники в специальных кристаллах[15]).
Стоит ли говорить об ускорении процесса адсорбции? Ведь молекулы газа движутся с огромными скоростями (молекула азота, например, при обычной температуре обладает скоростью более четырехсот метров в секунду) и, конечно, практически мгновенно достигнут поверхности адсорбента и закрепятся на ней. Все эти рассуждения правильны, если речь идет об адсорбции на гладкой, плоской поверхности, доступной для молекул газов и паров. Но мы уже знаем, что технические адсорбенты — пористые тела с очень сильно развитой внутренней поверхностью.
Современная техника требует, чтобы и адсорбция была скоростным процессом. Возьмите, к примеру, знакомый всем противогаз. Вам, конечно, известно, что слой активированного угля, находящийся в противогазовой коробке, предназначен для поглощения паров отравляющих веществ, проходящих через него. Так вот, нужно успеть, чтобы весь процесс поглощения завершился в слое угля, чтобы в легкие человека не попало такого количества ве
Щества, которое, по современным воззрениям медицины, является токсическим, то есть могущим повредить здоровью.
С какой же скоростью проходит вдыхаемый воздух через слой адсорбента в противогазе? Сколько времени отпускают нам биологи для защиты одного вдоха человека?
Время это очень мало. Работающий человек вдыхает воздух со средней скоростью около пятидесяти литров в минуту. Поперечное сечение коробки противогаза приблизительно равно 70 См2. Значит, через каждый квадратный сантиметр свободного сечения воздух проходит со скоростью 0,7 литра в минуту. А так как слой поглотителя имеет в среднем толщину 5—7 сантиметров, молекула отравляющего вещества проходит через него в течение всего только нескольких долей секунды. В такой ничтожный промежуток времени отравляющее вещество должно быть удалено из вдыхаемого воздуха, вернее, удалено в такой степени, чтобы остатки его не представляли вреда для человеческого организма.
Вот отсюда и возникает необходимость иметь сорбент с большой скоростью поглощения. Сорбент может обладать огромной внутренней поверхностью пор, но, если эта поверхность трудно доступна, кому нужен такой сорбент в наше время больших скоростей?
Техническая мысль направлена по такому пути: создать адсорбент со структурой, напоминающей коридорную систему в жилых домах. Вот перед нами широкие коридоры, по которым свободно несутся молекулы газа. Доходя до отдельных квартир, молекулы проникают туда и в них размещаются. Необходимо сделать все точки поверхности сорбента легко доступными для молекул газа. Только тогда сорбент будет отвечать требованиям большой скорости адсорбции.
Такое требование может быть выполнено. Вспомните, что активированный уголь, приготовленный из порошка антрацита, будет отвечать этим условиям: промежутки
Между порошинками представляют собою «коридоры», а разрыхленная поверхность каждой порошинки — отдельные «квартиры». Вот почему активированный уголь, приготовленный из порошкообразного материала, повсеместно вошел в технику противогазового дела и вытеснил уголь, получаемый из натурального растительного сырья.
Не удивляйтесь тому, что мы сейчас перенесемся на десятки лет назад, к войне 1914 года. Именно в этой войне немецкие империалисты впервые применили против наших войск страшное оружие — отравляющие газы. На борьбу с химическим оружием выступили русские химики; это было вполне естественно: раз оружие химическое, то и средства защиты должны были тоже основываться на химии.
Первым отравляющим веществом был газ хлор. Вещества, поглощающие хлор, были известны уже давно, и, конечно, они-то и были применены в первую очередь. Раствор гипосульфита, хорошо знакомый всем фотолюбителям, прекрасно поглощает хлор по следующей реакции:
Ыа25203 + 5Н20 + 4С12 = 8НС1 + Н,504 + Ыаа804.
Гипосульфит вода хлор соляная серная сернокислый
Кислота кислота натрий
Были изготовлены сотни тысяч марлевых повязок-масок, пропитанных раствором гипосульфита — главного поглощающего вещества, соды — нейтрализатора образующихся кислот и глицерина — вещества, обеспечивающего постоянную влажность маски. Последнее было совершенно необходимым, так как перечисленные химические реакции могли происходить только в присутствии влаги. Такая маска довольно хорошо поглощала хлор по крайней мере в тех количествах, которые применялись на войне. Когда немцы применили фосген, в пропитку маски пришлось добавить уротропин (известное лекарство), и маска стала более универсальной.
Однако стало ясно, что нельзя же пропитать маску всеми химикалиями, способными поглощать все вещества, которые может применить противник. Необходимо было применить более универсальный способ поглощения паров отравляющих веществ. Этот способ был найден, и вы уже догадываетесь, какой.
Бессмертна заслуга русского химика Николая Дмитриевича Зелинского, не только предложившего применить адсорбционный метод поглощения отравляющих веществ, но и воплотившего его в жизнь. Ученые хорошо знают, что предложить какое-либо новшество — это даже не полдела, а, скорее, одна десятая всего дела. Ведь важно не только открыть новый способ, нужно опробовать его сначала в лаборатории в сотнях и тысячах опытов, затем перейти к испытаниям в более крупных масштабах, потом в полу - производственных и, наконец, в производственных условиях.
При этом необходимо позаботиться о доступности исходного сырья. Для сырья же, которое шло на военные средства защиты, ставилось и ставится сейчас еще одно важное условие: оно должно быть отечественного происхождения, не должно быть связано с импортом.
Всего этого еще мало. Нужно было связать в единый производственный коллектив несколько отраслей промышленности, так как для изготовления нового противогаза требовался не только активированный уголь, но и жестяная коробка и резиновая маска. Вспомните, что в те годы у нас не было своего каучука для изготовления резины, и вы поймете, какие колоссальные трудности пришлось преодолевать Н. Д. Зелинскому и его сотрудникам. Да и этого было еще мало. Нужно было наладить испытания активированного угля, полигонные испытания всего противогаза в целом, разработать специальные инструкции для обучения солдат пользованию этим новым, невиданным средством защиты.
Все трудности были преодолены, и русская армия получила первый в мире угольный войсковой противогаз — универсальное средство защиты. Явление адсорбции, поглощения, спасло на фронте десятки тысяч человеческих жизней.
Стоит ли рассказывать о том, как устроен угольный противогаз? Пожалуй, не стоит: все видели его, занимались в кружках противовоздушной обороны, может быть, даже сами о нем рассказывали.
Однако раз мы уж говорим о скорости адсорбции, стоит подробнее ознакомиться с тем, каким образом «работает» слой угля, помещенный в противогазовой коробке. Поглощение молекул отравляющих веществ происходит в условиях движущегося потока воздуха, или, как говорят, в динамических условиях. Ясно, что довольно толстый — около шести сантиметров — слой угля будет использован не сразу, а постепенно, послойно.
Ученик Н. Д. Зелинского профессор Николай Александрович Шилов [16]) в период первой империалистической войны, во фронтовых условиях, развернув работу походного вагона-лаборатории, детально исследовал новое явление—поглощение газов и паров из тока воздуха. Чтобы наблюдать, с какой скоростью идет постепенное заполнение слоя угля молекулами отравляющего вещества, Шилов построил модель этого слоя. Небольшие количества угля были помещены в стеклянные трубочки, соединенные последовательно друг за другом. Все трубочки были предварительно взвешены на чувствительных весах. Опыт начинался с того, что через такую цепь пропускался ток воздуха, содержащий пары хлора. Через определенные промежутки времени трубочки разъединялись и по отдельности взвешивались.
Шилов изменял в отдельных опытах скорость тока воздуха, концентрацию хлора в нем, число отдельных трубочек и их размеры — словом, поступал так, как поступает всякий исследователь-экспериментатор, пытающийся объяснить, осмыслить новое явление.
Огромное количество разнообразных опытов было проделано и в вагоне-лаборатории, и по возращении с фронта. Н. А. Шилову удалось выразить довольно сложные физические закономерности, управляющие поглощением газов и паров в динамических условиях, очень краткой математической формулой; она и до сих пор называется «формулой Шилова». Формула отвечала на основной вопрос противогазового дела: сколько времени будет защищать человека слой угля такой-то длины при таких-то условиях пользования противогазом?
Давайте и мы с вами построим модель противогаза. Только мы выберем другой способ моделирования, часто применяющийся в науке и технике. Что больше всего интересует нас в свойствах угля, применяемого в противогазе? Во-первых, его емкость, способность поглощать то или иное количество паров, и, во-вторых, как мы уже не раз говорили, скорость поглощения этих паров. Ну вот, мы и возьмем вместо отдельных слоев угля сосуды с постоянной емкостью, а вместо газовоздушной смеси — воду.
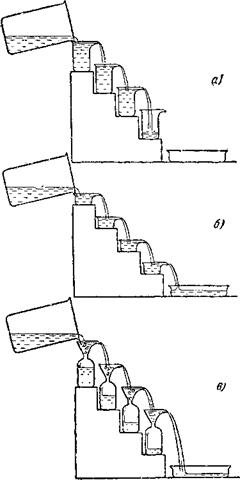
На рис. 8, А изображена такая модель из нескольких сосудов, стоящих на лесенке так, что из первого сосуда вода может переливаться во второй, из второго — в третий и т. д.
Пустим струю воды в первый сосуд. Пройдет некоторое время, пока из нижнего сосуда вода начнет выливаться в чашку. От чего будет зависеть это время? Конечно, от скорости потока: чем сильнее пустим мы воду, тем быстрее заполнится вся система. Это время уменьшится, если мы возьмем сосуды меньшей емкости (рис. 8, б).
|
Рис. 8. Водяная модель процесса послойной отработки сорбента. |
Вот мы и получили на нашей модели уже две закономер* ности: чем больше скорость тока газовоздушной смеси, чем меньше емкость угля, тем меньше «время защитного действия», то есть время от начала пропускания газа через слой до появления его за слоем.
Посмотрите на рис. 8, В. Емкость сосудов осталась той же, но скорость заполнения их значительно уменьшилась: у сосудов очень узкие горлышки. Вода, не успев заполнить первый сосуд, уже перебрасывается во второй, частично заполняет и третий — в общем, нарушилась вся стройность и последовательность процесса. Ясно, что вода начнет выливаться в чашку еще задолго до того, как будут использованы емкости всех сосудов. Последний из них только-только начнет заполняться, а опыт придется закончить: истекло «время защитного действия».
Мы сделали на нашей модели еще одно важное наблюдение. Чем меньше скорость заполнения емкости угля адсорбируемым веществом, тем меньше время защитного действия, тем хуже будет использован весь слой угля за время опыта. Последний слой угля почти не будет отработан, он только-только начал адсорбировать пары, а противогаз придется сменить: он уже не годен и пользоваться им опасно.
Значит, уголь, применяемый для поглощения, должен обладать не только большой адсорбционной емкостью, но и структурой, обеспечивающей большую скорость поглощения. А как достигается такая структура, мы уже говорили.
До сих пор нас не очень интересовал вопрос: что же будет, если адсорбент поместить в атмосферу, содержащую смесь двух или нескольких газов или паров? Будут ли они все сразу одинаково адсорбироваться или предпочтение будет отдано какому-нибудь одному из них?
Из смеси будут адсорбироваться все пары, но в большей или меньшей степени. Чем сильнее, крепче связь, обусловленная силами молекулярного притяжения между молекулами газа и поверхностью адсорбента, тем более конкурентоспособен данный газ, тем сильнее и полнее вытесняет он с поверхности остальные адсорбировавшиеся молекулы. Пары спирта, например, адсорбировавшиеся на поверхности угля, могут быть вытеснены, конечно не полностью, парами бензола, так как молекулы последнего прочнее связываются с поверхностью угля.
Водяные пары очень прочно связываются с поверхностью силикагеля и могут вытеснять с нее пары бензола, если они ранее были адсорбированы. Подобных примеров можно привести множество.
Явление вытеснения одного газа другим будет, вероятно, сказываться и на процессе динамического поглощения. Чтобы убедиться в этом, обратимся снова к нашей модели. Одна жидкость должна вытеснять другую из сосуда. Возьмем для наших целей насыщенный раствор поваренной соли и подкрасим его чернилами.
Повторим самый первый опыт и будем вести его почти до конца, когда только-только начнет заполняться последний сосуд. Теперь пустим в верхний сосуд «лучше адсорбирующийся газ», то есть более тяжелую жидкость, подкрашенный насыщенный раствор поваренной соли. Раствор сейчас же начнет вытеснять воду из верхнего сосуда, и вся система придет снова в действие. Из нижнего сосуда довольно долго будет вытекать неокрашенная вода. Посмотрите на нашу лестницу — на ней вся гамма оттенков: на самом верху раствор окрашен наиболее интенсивно, внизу же в сосуде совсем чистая вода.
Вот еще наблюдение, сделанное при помощи модели, Хорошо адсорбирующийся газ, впущенный в противогазовую коробку, будет вытеснять из слоя угля ранее содержавшееся в нем вещество, если оно сорбируется хуже. В технике явление вытеснения с успехом используется; как это делается, мы увидим в дальнейшем. В противогазовом деле вытеснение одного вещества другим иногда представляет большую опасность. Представьте себе, что противогаз успешно защитил вас от вдыхания паров какого - нибудь отравляющего вещества. Если этим же противогазом пользоваться в дальнейшем в атмосфере даже не отравляющего вещества, а такого, пары которого хорошо поглощаются, например в атмосфере паров бензина, вы рискуете пострадать от вытесненного из противогаза отравляющего вещества, о котором вы даже могли и забыть.
Но не тревожьтесь: во-первых, технологи в настоящее время достигли больших успехов в деле приготовления активированных углей с большой удерживающей способностью; стало не так-то легко вытеснить одно вещество другим. Во-вторых, если вы даже не знаете устройства и свойств противогаза, применяемого в промышленности, специальная служба защиты не разрешит вам проделывать рискованные опыты, только что описанные мною.
Мы уделили довольно много места описанию процесса поглощения газов и паров из тока воздуха. И это не случайно: все технологические процессы, в которых применяется явление сорбции и которые мы опишем в дальнейшем, связаны именно с динамикой поглощения газообразных или растворенных веществ. Технологически всегда удобнее пропускать раствор через слои зерненого адсорбента и непрерывно получать готовый продукт, чем смешивать отдельные порции раствора с поглотителем и затем отделять готовый продукт от адсорбента при помощи отфильтровы - вания, центрифугирования или других громоздких операций. А уж о газовых смесях и говорить не приходится: пропускание газовоздушной смеси через слой адсорбента — единственно технологически возможный способ ее адсорбционной очистки.