БЕЛКОВЫЕ ГИДРОЛИЗАТЫ
Для улучшения вкусовых качеств пищевых концентратов обеденных блюд, главным образом супов, применяют белковые гидролизаты.
Белковыми гидролизатами называют продукты гидролитического расщепления белков, состоящие в основном из отдельных аминокислот, их натриевых солей и полипептидных остатков.
Натриевые соли аминокислот, особенно глутаминовой кислоты (глутаминат натрия), обладают способностью усиливать естественный вкус таких продуктов, как мясо, рыба, овощи, при добавлении к блюду в небольших количествах.
Сами белковые гидролизаты обладают приятным мясным и грибным вкусом, обусловленным составом аминокислот, их натриевых солей и продуктами вторичного синтеза (меланоидины и т. п.).
Используя направленный гидролиз и строго подбирая сырье, можно получить белковые гидролизаты определенного вкуса (например, куриного бульона).
По вкусовым качествам и физиологическому действию белковые гидролизаты незначительно отличаются от мясных бульонов. Отсутствие в их составе пуриновых оснований, которые обычно присутствуют в мясном бульоне, дает возможность рекомендовать их в пищу человеку независимо от его возраста, основным сырьем для производства белковых гидролизатов служат продукты, содержащие белок, главным образом растительного происхождения (шроты и жмыхи масличных культур), используют для этой цели также казеин молока и др. Этим, между прочим, обусловливается низкая стоимость гидролизатов.
Предпочтение следует отдавать такому сырью, в котором полнее представлены аминокислоты, особенно незаменимые, и содержится больше азота и меньше жира и Сахаров. Казеин молока и соевый шрот являются с этой точки зрения желательным сырьем.
В СССР разработано два способа производства белковых ги - дролизатов: кислотный (химический) и ферментативный (биохимический). Оба они внедрены в промышленность.
Наиболее ценные с физиологической точки зрения гидроли - заты получают ферментативным способом. В ферментативном гидролизате сохраняются все аминокислоты, содержащиеся в сырье, в том числе и такие дефицитные, как триптофан и лизин, которые разрушаются при кислотном гидролизе.
При получении кислотного белкового гидролизата наблюдаются значительные потери аминного азота. По данным Р. М. Кудрявцевой и других исследователей, потерн а-аминного азота на стадиях технологического процесса составляют: при гидролизе белка соляной кислотой 35—42%, при нейтрализации смеси — до 12%, при отделении гуминовых веществ — до 19%, при осветлении гидролизата — до 5,7%.
При гидролизе белка в производственных условиях значительно разрушаются аминокислоты: цистин на 20%, тирозин на 37%, фенилаланин на 43%, лизин на 40%, гистидин на 38%, ас- парагиновая кислота на 17%.
Еще большие потери аминокислот наблюдаются на стадии нейтрализации, очевидно, в результате дезаминирования аминокислот, реакции меланоидинообразования и т. п. Так, цистина теряется до 40%, тирозина 25%, лизина 5%, гистидина 28%, ас - иарагиновой кислоты 13%, треонина 20%, лейцина и изолейцина 40%- Теряются отдельные аминокислоты и при осветлении гидролизата и отделении гуминов.
Приведенные данные свидетельствуют о том, что гидролиз белков с применением соляной кислоты как катализатора разрушает многие жизненно необходимые аминокислоты.
Чтобы сократить эти потери, надо строго соблюдать режимы проведения гидролиза.
Ферментативный гидролизат содержит также продукты гидролиза углеводов (органические кислоты, спирты и др.) и биологически активные вещества, накапливаемые грибом.
Ферментативный гидролиз проще осуществить — для этого не нужно сложной эмалированной аппаратуры, без которой нельзя обойтись при кислотном гидролизе. Однако при ферментативном гидролизе содержащийся в сырье белок не полностью расщепляется до аминокислот. Часть его остается в отходах. Кислотный гидролиз позволяет почти весь белок, содержащийся в сырье, перевести в аминокислоты, в связи с чем сырье используется более полно.
Недостаток кислотного гидролизата — большое содержание поваренной соли в нем; она образуется в результате нейтрализации соляной кислоты по окончании гидролиза двууглекислым натрием (содой). Обессоливание кислотного гидролизата — проблема, над которой работают многие исследователи.
В последнее время начинают внедрять в практику смешанный способ производства белковых гидролизатов. Вначале сырье подвергают ферментативному расщеплению с помощью ферментов гриба Aspergillus oryzae, а затем оставшуюся массу обрабатывают соляной кислотой с целью использования остаточного белка. Полученные гидролизаты смешивают. При таком способе производства используются преимущества обоих видов гидролиза — ферментативного и кислотного.
Белковые гидролизаты представляют собой светло-коричневую жидкость со специфическими грибными запахом и вкусом. Химический состав белковых гидролизатов (в %) приведен в табл. 19.
Плотность ферментативного гидролизата 1,57—1,60 г/см3, кислотного гидролизата — 1,22 г/см3.
|
Таблица 19
|
Производство белкового ферментативного гидролизата с помощью гриба Aspergillus oryzae
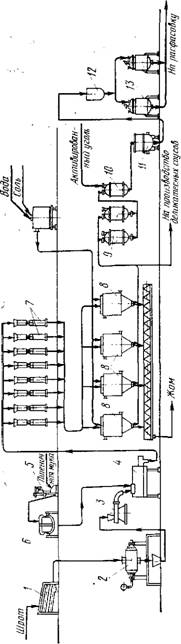
Технологическая схема производства белкового гидролизата методом биохимического гидролиза с помощью гриба Aspergillus oryzae представлена на рис. 29.
Соевый шрот просеивают на вибросите 1 для отделения случайных примесей и пропускают через магниты для улавливания ферропримесей; затем его загружают в стерилизационный аппарат 2, где стерилизуют острым паром при давлении 0,2 МПа в течение 30 мин. Стерилизованную массу охлаждают в том же аппарате, подавая в рубашку его холодную воду. Охлажденную массу гранулируют на волчке 3 и полученные гранулы смешивают в смесительном аппарате 4 со стерильной пшеничной мукой и маточной культурой плесневого гриба.
Взамен соевого шрота могут быть использованы зерна сои. В этом случае исключается процесс гранулирования стерилизованного материала.
Пшеничную муку подвергают просеиванию на вибросите 5 и стерилизуют в автоклаве 6. Охлажденную муку направляют на смешивание с гранулами шрота.
Смесь гранул с мукой и маточной культурой Aspergillus огу-
Zae загружают в аппараты 7 для выращивания гриба, которое длится 48 ч.
Массу, проросшую плесневым грибом, называемую код - жи, обрабатывают в диффузионной батарее 8 раствором поваренной соли.
Полученный гидролизат выдерживают в емкостях 9 в течение 5—6 дней и осветляют активированным углем в аппарате 10. Осветленный гидролизат фильтруют на нутч-фильтре 11, собирают в резервной емкости 12 и направляют на сгущение в вакуум-аппарат 13, а затем расфасовывают.
Технологический процесс производства белкового гидролизата методом биохимического гидролиза можно разделить на две основные фазы: производство коджи и обработка коджи раствором поваренной соли (ферментация). Эти процессы следуют один за другим без перерыва.
Полученный жидкий гидролизат немедленно направляют на сгущение или, если это необходимо, выдерживают в течение 20—30 дней. При такой выдержке наблюдается разрушение полипептидных цепей у остатков белковой молекулы и накопление в жидкости ами- ноазота.
|
|
Длительное хранение коджи до обработки раствором поваренной соли ведет к снижению протеолитической активности ферментов, накопленных плесневым грибом при его росте, а следовательно, к уменьшению выхода гидролизата.
При необходимости гидролизат без выдержки и сгущения может быть использован в производстве, например при изготовлении соусов.