Моделирование миграции подземных вод
Принципы проведения натурных наблюдений
Натурные наблюдения за процессами миграции подземных вод с помощью технических средств осуществляются прежде всего для выяснения качественных особенностей этих процессов, после чего их результаты направляются на идентификацию натурных данных и используемой теоретической модели с определением расчетных параметров процесса. Важным достоинством таких наблюдений является привлечение для идентификации миграционных моделей значительного по представительности исследуемого пространства. Недостаток их заключается в том, что в натурных условиях проявляется комплексность процессов, которая нивелирует воздействие значений отдельных параметров и затрудняет их идентификацию. В принципе при интерпретации измеренных характеристик процесса для определения параметров речь идет о решении эпи - гнозных задач, которое имеет практический Смысл и достижимо лишь с помощью гипотетической теоретической модёли процесса, задаваемой обычно квантифицированно. Подкрепляя модель количественным анализом, можно ограничить временное и пространственные координаты, в которых параметры достаточно чутко реагируют на процесс, чтобы удержать в определенных границах стоимость наблюдений и комплексность модели идентифицированных параметров.
Проведение натурных исследований геомиграционных процессов, как правило, должно иметь характер мониторинга, т. е. составлять целенаправленную систему, включающую научно обос - 376
нованную программу наблюдений за важнейшими динамическими характеристиками процесса; анализ и научно обоснованное объяснение происшедших в ходе процесса (эпигноз) изменений; научно обоснованный прогноз ожидаемых изменений процесса.
Планирование мониторинга — в соответствии с его целенаправленным характером — должно быть тесно связано с решением практических задач и обосновывать управление хозяйственными воздействиями на природные процессы.
В зависимости от решаемых задач в мониторинге геомиграционных процессов выделяются следующие основные направления: 1) обоснование качества ресурсов подземных вод для гарантированного их использования при водоснабжении (прежде всего пресные, а также минеральные и термальные воды); 2) контроль за потенциальными источниками загрязнения с позиций охраны окружающей среды; 3) оценка влияния подземных вод на сельскохозяйственное состояние земель.
Ядром мониторинга являются полевые наблюдения, при постановке которых необходимо прежде всего ответить на вопросы: что, где, когда и как следует наблюдать. Ответы на эти вопросы надо искать с обязательным использованием математических моделей, на которых должен имитироваться ход процесса при различных изменениях его параметров. Прежде всего обычно проводится моделирование геофильтрации, реализуемое на системе плановых и профильных геофильтрационных моделей, с которых для расчетов конвективного переноса снимаются показания о скорости фильтрации. После этого строится миграционная модель, соответствующая принятой теоретической модели геомиграции.
Важной частью такого моделирования является обоснование диапазона возможных изменений различных параметров процесса, которое производится на основе анализа литературных источников и фондового материала, а также имитационного моделирования, показывающего роль различных факторов и параметров в формировании изучаемого геомиграционного процесса.
При задании режима наблюдений (ответ на вопрос — когда?) следует учитывать весьма медленное развитие геомиграционных процессов, поэтому нередко целесообразно проведение единовременной гидрогеохимической (геомиграционной) съемки, повторяемой через определенные промежутки времени.
Существенным является также вопрос о том, кто должен проводить геомиграционные наблюдения — геологические организации, которым такие работы ближе по существу изучаемых процессов, или проектно-эксплуатацио. нные, для которых более важен результат такого "исследования. Здесь приходится учитывать формальные сложности решения этого вопроса, обусловленные, например, особенностями финансирования различных организаций, ведомственными «барьерами» и т. п. При решении этого вопроса надо исходить из особой важности целенаправленного проведения мониторинга, обязательно включающего кроме наблюдений эпигноз и прогноз. По-видимому, проводить мониторинг должна та организация, которая больше заинтересована в его результатах и имеет возможность осуществить его прогнозный и эпигнозный анализ. Существенным является вопрос о стоимости проводимых наблюдений, которая, разумеется, должна перекрываться экономическим выигрышем от использования результатов мониторинга.
В качестве примера мигрантов-индикаторов, используемых при изучении подземных вод, рассмотрим естественные радиоактивные изотопы 3Н, 14С, 39Аг и 85Кг, которые до сих пор использовались в основном для определения возраста подземных вод. Эти изотопы имеют следующие периоды полураспада і\/ч: тритий 12,43 года, аргон 570 лет, углерод 5730 лет, криптон 10,76 года.
При математическом описании процесса радиоактивного распада по уравнению кинетики реакции первого порядка г=—кс получается константа скорости распада (коэффициент скорости) а=1п2 : ^/2=0,693 : Концентрации этих изотопов в воде задаются для 3Н в тритиевых единицах (1ТЕ=0,118 Бк/л воды при изотопном соотношении зН/1Н== ю-18); для в процентах от современного содержания (СС) углерода (1 % СС=2,26 мБк/г углерода), присутствующего в подземных водах в компонентах карбонатной системы — НС03_, СОз2- и Н20-С02; для 39Аг и 85Кг в беккерелях на литр или на моль Аг или Кг.
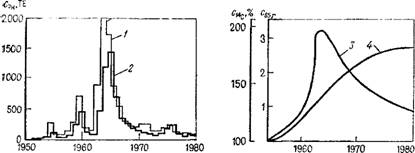
Тритий, образовавшись под действием космического излучения из азота в атмосфере, окисляется до воды и с осадками в виде 'Н3НО поступает на земную поверхность. Процесс переноса трития осуществляется так быстро, что в тропосфере происходит лишь незначительное выравнивание концентраций, поэтому концентрация 3Н в осадках подвержена резким колебаниям. Сезонные изменения концентрации обусловлены особенностями воздухообмена между стратосферой и атмосферой. Для изучения формирования грунтовых вод особенно важное значение имеют зимние поступления. На континентах концентрация 3Н в осадках растет с увеличением расстояния от побережий (континентальный эффект) вследствие фракционирования изотопов. Среднее годовое поступление 3Н до 1953 г. составляло 6ТЕ, а в зимние месяцы 4ТЕ. Вследствие проведения ядерных испытаний в атмосфере к середине 60-х годов эта концентрация возросла до 2000 ТЕ, а в настоящее время снова снизилась и составляет 10—30 ТЕ. На рис. 45 приведен типичный график изменений концентраций 3Н в осадках по данным наблюдательных станций в Вене и Мюнхене, который может использоваться для приближенной оценки формирования грунтовых вод за счет поступления осадков в Центральной Европе. В мировом масштабе по данным сети наблюдений Международное агенство по атомной энергии (IAEA) и Всемирная организация по метеорологии (WMO) представляют точные месячные данные поступления 3Н с осадками. Для периода до 1954 г, начальную концентрацию 3Н, в подземных условиях можно считать примерно равной нулю.
Концентрация 85Кг в атмосфере в настоящее время Обусловлена развитием различной ядерной техники и технологии. В отличие
|
Рис. 45. Поступление естественных радиоактивных изотопов трития 3Н (1 — годовое, 2 — в течение зимы), углерода 14С (5) и криптона 85Кг (4) |
•от 3Н концентрация 85Кг практически не подвержена сезонным колебаниям и влиянию континентального эффекта. Посредством ■функции сглаживания t ехр (ajt-\-b) (где а, b — параметры уравнения) можно достаточно точно отобразить измеренные Значения между 40° и 60° с. ш. На рис. 45, б показана функция поступления 85Кг по данным 450 замеров между 40° и 60° с. ш. с доверительной областью, соответствующей стандартному отклонению, умноженному на t — фактор распределения Стьюдента, с уровнем значимости $9%. Аналогичные данные по Северному и Южному полушариям представлены в работе [69]. Функция поступления отчетливо показывает, что до 1956 г. начальная концентрация 85Кг может считаться примерно равной Ю-7 уровня в настоящее время, т. е. ее можно приравнять к нулю.
Растворенные в осадках и газообразные атомы редких газов в атмосфере находятся в термодинамическом равновесии по отношению друг к другу (это касается также неглубоких поверхностных водоемов). В атмосферном воздухе доля вещества Кг составляет 1,1 • 10-6= 1,1 млн-1. При 10 °С и атмосферном давлении в 1 м3 воды растворяется 80 мкл Кг. Поэтому часто используют следующий аппроксимированный пересчет: 1 Бк/мл Кг атмосферы— ==0,080 Бк/м3 воды.
Космогенная концентрация 39Аг в атмосферном воздухе практически не подвергается антропогенному влиянию. Антропогенная составляющая оценивается менее чем в 7 % естественной концентрации, что позволяет применять постоянную функцию поступления 39Аг в 1,9 мБк/л Аг атмосферы или 0,5 мБк/м3 воды, находящейся в контакте с атмосферой. Вследствие этого, распределение начальных концентраций получается из стационарного решения модели миграционного процесса (ММП).
По аналогии с 3Н в верхних слоях атмосферы под воздействием космических лучей из азота образуется также 14С, который окисляется до ИС02. До испытаний ядерного оружия концентрация НС была примерно равна современной (0,226 Бк/г), к середине 60-х годов она почти удвоилась, а сейчас составляет примерно 1,3 естественной концентрации.
Так как ИС обычно используется для определения абсолютного возраста в интервале от 1000 до 10 000 лет, то особый интерес представляет постоянная функция поступления углерода (0,226 Бк/г) атмосферного происхождения до начала ядерных испытаний. В областях с гумидным климатом 14С первично вносятся в подземные воды в основном растениями (содержание С02 в почвенном воздухе часто более 1 %) и только во вторую очередь осадками (содержание СОг в атмосферном воздухе 0,03%). В подземных условиях растворяется свободный от 14С автохтонный карбонат. В настоящее время концентрация 14С в инфильтрующихся осадках считается равной 85±5 % от современной и от 120 до 80 % от современной для зоны аэрации. В качестве входной функции для инфильтрата, поступающего в грунтовые воды, до 1954 г. рекомендуется концентрация в 65 % от современной.
В тех случаях, когда известны количество и время ввода загрязнителя, можно получить сопоставимые функции поступления для целого ряда специфических атмосферных загрязнителей, в том числе кислых газообразных выбросов, агрохимикатов (гербицидов, инсектицидов, фунгицидов) и т. п. В ряде случаев поверхностные воды, питающие грунтовые, несут очень характерные загрязнители, которые также могут применяться в качестве мигрантов-индикаторов.
При построении теоретической модели динамики распространения рассматриваемых мигрантов-индикаторов обычно используют предпосылку о равновесном характере обменных процессов,, имея в виду, что мигранты 3Н, 39Аг и 85Кг консервативны, не реагируют с другими веществами и биохимически не разлагаются. Следовательно, миграционная модель отражает уравнение баланса вещества:
[TR]=[S] + [R] + [QU], (3.1)
Где [TR] и [5]— члены, выражающие перенос (транспорт) и накопление мигранта, а соединение рассматриваемого мигранта с другими выражается через члены реакций [/?] и источников-сто - ков [QM].
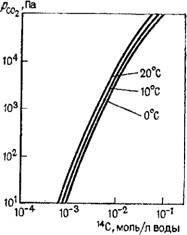
Для такого мигранта как 14С модель имеет более сложный вид, поскольку углерод входит в состав многих растворенных в воде компонентов. В качестве примера на рис. 46 для этой системы показана суммарная концентрация растворенного неорганического углерода в зависимости от парциального давления С02 на границе газовой фазы. В общем случае необходимо использовать и другие комплексные термодинамические модели равновесий. В отдельных случаях, когда надо прийти к обозримым моделям миграционных процессов, проводят радикальную аппроксимацию. Эта задача при использовании 14С в качестве мигранта имеет большое значение (см. [69]). 180
Заметим, что известные примеры использования натурных наблюдений для обоснования параметров теоретической модели миграции обычно базируются на мало представительных материалах и чаще всего направляются на определение параметров макродисперсии без попыток диагностической проверки материалов наблюдений [14].
Анализ проб
Подземных вод
Полевой анализ. Измерение температуры или концентрации рассматриваемых мигрантов в подземных водах непосредственно после произведенной сепарации представляет собой весьма существенную задачу. Последующих искажений результатов анализа в значительной мере можно избежать, если измерение производилось после раздела фаз по возможности быстро и с небольшими нарушениями соотношений температуры, парциального давления и освещения в сравнении с природной обстановкой. Решить эту задачу можно, применяя скважинные зонды.
Измерительная головка современного скважинного зонда оснащена различными сенсорными элементами. Необходимая турбулентность. воды перед «измерительным окном» достигается с помощью вертушки. Измерительная головка зонда спускается в скважину на кабеле, который связывает ее с полевым измерительным прибором на поверхности. Этот прибор фиксирует, а при необходимости накапливает и обрабатывает замеры с помощью микропроцессора.
|
Рис. 46. Графики зависимости концентрации углерода 14С от парциального давления С02 и температуры в системе С02— СаСОз—Н20 |
Такими зондами измеряются, например, концентрация 02, величина рН, электропроводность и температура; электроды для замера рН можно заменить на Red-ox электроды. Уже сегодня есть достаточно миниатюрные варианты таких зондов [42]. Работа ионселективных электродов при определении, например, Na+, К+, Са2+, Cd2+, Cu+, Cl~, N03~ и других ионов может сопровождаться; сильными помехами, что приводит к существенным погрешностям в результатах измерения. вследствие «сверхчувствительности» электродов к влиянию мешающих ионов. Поэтому иономер-микро - процессор пока широко используется только в лабораторной практике [42]. Если проба воды извлечена из пласта и тут же на поверхности земли отфильтрована, то рекомендуется немедленна провести анализ ее состава. Для этого прежде всего используются: проточные измерительные ячейки с ионселективными электродами».
А также фотометрические кюветы и другие быстродействующие анализаторы.
Проточные измерительные ячейки направляют анализируемый поток (например, через небольшую форсунку) прямо на мембрану ионнселективного электрода, задавая тем самым желаемую турбулентность. (В проточной ячейке часто располагается несколько электродов и поток направляется по очереди на каждый; испытаны также ячейки со сменными электродами.) Проточная измерительная ячейка служит для контроля за краткосрочными изменениями показателей состава воды и немедленного выборочного их анализа. Такая форма контроля используется также для определения времени начала отбора пробы на лабораторный анализ, исходя из достижения постоянства качества по избранному критерию. Обычно контролируются температура, проводимость, содержание растворенного кислорода 02 и (или) рН, а также Red-ox потенциал и мутность.
Использование проточных ячеек гарантирует минимальные затраты времени на отбор представительных проб и тем самым резко повышает надежность и эффективность самого отбора. Значения, измеренные при отборе пробы, дают возможность оценить представительность последующего лабораторного анализа. Примеры описаний проточных ячеек приведены в работе [54].
Кроме того, на месте отбора следует определять свободную углекислоту и проводить органолептические испытания (цвета, запаха и вкуса отобранной воды). Органолептическая оценка часто весьма ценна для последующего лабораторного анализа.
Для немедленного определения большого числа показателей состава на месте обычно применяют полевые анализаторы, например оснащенный микропроцессором полевой фотометр с кюветами [62]. Такие приборы позволяют проводить быстрый анализ на выявление NH4+, РО43-, NO3-, N02~, Cr3+, CN-, Ni2+, Cu2+, S042", Fe2+ и Cd2+. С помощью универсального индикатора утечки газа (газоанализатора) эффективно обнаруживаются многие мигранты в почвенном воздухе, содержание которых измеряется в частях на миллион (например, аммиак, этилен, углеводороды бензинового ряда, бензол, хлор, диоксид углерода, фенол, фосген, кислород, ©ксид серы (IV), сероводород, вода и др.).
В полевых условиях также рекомендуется применять газовые хроматографы, которые позволяют эффективно определять, например, галоидсодержащие углеводороды в зоне аэрации и подземной воде. При всех этих способах полевых испытаний достигаемая аналитическая точность часто не так важна, как сама возможность быстро, на месте получить результаты измерений, что дает возможность принять немедленное решение о дальнейшем ходе опробования.
Консервация. На месте отбора проб воды, предназначенных для лабораторного анализа, осуществляется их первичная обработка или консервация. Цель такой консервации — по возможности замедлить химические и биологические обменные реакции с участием 182
|
Таблица 15 Способы консервации и возможности их применения
|
Анализируемых компонентов, а также уменьшить их летучесть. Полная консервация проб вряд ли возможна, но часто можно достаточно эффективно замедлить процессы изменения их свойств.
Для консервации проб прежде всего используют регулирование величины рН, превращение вещества путем добавки химикатов, а также охлаждение и замораживание. В табл. 15 приведены некоторые вещества, применяемые при консервации, специфика их действия и возможностей для применения.
Для определения некоторых компонентов (например, фосфатов) иногда требуется на месте отфильтровать пробу воды через тонкопористый фильтр (0,45 м«м). Все приемы обработки проб на месте, отбираемое количество проб и условия их транспортировки должны быть согласованы с аналитиком в лаборатории, так как они зависят от методов анализа. Тем не менее можно дать некоторые общие рекомендации [75].
Из катионов только щелочные Na+ и К+ не нуждаются в консервации. Пробы для анализа тяжелых металлов Fe2+, Мп2+, щелочноземельных ионов Са2+, Mg2+ и ЫН4+ должны консервироваться кислотой до значений рН 1,5. Среди анионов в консервации не нуждаются только хлориды. Нитритам и нитратам она необходима, если нет гарантии, что проба может быть проанализирована в день отбора. Прежде всего в мягких водах изменяется концентрация НС03". Для отбора фосфатов рекомендуются стеклянные емкости и консервация с помощью NaOH до рН более 12. В полиэтиленовых емкостях наблюдалась потеря фосфатов. Напротив, фториды могут сохраняться не только в стеклянных бутылках.
Очень тщательной обработки требуют воды с низким окислительно-восстановительным потенциалом (например, так называемые «серные» воды). Щелочность проб из глинистых и вулканических пород при рН 8,2 необходимо определять на месте, так как эти породы легко поглощают С02.
Растворенные газы необходимо определять на месте или тщательно консервировать пробы. Определение растворенного кислорода осуществляется по методу Винклера или с помощью кислородного электрода. Содержание свободной углекислоты также необходимо устанавливать тотчас на месте.
Важнейшими анализируемыми группами органических веществ являются углеводороды (утечки минерального масла, в особенности, бензина, дизельного топлива, мазута и т. д.), фенолы (консервация является спорной, рекомендуется применение NaOH, еще лучше замораживание или быстрый анализ), хлорсодержащие углеводороды (растворители, чаще летучие), полициклические ароматические углеводороды (ПАУ), агрохимикаты, детергенты. Каждая такая группа часто нуждается в специальной консервации. Многие органические водорастворимые вещества чувствительны к бактериальному обмену, кислороду и свету, кроме того, некоторые из них летучи вследствие высокого давления их паров. Поэтому основная рекомендация при отборе проб — использовать посуду темного стекла, возможно быстрый анализ и охлаждение.
Важнейшими анализируемыми изотопами в подземных водах являются 180, 2Н, 3Н, 13С, 14С, 15N, 39Аг и 85Кг. Стабильные изотопы 180 и 2Н, а также нестабильный 3Н не нуждаются в консервации, и их анализ не требует большой пробы (от 50 до 100 см3). Для анализа 13С и 14С, а также 39Аг и 85Кг, напротив, необходимы большие объемы пробы (200—1000 л). Для определения 15N, 39Аг и 85Кг консервация не требуется.
Для микробиологических исследований необходимо наряду с дезинфекцией или стерилизацией перед отбором и при отборе проб использовать специальные приемы консервации [75].
Лабораторный анализ. При химическом анализе проб подземных вод обычно речь идет о выявлении следов веществ, что предъявляет особые требования к аналитической работе. Хотя в подземных водах водорастворенные вещества присутствуют в иных концентрациях, чем в поверхностных или сточных, для определения большинства критериев используются одни и те же аналитические методики [64]. Из большого числа методов анализов, по которым возможно определение веществ в воде, развиты стандартные методы, описанные, например, в [41]. В то же время следует отметить, что в каждом конкретном случае необходимо учитывать особенности состава пробы воды и их влияние на анализ каждого из компонентов.
Наряду с классическими методами объемного анализа (титри - метрией и калориметрией), которые достаточно широко используются в анализе подземных вод, все возрастающее значение получают инструментальные (фотометрия, потенциометрия, кондук - 184 тометрия, амперометрия, атомная спектроскопия) и другие методы, с помощью которых возможен анализ неорганических веществ в воде.
Для установления органических веществ используются методы суммарного определения (например, общего органического углерода) и методы определения отдельных групп органических веществ или соединений, например, с помощью хроматографических методов анализа.
Фотометрия принадлежит к методам, наиболее часто используемым при анализе воды, так как с ее помощью по величине поглощения монохроматического света, проходящего через окрашенные пробы раствора, можно быстро и с большой точностью определить такие параметры качества воды, как содержание хлоридов, алюминия, Железа, марганца, фосфатов, нитратов и сульфидов. Интенсивность окраски, характерная для каждого вещества и вызываемая специфической реакцией, служит при этом измеряемой величиной. По роду генератора монохроматического света (монохроматора) различают фотометры и спектрофотометры. Для достижения высокой точности измерения важно правильно установить длину волны и выбрать фильтр. Предполагается, что исследуемые пробы воды оптически прозрачны, так как малейшие помутнения способствуют увеличению интенсивности окраски. Необходимо принимать во внимание и собственную окраску исследуемой воды.
Применение инструментальных методов требует специальной методической подготовки и прежде всего знания принципа измерения и управления аналитическим прибором [62].
Потенциометрия является широко распространенным электрохимическим методом анализа воды, основанным на изменении потенциала химической системы, входящей в состав измерительной цепи. Для того чтобы установить функциональную зависимость между измеряемым потенциалом и химическим критерием,, используется измерительный (индикаторный) электрод с возможно более высокой селективностью измерения. До сих пор лучше всего удается определение активности иона водорода, поэтому измерение рН является главной областью использования потенцио - метрии. Для этой цели используется измерительная цепь стеклянного электрода, в которую кроме стеклянного электрода измерения входит электрод сравнения (каломельный или хлорсеребря- ный) с постоянным потенциалом. Широкое распространение получили прямые потенциометрические определения активности многих ионов с помощью ионселективных электродов, например, кальция, хлора, брома, иода, фтора, нитрата и серы. Однако применение этих электродов в сравнении со стеклянным имеет немало проблем, так как все они более или менее подвержены мешающим влияниям.
Кондуктометрия (измерение электропроводности) является методом суммарного определения, и возможности его применения зависят от концентрации, степени диссоциации электролита, электрохимической валентности и скорости переноса ионов, а также от температуры анализируемого раствора. Данных относительно вида электролитов с помощью этого метода не получают, однако электролитическая электропроводность дает информацию о суммарной концентрации растворенных в воде диссоциированных веществ, которая в большинстве случаев идентична солесодержанию.
Амперометрия как метод анализа также основана на электродных реакциях и применяется в основном для измерения содержания в воде растворенного кислорода с помощью так называемых электродов с мембранным покрытием. Поскольку растворимость кислорода в воде и его диффузия через мембрану зависят от температуры, современные кислородные измерительные приборы снабжены устройством автоматической температурной компенсации.
Среди атомно-спектроскопических методов, которые нашли применение в анализе подземных вод, можно назвать атомно-абсорбционную спектроскопию (ААС) и атомно-эмиссион - ную спектроскопию (АЭС). Методы ААС наиболее пригодны для определения элементов-металлов. С большим успехом для анализа следов металлов используется непламенная ААС, которая, благодаря высокой чувствительности, позволяет непосредственно определять металлы в области концентраций от нескольких миллиграммов на литр. Современные приборы ААС и АЭС оснащены компьютером, который частично осуществляет управление ходом анализа. Рационализация в области аналитических методов измерения в последние годы связана с введением так называемых мультиэле - ментных методов. Была предложена атомно-эмиссионная спектроскопия, которая отличается от ААС скоростью проведения анализа,—после оптимизации и калибровки нужно только около 20 с для одновременного определения этим методом 25 элементов [68].
Главная проблема химического анализа содержания органических веществ в подземных водах связана с многообразием органических соединений. Для определения групп органических веществ и отдельных соединений привлекаются хрома тографи - ческие методы, которые дают возможность проводить разделение смеси веществ, но не их идентификацию. Тонкослойная хроматография пригодна для использования в каждой лаборатории и особенно для исследования таких важных групп веществ, как хлорсодержащие (например, инсектициды) и полициклические ароматические углеводороды. Из традиционной тонкослойной хроматографии развилась современная высокопроизводительная тонкослойная хроматография, которая характеризуется новой системой пластин, техникой нанесения проб, методами развития и прямой фотометрической оценкой хроматографических пластин. Газо - хроматографические методы позволяют разделять смеси веществ, находящихся в газообразном состоянии. Хроматографические определения возможны, если подобрано соответствующее стандартное вещество, что при исследованиях воды не всегда может быть гарантировано. Поэтому такое разделение должно быть подкреплено другими методами, например, ИК-спектроскопиёй, масс - 186 спектрометрией. Вследствие значительных затрат на материалы и аппараты приобретение современной системы приборов газовая хроматография — масс-спектрометрия (ГХ—МС) может быть оправдано лишь для центральных лабораторий со специальными задачами.
Аналитические исследования воды следует стремиться ставить с учетом многих критериев с необходимыми компромиссами, в которых решающее слово принадлежит аналитикам.