Получение циркония электролизом
Цирконий может быть получен электролизом галогенидов циркония в солевом расплаве.
Лучшие результаты получены с электролитами, содержащими K2ZrF6 в расплаве NaCl или КС1. Электролиз проводят в ваннах состава: 20% K2ZrF6 +80% NaCl или 25-30% K2ZrF6 + 70+75% КС1. Второй электролит имеет преимущества: напряжение разложения КС1 выше, чем NaCl, анодный эффект наступает при более высоких плотностях тока, температура плавления ниже, чем электролита с NaCl, что позволяет проводить электролиз при 750-800 С.
Приближенно процессы на катоде можно представить со
стоящими из диссоциации анионов ZrFІ" (в прикатодном
Пространстве) и последующего ступенчатого разряда катионов Zr4+:
2- 4+ _
Zr + 6 F ; — Zr2+ + 2 e
ZrF6 ч= Zr3+ + е
(4.43)
Zr°.
Zr4+ + е
На аноде разряжаются ионы Cl~, электродный потенциал коїорьіх в солевом расплаве (+3,39 В) ниже, чем анионов F~(+3,51 В)! Соответственно этому основная реакция на аноде:
4 F + 4 КС1 (4 NaCl) - 4 е = 4 KF (4 NaF) + 2 Cl2*. (4.44)
Однако по мере накопления в ванне фторидов на аноде происходит разряд ионов F~. Выделяющийся фтор взаимодействует с графитовым анодом, образуя CF4.
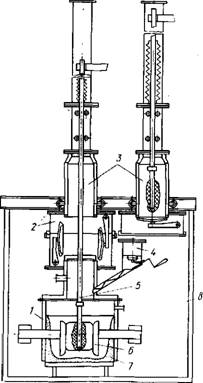
Ржс.57. Герметичный электролизер для получения циркония: 1 - стальная водоохлаждаемая ванна с гарниссажной зашитой стенок; 2 - разъемный шлюз; 3 - охладительная камера; 4 - бункер; 5 - катод; б - графитовые аноды; 7 - гарниссаж; 8 - камера, заполненная аргоном
Накопление фторидов происходит медленно, так как значительное количество фторида увлекается из ванны с катодным осадком. Процесс ведут при катодной плотности тока 350-450 А/дм2. Катодный осадок содержит около 30% порошка циркония с размерами частиц 50-200 мкм. В процессе электролиза наблюдается существенная очистка циркония от гафния, так как потенциал выделения гафния ниже, чем циркония.
. На рис. 57 показана схема герметичного электролизера отечественной конструкции для получения циркония. Ванна - из нержавеющей стали с водяной рубашкой. На внутренних стенках образуется гарниссаж застывшего электролита, предохраняющий от загрязнения электролита железом.
В ванну введены четыре графитовых электрода: два анода и два электрода переменного тока для разогрева и расплавления электролита.- Катод - стальной.
После отложения заданного количества металла катод с осадком извлекают через шлюз в охладительную камеру, заполненную аргоном, которую отсоединяют и к шлюзу присоединяют камеру с новым катодом, который после заполнения камеры аргоном опускают в электролит.
После охлаждения в аргоне катодный осадок сбивают с катода, дробят и обрабатывают водой, 10 %-ной НС1, промывают водой, спиртом и сушат в вакууме при 50-60 °С. Чистота порошков характеризуется следующим примерным составом, %: N 0,003; С 0,05; О 0,06; Fe 0,013; Ni 0,07; Ті 0,002; Mn, CI < 0,002; CO < 0,05; Mg < 0,01; Si < 0,05.
После переплавки в дуговой печи с расходуемым электродом слиток циркония имеет твердость НВ 1300-1400 МПа.
При условии разработки конструкций больших электролизеров, в которых можно осуществить непрерывный или полунепрерывный процесс, электролитический способ получения циркония может конкурировать с магниетермическим способом восстановления из хлоридов.