ИЗВЛЕЧЕНИЕ СЕЛЕНА И ТЕЛЛУРА ИЗ ШЛАМОВ СЕРНОКИСЛОТНОГО И ЦЕЛЛЮЛОЗНО — БУМАЖНОГО ПРОИЗВОДСТВА
Этот вид сырья характеризуется большим разнообразием химического и фазового состава. Шламы содержат оксиды и сульфаты тяжелых цветных металлов, железа, алюминия, элементарные селен и теллур, оксид и сульфид мышьяка и др. В сернокислотных шламах свинцово-цинковых предприятий находят селениды цинка, ртути, свинца.
Шламы с повышенным содержанием мышьяка (десятки процентов) предварительно выщелачивают водой, 10-20 %-ными растворами соды, щелочи или 5-7 %-ным раствором соляной кислоты. Шламы с небольшим содержанием мышьяка сразу подвергают окислительному обжигу или спеканию с содой. Бедные по содержанию селена и теллура шламы обогащают флотацией. Из концентрата с 0,5-1,0 % Se можно получить концентрат с 15-20% Se с извлечением до 90%.
Шламы со значительным содержанием селена, теллура и их соединений перерабатывают сульфидным способом.
Окислительный обжиг основан на окислении селена и теллура до диоксидов. В системе мокрого пылеулавливания часть селена переходит в раствор в составе HjSOj, часть - в осадок (элементарный селен). Осадок возвращают на обжиг. Из растворов селен осаждают бисульфитом натрия в солянокислой среде:
H2Se03 + 2NaHS03 = Se + Na2S04 + H2S04 + H20. (6.29)
Из огарка трехкратным выщелачиванием растворами соляной кислоты (100-120 г/л) извлекают теллур, который затем восстанавливают при 80-85 °С сернистым газом (рис.65).
Сернокислотный шлам
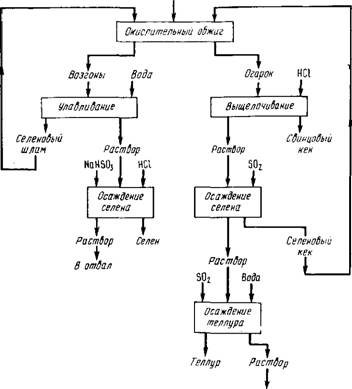
В отбал
Рас. б5. Технологическая схема извлечения селена и теллура из сернокислотных шламов
Сульфидный способ основан на образовании растворимых полисульфоселенида H2SSe„, полисульфотеллурида Na2STe„, тиосолей типа Na2TeS3 при взаимодействии компонентов шлама с сернистым натрием в щелочной среде:
NSe + Na2S = Na2SSe„; (6.30)
S + Na2S = Na2S2; (6.31)
2Na2S2 + nSe = Na2SSe„ + Na2S3; (6.32)
Na2S3 + Те = Na2TeS3; (6.33)
249
Na2S + лТе = Na2STe„; (6.34)
HgSe + Na2S = HgSe • Na2S. (6.35)
В щелочном растворе сначала восстанавливают ртуть гранулированным алюминием:
3(HgSe • Na2S) + 8NaOH + 2АІ = 3Hg + 3Na2S + 3Na2Se +
+ 2Na[Al(OH)J. (6.36)
Затем из раствора осаждают селен, окисляя кислородом воздуха:
2Na2Se + 02 + 2Н20 = 2Se + 4NaOH; (6.37)
2Na2SSe„ + 202 + 2Н20 = 2nSe + Na2S2Os + 2NaOH. (6.38)
Теллур при этом остается в растворе в составе Na2TeS3. Его осаждают, восстанавливая сульфитом натрия:
Na2TeS3 + 2Na2S03 = Те + 2Na2S203 + Na2S. (6.39)
Черновые селен, теллур, ртуть рафинируют. Извлечение селена и теллура из вторичного сырья
Вторичное сырье - это отходы и брак селеновых выпрямителей, отработанные селеновые элементы, теллуровые полупроводниковые приборы и др. В отходах селен и теллур находятся в основном в элементарной форме и в составе халь - когенидов металлов. Поэтому для их растворения применяют концентрированные растворы HN03, Na2S, Na2S03, расплавы NaOH. Селен можно также выплавлять или возгонять в вакууме, осаждать электролизом из селенидного щелочного раствора.
По одной из технологических схем селен извлекают из вторичного сырья обработкой его расплавленной щелочью по реакции:
3Se + 6NaOH = 2Na2Se + Na2Se03 + 3H20. (6.40)
При содержании в отходах селенидов к расплаву добавляют окислитель NaN03. Селен выщелачивают из щелочного плава слабым раствором НСІ, затем осаждают сернистым газом, дистиллируют в вакууме, получая чистый селен. Технологическая схема извлечения селена из отходов представлена на рис.65. 250
Другой способ предусмаривает выщелачивание селена из отходов слабощелочными растворами при 60-65 С с последующим выделением его аэрацией раствора. При извлечении селена до 95 % способ обеспечивает получение 99,5 %-ного продукта.
5. РАФИНИРОВАНИЕ СЕЛЕНА И ТЕЛЛУРА
Технические селен и теллур содержат 2,5-4 % примесей других элементов - Hg, S, As, Си, Ni, Bi, Pb, Те, Si, Na и др. В СССР выпускают селен трех марок по ГОСТ 10298-69-СТ0 (99,4 %), СТ1(99,0 %), СТ2(97,5 %); теллур шести марок - по ГОСТ 18428-73-TB3(99,996 %); ТА1(99,96 %); по ГОСТ 17б14-72-Т00(99,9 %), Т0(99,8 %), Т1(99,0 %),Т2(96 %).
Для рафинирования технических селена и теллура используют физические и химические способы: сульфитный способ очистки селена, плавка селена с аммонийной селитрой, селенидный и теллуридный способы, дистилляция селена и теллура. Для получения полупроводниковых селена и теллура применяют кристаллофизические методы и ряд других.
Сульфитный способ основан на растворении элементарного селена в горячем растворе сульфита натрия с последующей кристаллизацией его из раствора при охлаждении.
Процессы протекают по схеме:
>90 °С,
Se + Na2S03 < Na2SeS03. (6.41)
20 °С
Растворимость селена возрастает с повышением температуры и концентрации сульфита натрия, она максимальна в насыщенном растворе Na2S03. Так, при 97,5 °С раствор содержит 322 г/л Na2S03 и 128 г/л Se, при 20 °С - 250 г/л Na2S03, 49 г/л Se. Следовательно, при охлаждении раствора от 97,5 до 20 С может быть выделено 60% селена. Осадок селена промывают, сушат и при необходимости направляют на глубокую очистку. Маточный раствор используют при растворении следующей партии селена. Получаемый селен по возможности очищают от меди и железа (остаются в нерастворимом остатке), теллура, серы и других. Суммарное содержание примесей в селене не превышает 0,02-0,05 %.
Селенидный и теллуридный способы. Технологические приемы получения элементарных селена и теллура, повторенные многократно, ведут к очитке от многих примесей. В частности, технический селен и теллур переводят в раствор, затем восстанавливают порошком алюминия в щелочной среде. Примеси тяжелых металлов осаждают сульфидом натрия, после чего аэрацией раствора выделяют селен и теллур. Чистота продуктов достигает 99,9 %.
Плавка селена с аммонийной селитрой. Способ основан на окислении и переводе в шлак примесей при плавке селена с NH4N03. Так, примесь теллура окисляется по реакции:
Те + 2NH4N03 = Те02 + 2N2 + 4Н20. (6.42)
Процесс проводят при 210-230 °С (ґпл NH4N03 169,6 °С, Se 221 °С). Разложение селитры и окисление примесей начинается при 190 °С. Шлака получается 2-5 % от массы селена, содержание селена в шлаке 0,6-1,1 %. Извлечение селена в готовый продукт составляте до 99%. Плавку шихты проводят в аппарате из нержавеющей стали с наружным электрообогревом до прекращения выделения газов. Рафинированный селен сливают в изложницы из нержавеющей стали. По этому способу получают селен чистотой 97,5-99,4%.
Дистилляция селена и теллура основана на различии в давлении паров элементарных селена, теллура и примесей. В процессе дистилляции основная масса примесей остается в нелетучем остатке.
Селен дистиллируют при 650-680 С (при атмосферном давлении) или при 310-420 °С [при разрежении 27-800 Па (0,2-6 мм рт. ст.)]. Пары конденсируют при 250-100 С. Жидкий селен из конденсатора разливают в изложницы.
Телл)у дистиллируют в вакууме ~ 1 Па (Ю-2 мм рт. ст.) при 500 С. Примеси с меньшим, чем у теллура, давлением паров (Sb, Pb, Al, Ві, Те, Ag, Cu, Si, Au) остаются в остатке, примеси, давление пара которых выше или равно давлению пара теллура (Se, Na, К, Mg), переходят в дистиллят и конденсируют в различных температурных зонах. В интервале 320-425 °С конденсируется 75 % теллура, при 215-320 С - 22 %. Остаток составляет 3-5 % от количества взятого теллура.
Способ дистилляции с предварительной химической очисткой обеспечивает получение теллура чистотой 99,99 %.
Техника безопасности при работе с селеном и теллуром
Соединения селена и теллура ядовиты. По нормам, действующим в СССР, предельная допустимая концентрация селена и теллура в воздухе 0,01 мг/м3. Попадание соединений селена и теллура в организм человеку через дыхательные пути, желудок и кожу обнаруживается по специфическому "чесночному" запаху выдыхаемого воздуха. Гидриды (H2Se, Н2Те) вызывают сильное раздражение слизистых оболочек дыхательных путей и глаз. Галогениды, диоксиды и другие соединения при попадании на кожу вызывают экзему и болезненные ожоги. В связи с этим технологические процессы должны быть механизированы, а аппараты - герметизированы и снабжены вытяжной вентиляцией.