ОБРАЗОВАНИЕ ЖИВИЦЫ И ТЕОРИЯ СМОЛОВЫДЕЛЕНИЯ
Вопросы образования живицы и теория смоловыделения в настоящее время интенсивно изучаются. Это необходимо потому, что знание теории поможет нам лучше решить практиче^ ские вопросы ведения подсочного хозяйства, найти пути воздействия на биосинтез живицы, а следовательно, пути увеличения валового сбора живицы.
В 1909 г. X. Эйлер [124] выдвинул гипотезу образования по - лиизопреновых веществ. Согласно этой гипотезе, ацетон и уксусный альдегид, получающиеся из углеводов, конденсируются, давая р-метилкротоновый альдегид. Последующая конденсация двух молекул этого альдегида, по мнению X. Эйлера, приводит к гераниолу, а нескольких молекул — к политерпену.
В 1923 г. О. Аскан [43] высказал взгляды, сходные со взглядами X. Эйлера. По мнению О. Аскана, терпеновые углеводороды образуются из ацетона и уксусного альдегида через изопрен.
Гипотеза О. Аскана получила некоторое подтверждение в работе А. Е. Фаворского и А. И. Лебедевой [43], которые из ацетона и ацетилена синтезировали изопрен, линалоол, гераниол и терпингидрат.
По гипотезе О. Аскана, почти каждый терпен теоретически может быть представлен как сочетание нескольких молекул изопрена. На этом основании Л. Ружичка [43, 125] ввел понятие изопренового правила и дал классификацию терпенов, приведенную в несколько измененном виде в табл. 3 [152].
Открытие кофермента ацетилирования (Н—S—КоА), произведенное почти одновременно в различных лабораториях: Лип - манном (1945 г.), Нахманзоном и Берманом (1946 г.), Фельд - бергом и Манном (1946 г.) позволило достигнуть значительных успехов в теории образования жирных кислот и полиизопреновых соединений [32].
Было доказано, что именно ацетат является исходным веществом, необходимым для синтеза вышеуказанных соединений.
Кофермент А необходим для связывания ацетильных групп и их последующей передачи. Свое название кофермент А получил благодаря участию в каталитической функции активации ацетата (І). Кофермент А (II) найден в бактериях, дрожжах, животных тканях и высших растениях и выделен в очищенном виде
Кроме того, в активировании уксусной кислоты при образовании комплекса ацетил — КоА (III) участвует аденозинтрифос - фат (АТФ). Процесс активирования уксусной кислоты может быть изображен следующим образом:
CH3C00H - f HSKoA - f АТФ Фермент, активирующий ацетат і п
----- > CHgCO - SKoA + АМФ + ФФ,
Ні
Где АМФ — аденозинмонофосфат, а ФФ — пирофосфат.
Т аб л и U а 3
Примеры соединение
Изопрен
Пинен, Карен, терпинен и т. д. Составные части эфирных масел
Фарнезол, кадинен, кариофиллен. Составные части эфирных масел
Смоляные кислоты канифоли, копалов и т. д. В гидрированной форме в качестве фитола, в дегидрированной форме в качестве витамина А
Продолжение
|
Брутто - формула |
|
Классы терпенов |
|
Углеродная структурз |
|
Примеры соединений |
|
Ъ |
|
Ч |
|
Трнторпены |
|
СЯ„Н |
|
'30п48 |
|
Ч/1 X / Х Ч/1 |
|
Ч |
|
Тетратерпены |
|
С4ПН |
|
10" 84 |
Сквален, ланостерин, амирин. В уменьшенной молекуле в стеро - идах и алкалоидах
Существуют только в дегидрированной форме, например в каротино - идах
|
|
|
П >100000 |
|
I (С5Н8)„ |
|
Полипрены |
Натуральный каучук (цис-форма)
Гуттаперча и Балата (транс-форма)
Образовавшийся указанным путем ацетилкофермент А (СН3СО~5КоА) содержит богатую энергией макроэргическую тиоэфирную связь, при гидролизе которой освобождается 8200 калорий.
Ацетилкофермент А может затем передавать активированный ацетильный остаток различным соединениям. Так, в опытах с меченым радиоактивным углеродным атомом С14 ацетатом [75] было показано, что у бактерии Closidium acetobutylicum масляная кислота образуется путем конденсации двух молекул уксусной. кислоты в ацетоуксусную кислоту (IV) по схеме:
2СН3СО ~ SKoA СН3СО — СН, СО ~ SKoA + НКоА їм п
Ацетокофермеит А Ацсто-ацетнлкофсрмснт А - Кофермент А
CHgCO —CHsCO~SKoA+ Н20 ^ СН3СО—СН2СООН + HSKoA
IV її
Ацсто-ацетнлкофсрмснт А Ацстоуксусная кислота
Ацетоуксусная кислота (IV) восстанавливается до масляной,; которая снова вступает в реакцию с ацетилкоферментом А, образуя капроновую кислоту.
Таким образом, путем последовательного присоединения аце-| тильных радикалов происходит биосинтез жирных кислот^ в организме [32]. Необходимо подчеркнуть, что механизм био-' синтеза жирных кислот у растений исследован слабее. j
Несомненно, что биосинтез полиизопреновых соединений проходит по общей схеме. По-видимому, все эти вещества синтезируются из одного общего исходного продукта, образующегося при участии кофермента А. Взаимная связь изопрена, различных терпенов, каротиноидов и каучука показана схемами строе-; ния этих веществ, приведенными в табл. 3. j
Биосинтез полиизопреновых соединений значительно слож-j нее, чем биосинтез жирных кислот, сложнее и эксперименталь-; пая проверка этого синтеза. Так, чтобы выяснить, какимі образом происходит построение каротина (V) из ацетата [32], произвели синтез радиоактивных р-каротинов и последующее дробное окислительное расщепление их. Синтез радиоактивных; р-каротинов осуществляли при выращивании плесени Mucor hie-' malis на питательной среде, где единственным источником угле-j рода служил C!4H3COsNa и при выращивании той же плесени' на среде, содержащей CH3CI402Na. Тот и другой радиоактив-j ный изомер р-каротина при дробном окислительном расщеп-; лении давали уксусную кислоту. Полученную уксусную кис-! лоту переводили в метиламин и углекислый газ, радиоактив-! ность которых и определяли. В результате было выяснено, что углеродные атомы исходного ацетата располагаются в следую-] щем порядке:
|
Н3с |
|
Сня |
|
С |
Нис С —СН = СН —с-сн—сн=сн—с=сн—сн=
|
Сня |
|
Н3с |
/х СН2 сн8
|
Сня |
|
Сн. |
=сн—сн=с—сн=сн—сн=с—сн=сн—с сн„
СНд СН2
Где х обозначены углеродные атомы каротина, образовавшиеся из С14, находящегося в карбоксильной группе ацетата; о — углеродные атомы каротина, образовавшиеся из С14, находящегося в метильной группе ацетата.
На примере сквалена [120] показано, что биосинтез полиизо - преновых соединений идет через ацетат и мевалоновую кислоту по схеме:
СН'3СО ~ SKoA -1- СН3СО—СН„СО ~ SKoA - KoAS ~ Н + III II
Ацетонофермент А Ацсто-ацетилкофермснт А Кофермент А СНя СНя
/с
СН, он С Но I
<оЛМ>г COOH
3. 3-імлріжси З-мстнл
|
ЛТФ |
|
АТФ |
|
/ |
|
I I |
Г ivr. i],!,_., І^цД
СН,
I
|
(Трифосфорпирндиинукленд) |
|
ТФПН-Н, |
■С
/К
СН, ОН СН.
Ноос соон
VII
|
(Аденоэнитрн- Фосфат) ЛТФ |
Мспалоиоьая кислоіа
|
Посредник С тремя атомами Р |
|
Сна нас Он "сна Н=0,Р0112С соон н3о„раонас СООН VII VIII 5-Фосфомева.'іоновая кислота 5-Дифосфомевалоиовая кислота |
Сн3
АТФ
Ус - СН3-СН, ОРаО„Н3
IljC
IX
|
Н, С ' > Их |
|
3.3-Диметилаллиллирофосфат |
Изопеитилпирофосфат
С=СН—СНаОРаОаНэ
Наибольший прогресс в исследовании химизма биосинтеза был достигнут при использовании ферментативных препаратов, полученных из дрожжей [120].
В опытах с ферментативными препаратами дрожжей было показано, что первые три стадии синтеза проходят с участием аденозинтрифосфата (АТФ) и двухвалентного катиона магния. В первой ступени синтеза происходит образование 5-фосфоме - валоновой кислоты (VII). Она может быть выделена из дрожжевого автолизата.
Второй процесс фосфорилирования, очевидно, приводит к 5-дифосфомевалоновой кислоте (VIII), все еще недостаточно охарактеризованной.
Следующим, третьим идентифицированным продуктом является изопентилпирофосфат (IX), строение которого доказано при ферментативном гидролизе, через изопентенол (XI).
СН2=С (СН3) —СНа—СН2ОН XI
Кроме того, он был искусственно синтезирован.
В изопентилпирофосфате (IX) карбоксильный углерод С] мевалоновой кислоты (VI) окисляется и не включается в молекулу сквалена и далее — в холестерин. Есть доказательства, что этот процесс не является простым декарбоксилирова - нием [120].
После образования изопентилпирофосфата (IX) биосинтез проходит через ряд превращений, из которых доминирующими
Являются ядернофильные активации—С—С— двойной связи. Было показано прямое энзиматиче9кое превращение изопентилпирофосфата в организме (также и синтетическим путем) в сква - лен. Есть основание предполагать, что первоначальная конденсация двух С5 единиц происходит при изомеризации одной и; них с образованием 3,3-диметилаллилпирофосфата (XI). Диме- тилаллилпирофосфат является веществом, которое может бы стро давать аллиловый катион при помощи потери пирофосфат ного нона. Этот катион, и качестве электрофилыюю агента может затем присоединиться по двойной связи изопентилпирофосфата (IX).
TOC o "1-3" h z ОРАНз СНз
">С=СН—СН2 + СН2=С—СН—СН2ОР2ОвН8
X Н IX
НзС,
^С=СН—СН2—СН2—С-=СН— CH2OPAHs + НОР АН3
Нчс XII
Гераиилпирофосфат
Подобная реакция приводит к геранилпирофосфату (XII), который может сам давать катион и реагировать тем же путем с другой молекулой изопентилпирофосфата (IX) и, в свою очередь, давать фарнезилпирофосфат (XIII).
,, г СН3 сн3
НзС | |
СН—CHg—СН2— С=СН—СН2—СН2—С^СН—СН„ОР2ОвН3
Н3С XIII
Фарнезилпирофосфат был идентифицирован как промежуточный продукт в биосинтезе сквалена.
Как отмечалось в опытах с гранами, выделенными из дрожжей [120], фарнезилпирофосфат превращается в сквален в присутствии восстановленного трифосфорпиридиннуклеида (ТФПН-Нг). Этот процесс проходит путем соединения двух Cis единиц углеродных атомов в месте, где углеродные атомы имеют сложноэфирные группы. Таким образом, имеется внешнее сходство с химическим синтезом сквалена (XIV) при реакции фар- незилбромида с литием. _
Н*сх I I
У С=СН—СН2—СН2—С=СН—СН2—СНа—С=СН—СНа— Н3С XIV
Сквален
В дальнейшем биосинтез от сквалена до холестерина требует присутствия в среде фермента, вызывающего окисление и циклизацию, отсюда и название его — сквалено-оксидоциклаза.
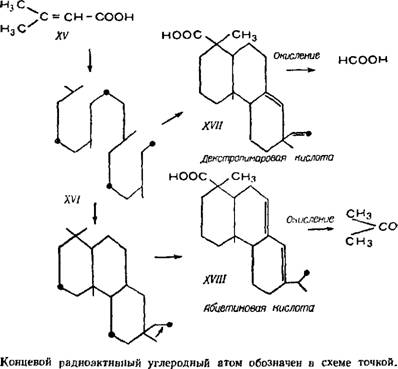
Если в настоящее время довольно хорошо изучен процесс биосинтеза от мевалоновой кислоты до холестерина [120], то процесс биосинтеза от мевалоновой кислоты до смоляных кислот изучен значительно слабее [152]. Тем не менее, опираясь на опыты по усвоению растениями соли калия радиоактивной 3,3-диметилакриловой кислоты (XV) и на предыдущий материал, приведенный в этом разделе, можно предполагать, что з растительном организме калиевая соль 3,3-диметилакриловой.•пк-лоты фосфорнлируется с образованием изопентилпирофосфата (IX). В дальнейшем через аллиловый катион и при помощи потери пирофосфатного fiona образуется гераниилпи- рофосфат (XII). Для образования дитерпенов требуется повторение последней реакции, что должно привести к гипотетическому ненасыщенному углеводороду ряда фитена (XVI), который в свою очередь окисляется и циклизуется.
Опыты по усвоению растениями калиевой соли 3,3-диметил - акриловой кислоты были поставлены следующим образом: соль, меченная по углеродному атому кислотной группы, вносилась в сосуд с почвой, в которой выращивался саженец сосны. Через в месяцев образовавшиеся в сосне смолистые вещества были извлечены экстракцией. Радиоактивностью обладали смоляные кислоты, скипидар, фитостерин и фитол. Затем провели исследование для доказательства радиоактивности концевых виниль - иой и изопропильной групп смоляных кислот. Разрушение смоляных кислот с целью отделения этих концевых групп производилось марганцовокислым калием в растворе этилового! спирта. Вначале в качестве моделей испытывались нерадиоактивные индивидуальные смоляные кислоты и их смеси и было показано, что изопропильная группа абиетиновой кислоты дает ацетон, а имеющаяся в декстропимаровой кислоте винильная группа образует формальдегид. Заключительный опыт был проведен с изомеризованной радиоактивной смесью смоляных кислот Образовавшиеся после окисления ацетон и формальдегид были разогнаны в виде их 2,4-динитрофенилгидразонов методом бумажной хроматографии. Оба соединения были радиоактивны. На основании этих опытов была составлена схема, показывающая, что обе группы смоляных кислот образуются из одного общего первичного вещества (XVII) (см. также табл. 3). При этом соединения группы пимарана (XVII) образуются без перестройки скелета, а группа абиетана (XVIII) —с перестройкой конца молекулы.
|
|
В заключение следует сказать, что биохимические работы значительно расширили наши сведения о биогенезисе терпенов и терпенондов, много вопросов по биохимии решено, ио еще больше ждут своего решения.
Недостаточно разработанной пока остается и теория смоловыделения, хотя частные вопросы этой теории разрабатывались многими исследователями, в том числе А. Е. Арбузовым, Е. Ф. Вотчалом, Л. А. Ивановым, А. Н. Шатернико- вой, Н. Л. Коссович и Ф. Т. Солодким.
По представлениям большинства исследователей, живица и древесине заполняет смоляные ходы. Эти ходы созданы живыми выделительными клетками, наружные оболочки которых срастаются в сплошное кольцо, образуя внешнюю стенку канала. Вещества, необходимые для синтеза живицы, находятся и плазме живых клеток. В живых клетках, как доказано исследованиями под микроскопом, возникают мельчайшие капельки живицы, которые проникают через внутренние стенки выделительных клеток, попадают в смоляной канал и заполняют его. Оболочки выдели тельных клеток обладают свойством пропускать живицу только с внутренней стороны в канал. После того как канал смоляного хода наполнится живицей, его выделительные клетки сплющиваются и прижимаются к стенкам канала. Когда смоляной ход надрезан, живица, находящаяся под давлением 12—20 атм, начинает вытекать. Процесс истечения длится до тех пор, пока сжатые смолой выделительные клетки под действием осмотического давления не примут первоначального вида. Чаще всего этот процесс прекращается из-за закупорки вскрытой части смоляного хода закристаллизовавшейся и заіустеишей живицей [23, 29, 37].
По представлениям Ф. Т. Солодкого, движение смолы по смолоходу живого дерева определяется не только силой осмотического давления клеточного сока, насасывающего воду в выстилающие клетки, расширяющего и и сжимающего тем самым смолоход. но и натяжением водяного тока, которое отсасьгваоі «оду п.: выстилающих клеток. Эта сила транспирационного сосания возникает в результате испарения воды в хвое. Ф. Т. Солодкий считает, что сосущую силу нужно считать активной, а силу осмотического давления — пассивной и зависимой. Когда сила транспирационного сосания меньше силы осмотического давления, то результирующая сила, действующая на смолу, является положительной величиной, и смоляной ход должен выдавливать смолу. Таким образом, выдвигаемая Ф. Т. Солодким теория движения смолы в заболони живого дерева основывается на наличии в смолоходе сил, выталкивающих и засасывающих смолу. Эта теория, по заявлению самого автора, явлиеіси лишь основой, упрощенной схемой, требующей подтверждения и дальнейшего развития.
Свежая, только что вытекшая из дерева живица представляет светлую вязкую жидкость, являющуюся раствором твердых смоляных кислот в жидкой смеси терпенов. При хранении живица теряет часть летучих веществ, густеет и выделяет кристаллы смоляных кислот. При соприкосновении с кислородом воздуха живица темнеет — окисляется, приобретая сначала светло-желтый цвет, а затем коричнево-вишневый.
При подсочке с закрытой раной можно получить живицу с содержанием скипидара 35,5%, но это содержание скипидара является максимальным и возможно только в том случае, ссли приняты меры полной герметизации приемников. Промышленная сосновая живица, как показывает табл. 4, содержит
|
Т аб л н ц а 4
|
Скипидара значительно меньше, и в ней на долю канифоли приходится 73,6—79,3%.
Несколько меньше скипидара, обычно до 12%, содержит ■еловая живица.
НАКОПЛЕНИЕ ФИЗИОЛОГИЧЕСКОЙ СМОЛЫ В СОСНОВОЙ «•ДРЕВЕСИНЕ И ЕЕ СОСТАВ
Из живицы при обработке паром получают скипидар и живичную канифоль. Остальные технические продукты, содержащие смоляные кислоты — экстракционную канифоль, талловос масло, талловую канифоль и сухоперегонную смолу из пневого осмола — получают из физиологической смолы, которую извлекают обработкой древесины органическими растворителями, щелочами или действием высоких температур. Состав физиологической смолы более сложен, чем состав живицы — патологической смолы.
Древесина сосны не во всех ее частях одинаково богата смолой. В заболонной части смола заполняет смоляные ходы; ее количество 2—4% по отношению к абсолютно сухой обессмо - ленной древесине. В ядровой части ствола смола в основном находится в трахеидах. Особенно богаты смолой трахеиды ядра в корневой шейке ствола. Отмирание дерева повышает смолистость древесины, но в распределение смолы не вносит каких-либо заметных изменений {55]. Это можно видеть из данных табл. 5.
|
Таблица 5
|
Основное промышленное значение имеет пневый осмол — естественно просмолившаяся часть долго находившегося в земле соснового пня. Исследованиями советских химиков установлено, что к 10—20 годам смолистость пневого осмола увеличивается на 20—30%.
Л. А. Иванов [37] и Э. И. Адамович [43] считают, что увеличение смолистости в ядровой части ствола происходит в основном в период жизни дерева. По данным работ, проведенных лабораторией лесохимии Карельского филиала АН СССР (46], при среднем возрасте сосны 122 г. средняя смолистость свежих пней составляла 14,0%, а в 167 лет она повысилась до 19,2% на абсолютно сухую обессмолснную древесину.
Л. К. Толкачев [37] показал, что осмол, полученный после рубки одновозрастных сосновых насаждений, оказался богаче У тех экземпляров, диаметр которых был больше. Увеличение количества смолистых веществ в осмоле, имеющем больший диаметр, также происходит быстрее. Автор исследовал 10- и 15-летние вырубки 115—120-летних насаждений под Ленинградом. Результаты исследований сведены в табл. 6.
Многочисленные наблюдения показывают, что очень высокое содержание смолы в древесине, как правило, сопровождается какими-либо поражениями древесины. Эти поражения могут являться следствием механических повреждений, произведенных человеком или насекомыми, или вызываться заболеваниями древесины, возбудителями которых могут быть бактерии и грибы (см. табл. 7).
|
Таблица 6
|
|
Таблица 7
|
Попутно необходимо отметить, что увеличение содержания смолистых веществ при жизни дерева зависит не только от его возраста, быстроты роста, процессов, связанных с отмиранием древесины, но и от тех условий среды (почвы, влаги), в которых оно произрастало. Болотные почвы дают осмол бедный, а боровые—богатый. Результаты работы К. Н. Короткова и В. И. Янушко [56]. отражающие зависимость смолистости осмола от состава почвы и типа леса, даны в табл. 8.
|
Таллина 8 СиСган смочи. "> к.'ific.
|
Касаясь механизма проникновения смолы из живой заболони к ядру, Н. Л. Коссович [37, 43Ц объясняет это тем, что выталкиваемая давлением живых клеток живица течет в сторону наименьшего сопротивления — в отмершие части смоляных ходов и через мертвые клетки — дальше в трахеиды.
Л. А. Иванов [37] и Э. И. Адамович [43] считают, что новообразование смолистых веществ в сосновом пне возможно за счет нормальной деятельности смоляных ходов в первые годы после рубки. В дальнейшем, как это отмечают Л. А. Иванов [37], Э. И. Адамович [43] и Ю. Н. Емельянов [43], происходит только относительное увеличение смолистости за счет уменьшения объемного веса древесины и отпада малосмолистой заболони.
Нами (43, 46] установлено, что происходит не только отпад малосмолистой древесины, но и концентрация смолы в верхних частях осмольного пня. Смола поднимается из корней в ствол по трахеидам ядра под действием капиллярного давления.
Процесс обогащения пневого осмола смолой быстрее происходит на юге и медленнее на севере (табл. 9). Это объясняется, может быть, более быстрым гниением заболони пня на юге, а вероятно, и тем, что на юге пневый осмол интенсивнее прогревается, смола становится менее вязкой и более подвижной.
|
Таблица 9
|
Анализы осмола на смолистость, произведенные в 1920 г. Н. П. Простосердовым на Соловецких островах Белого моря и А. И. Терлецким около Пинозера, севернее г. Кандалакши в Мурманской обл., подтвердили, что осмол на Севере через 15—30 лет созревает и вполне пригоден для эксплуатации. Средняя смолистость осмола, по данным А. И. Терлецкого, составляла 30,0% на абс. сухую и обесмоленную древесину. Почти такие же данные получены для сырьевой базы канифольно - экстракционного производства в районе г. Сегежи и г. Мед- вежьегорска Карельской АССР. Эта база изучалась в 1951— 1956 гг. Н. Ф. Комшиловым, И. В. Первозванским, О. И. Пи - липчук и Л. И. Спирковой [54]. Для осмола 15—30-летней спелости, добытого в Сегежском и Медвежьегорском районах, смолистость составляла 32,9—31,4%.
Основываясь на том, что пень проявляет жизнедеятельность первые годы после рубки, Ф. А. Медников [43] предложил удалять кору со свежих пней и тем стимулировать деятельность смоляных ходов. Это повысит смолистость заболони и ускорит возможность эксплуатации осмола.
Содержание канифоли в заболони свежих пней составило в среднем 1,82% на древесину 20%-ной влажности, в то время как окоренные пни содержали канифоли в заболони в первый год просмоления 7,5—9%, а после 2 лет— 10,7%.
Окоренные пни через 2 г. интенсивнее всего просмоляются в наружном слое (см. табл. 10). Содержание смолы в окоренных пнях повышается не только в заболони, но и в ядре [64].
|
Таблица 10
|
Смолистость всей древесины окоренных пней после 1—2 лет просмоления колебалась в пределах 13—14%. По содержанию канифоли эти пни являлись стандартным пневым сосновым осмолом. Контрольные неокоренные сосновые пни имели смолистость 5,6%.
Еще более интенсивно происходит просмоление заболони у окоренных на корню комлей сосновых стволов. За 1—2 г. содержание смолы в заболони комлей сосновых стволов возрастало в 4—6 раз и достигло 8—12%.
Особенно сильно просмоляются пни с единой корневой системой живого дерева [43, 46]. Анализ одного такого пня покапал содержание канифоли 50,0%, скипидара 5,6% при влажности древесины 2,0%.
По данным Д. Н. Смирнова и Ф. А. Медникова [43], состав нелетучей части эфирной вытяжки физиологической смолы пневого осмола сосны Pinus silvestris изменяется в зависимости от продолжительности хранения. Данные наблюдений отражены в табл. 11.
Как показывают данные табл. 11, интенсивно уменьшается количество жирных кислот по мере старения пня. Это можно объяснить отпадом заболони, богатой жирными кислотами; имеет значение и несовершенство метода количественного определения жирных кислот путем этерификации — сильно окисленные жирные кислоты этерифицируются с большим трудом [43, 55].
|
Таблица И
|
|
Зависимость состава смолы от места взятия пробы показана в табл. 12 [43]. Исходя из данных табл. 12 можно сделать заключение, что смоляных кислот больше всего в ядре, жирных— в заболони, а стеринов — в камбии. |
|
Таблица 12
|
Осмолозаготовители выкорчевывают сосновый пневый осмол на вырубках 7—15-летней давности. Добыча осмола производится в основном взрывным способом. Бригада в 6—8 человек может заготовить 20—30 скл. м3 за смену.
Заготовка сосновых пней тракторами С-80-100, оснащенных корчевателями Д-2Ю и др., высокопроизводительна и позволяет получать 20—30 скл. ж3 за смену, но не обеспечивает механизированной очистки пней от земли и может применяться лишь на вырубках, не имеющих подроста.
К. А. Демин и С. С. Ситников [33] предложили использовать для корчевки сосновых пней краны с применением виброзахватного устройства с возмущающей силой до 7 т. Опыты по заготовке сосновых пней краном К-Ю4 и краном, смонтированным на тракторе ТДТ-40, проводились в Медвежьегорском и Пове - нецком лесничествах Карельской АССР.
Кран двигается посередине полосы шириной 20 м с остановками через отрезки пути в 10 м — равные одному максимальному вылету стрелы. Крановщик регулирует вылет стрелы таким образом, чтобы виброзахватное устройство приняло отвесное положение непосредственно над пнем. Затем виброзахват опускается, его выступающие части подводятся под корни пня а стойки стягиваются при помощи двух болтов и цепи. После этого включается электродвигатель виброзахвата и пень извлекается из земли лебедкой 'Крана. Производительность агрегатг составляет 15—20 скл. м3 за смену. Трудовые затраты по заготовке осмола по сравнению со взрывным способом снижаются более чем в 2 раза. При этом ликвидируются такие тяжелые .ручные операции, как бурение, заравнивание подпневых ям и погрузка пней на автомашины. Кроме того, при такой корчевке. подрост практически не повреждается.
В настоящее время также изучается вопрос заготовки свежих сосновых пней одновременно при заготовке леса. Т. И. Ки - щенко и др. [42] дали следующие рекомендации по системе машин, применяемых при заготовке деревьев с корнями: дл* валки — трактор С-80 с бульдозером или другие валочные машины, для отряхивания земли от корней — вибромолот с воз мущающей силой до 7 т, для трелевки, погрузки на автомашинь и вывозки — любые существующие на лесозаготовках машины для разделки пней и корней—отбойные молотки с широкие лезвием, для раскалывания — колун специального назначения для переработки пневой древесины в технологическую щепу — рубительные машины и для сортировки щепы — обычные плоские или барабанные сортировки.
Заготовка деревьев с корневой системой в сосновых насаждениях и переработка свежих сосновых пней может в дальнейшем найти применение.
Выполнение плана производства экстракционной канифоли при условии завершения строительства запланированных заводов, все же может натолкнуться на некоторые затруднения, Видимо, за пределами 1970 г. запасы спелого пневого осмола будут сокращаться и постепенно могут сойти на нет. Причины этого в следующем: основная масса пневого осмола заготовляется в настоящее время из пней высотой 30—40 см. Обследования, проведенные за последние 10 лет, показали, чтс средняя высота пней на вырубках последних лет составляет лишь 15—20 см. Современная техника лесозаготовок позволяет] а на волоках даже предписывает спиливать деревья заподлицо с землей. Такая технология увеличивает выход деловой древесины и улучшает условия для использования механизмов. Есть опасения, что через 10—12 лет эти пни вообще нельзя будеї обнаружить — они зарастут мхом и травой, а это безусловнсі приведет к снижению запасов, концентрации спелого осмола м к значительному удорожанию его заготовки.
И. И. Бардышев, А. И. Калниньш [37,38], Ф. А. Медников[66' считают, что спелый пневый осмол вообще не является перспективным сырьем для развивающейся канифольно-экстракцион - ной промышленности.
Наиболее вероятным заменителем спелого пневого осмола является стволовый осмол. К сожалению, этому виду сырья в последние годы уделяется незаслуженно мало внимания.
Вельская подсочка или старинная система осмолоподсочки применялась еще до середины XVIII века, о чем свидетельствуют архивные документы.
Основные промыслы были сосредоточены в Архангельской губернии и особенно в Вельском уезде, в Вологодской губернии, а также в Финляндии.
В наше советское время осмолоподсочка сосредоточена в пяти районах Архангельской области: Вельском, Шенкурском, Ровдинском, Устьянском и Верхне-Томском. В отдельные годы в Архангельской обл. добывалось до 4,45 тыс. т терпентин-бар - раса и заготовлялось 100 тыс. пл. ж3 стволового осмола для использования в сухой перегонке.
Стволовый осмол как сырье для канифольно-экстракцион- ного производства имеет ряд преимуществ: 1) запасы стволового осмола на 1 га составляют минимум 30 пл. ж3, а запасы пневого осмола — максимум 10 скл. ж3, т. е. запасы стволового осмола на единице площади в несколько раз выше, чем пневого осмола, что существенно облегчает заготовку смолья-подсочки; 2) заготовлять стволовый осмол легче, и он более удобен к перевозке, что, несомненно, удешевляет стоимость сырья для ка- нифольно-экстракционного производства; 3) смолистые вещества могут быть извлечены из стволового осмола полнее и в более короткий срок, что также удешевляет стоимость продукции; 4) качество канифоли и скипидара будет выше; 5) качество проэкстрагированной щепы из стволового осмола будет также выше, чем из пневого осмола, а следовательно, из нее можно будет готовить хорошую целлюлозу, картон, древесноволокнистые и самого высокого качества древесностружечные :1Л1пы.
<-читается, что сгиоловыи осмол имеет существенный недостаток— низкую смолистость—10—12% на древесину 20%-ной влажности [100]. А низкая она потому, что сроки осмолоподсочки были необоснованно короткими, и древесина не просмаливалась должным образом. Срок в 8 лет осмолоподсочки без химического воздействия, обусловленный инструкцией 1963 г., также не даст осмол надлежащего качества.
Вот как описывал И. Гриневич (1877) [30] получение осмоло - подсочной высококачественной древесины. К осени второго года подсочка уже имела в вышину 4 аршина (2 ж 85 см). В этот год сбор терпентин-барраса был окончательный, и, сколько бы времени дерево подсоченным ни стояло на корню, терпентип - баррас с него уже не собирали. Потом в течение 5—7 лет дерево не подсачивали, и оно просмаливалось не только в районе карры, но и выше ее. После такого отдыха поднимали подсочку настолько, насколько позволял ствол, свободный от сучков, и опять давали отдых на два года. В последнее лето снимали оставленный ремень, и в октябре или ноябре дерево рубили. Таким образом, осмолоподсочка продолжалась 10— 12 лет, и подсоченная часть ствола имела высокую смолистость.
М. А. Токарский (1895) [94] сообщил, что до 1861 г. осмолоподсочка в некоторых случаях проводилась в течение 20 лет, а позднее после проведения лесоустройства в Вельском удельном имении, как правило, 10 лет. В. И. Лебедев считал, что осмолоподсочка в Архангельской обл. должна продолжаться от 7 до 15 лет.
На наш взгляд, осмолоподсочка должна продолжаться до тех пор, пока осмолоподсочный кряж не будет иметь смолистость выше 13% на древесину 20%-ной влажности, или иными словами, не будет удовлетворять ГОСТ 10077—62 на осмол, пригодный для использования на канифольно-экстракционных заводах. По нашим предварительным данным, в Карелии каждый год осмолоподсочка повышает смолистость заподсоченной части ствола приблизительно на 0,8% на древесину 20%-ной влажности. Отсюда вычисляется срок подсочки (13—4): 0,8= 11 лет, где 4 — процент смолистости неподсоченной сосновой древесины. Такой срок осмолоподсочки получается без применения химических стимуляторов, химические же стимуляторы должны несколько повысить ежегодную просмоляемость ствола [38].
Осмолоподсочка на севере может конкурировать с обычной подсочкой.
По данным треста Карелхимлесзаг, с 1 га можно собрать живицы-барраса 30 кг за сезон.
По нашим данным, с 1 га сосновых насаждений V бонитета можно получить около 30 пл. ма осмолоподсочной древесины. При смолистости осмола 13% на древесину 20%-ной влажности и прн коэффициенте извлечения 0,83 можно будет получить канифоли 10,8% от веса древесины, или 50 кг с 1 м3 Всего за 11 лет подсочки с 1 га можно получить (30x50) = 1500 кг канифоли, или за 1 год 136 кг. Таким образом, с 1 га осмолоподсочки можно иметь (136 + 30) = 166 кг канифольных продуктов, в то время как при проведении обычной подсочки самых высокопродуктивных насаждений в Карелии за 1 год получают менее 80 кг живицы.