НЕЛИНЕЙНЫЕ ДИНАМИЧЕСКИЕ ПРОЦЕССЫ И ФАЗОВЫЕ ПЕРЕХОДЫ
Нелинейные системы характеризуются фазовыми портретами с различными особенностями, в частности, с устойчивыми и неустойчивыми особыми точками. Нелинейные системы способны переходить из одних состояний в другие под действием малых флуктуаций, нарастающих до макроскопического уровня.
Шлёгль впервые показал, что в ряде случаев поведение нелинейной системы оказывается подобным фазовому переходу первого или второго рода [117]. Возникновение новой структуры в распределенной нелинейной системе имеет такой характер. Неравновесные переходы, определяемые неустойчивостями, давно известны в гидродинамике (например, переход от ламинарного к турбулентному течению и эффект Бенара, см. [1, 115,
116]).
Рассмотрим вслед за Шлёглем [117, 118] автокаталитические реакции (ср. стр. 415)
![]()
А + 2Х
С.
К.
■—2
Скорости реакций равны
(8.121)
V, = kxAX2-k-xX\ v2 = k2BX — k-2C,
Положим для простоты k. i = 1, k\A = 3 и обозначим k2B = р, k-чС = у. Скорость изменения концентрации X равна
X = v]-v2=-X3 + 3X2 — p>X + y. (8.122)
Стационарные состояния отвечают условию X = 0 или
Y = - ЗХ2 + pjf. (8.123)
Кривые vW, представляющие эту зависимость, показаны на
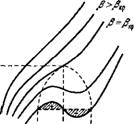
X/ Х3-7 Х2
Рис. 8.45. Фазовый переход первого рода в автокаталитической химической реакции.
1.
Х
Рис. 8.45. Уравнение X = 0 имеет три корня. Эти корни совпадают при критическом значении р — = Ркр:
Три различных вещественных и положительных значения корней Х2 > Х3 > Х[ возможны лишь при р < 3. Решения Xi, Х2 устойчивы, неустойчивый корень находится на убывающей ветви у(Х). Получилась картина, весьма сходная с диаграммой состояния газ — жидкость. При этом концентрация X играет роль плотности V-1, величина у соответствует давлению р, а величина р — температуре RT. Имеем
(8.124)
V3
Р 3,1 Y = V-T7T+
Уравнение Ван-дер-Ваальса имеет вид
RT о_
(8.125)
Р— V — b V2
B2RT - jTT-
Или в вириальной форме
(8.126)
RT, bRT ■
V2
Полная аналогия получается для вириального уравнения состояния
Р = RT/V — fli/V2 + (8.127)
С вириальными коэффициентами ai и а2, независимыми от температуры.
Таким образом, в рассматриваемой автокаталитической системе при р < ркр происходит переход между двумя устойчи
выми стационарными состояниями и Х2, подобный фазовому переходу первого рода. Внешним условиям, задаваемым р и у, отвечают два конкурирующих состояния Xi и Х2. Этот переход не связан с нарушением симметрии. Можно показать, что условие Максвелла — равенство площадей + и — на рис. 8.45 — соблюдается.
(8.128)
А® (Л)
(8.131)
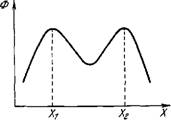
Рис. 8.46. Сосуществование фаз Xi и Х2.
(8.133)
Y = P'
*.,2=l=F(3-f5)\ *з=1.
Если одновременно с химической реакцией происходит диффузия компонента X (система является распределенной), то при постоянных значениях А, В, С получаем
X = у (*) + DV2X, причем y W можно представить в виде
У W'= Ж'ф Ф W = 'А*4 ~ + '/г?*2. (8.129)
Ф(^) играет роль некоторого потенциала. Считая диффузию одномерной, перепишем уравнение (8.128) в виде
(8.130)
Стационарные состояния удовлетворяют уравнению
D4^ =
Дг2 дХ
Это уравнение сходно с уравнением, описывающим движение массы в потенциальном поле, если 2 играет роль времени, а X — координаты. Имеется стационарное состояние, в котором сосуществуют две фазы Х\, Х2, причем Х-+Х\ при z —> ОО И Х-*~Х2 при 2 ->—OO. Xi и Х2 соответствуют относительные максимумы Ф(^). В стационарном состоянии происходит перемещение «массы» D от одного максимума Ф(Х), при котором эта масса покоилась, к другому максимуму, в котором она также достигает состояния покоя. Это возможно лишь в том случае, когда значения Ф в обеих точках одинаковы (рис. 8.46):
Ф(^,) = ф(^2). (8.132)
Мы получили условие сосуществования двух фаз, которое фиксирует значение у. Как показывает Шлёгль, из условия (8.132) следует
Наряду с фазовыми переходами первого рода нелинейные автокаталитические процессы могут приводить к неравновесным переходам, подобным фазовым переходам второго рода. Рассмотрим реакции
А + X 5± 2Х, В + X ї± С.
Их скорости равны
V2 = k2BX — k-2c.
(8.134)
V^kiAX-k-tX2,
Положим kiA= 1, k-t = \, k2B = $, k-2C — у. Находим
+ + + (8Л35)
X > 0 при малых X и X < 0 при больших X. Следовательно, стационарное состояние, отвечающее X = 0, устойчиво. В этом состоянии
Y = Z2-(1 — $)X = - f{X). (8.136)
Ч1;
(8.137)
X
Если Y — О, т0
— Р при Р< 1, при 1.
Такое поведение величины X характерно для фазового перехода второго рода, скажем, перехода из ферромагнитного в парамагнитное состояние. В этой аналогии X играет роль параметра упорядоченности (намагниченности), у — напряженности магнитного поля, р— температуры. Значение р = рКр = 1 отвечает точке Кюри. При р < ркр происходит нарушение симметрии. В критической точке малые флуктуации возрастают до макроскопических значений. Имеем, согласно (8.135),
Y + f(X)-,
ЬХ.
ДХ
Или
ДІ
(8.138)
6* = - (1/т) 6Z, (8.139)
Где т-1 = 2Х — (1 — р). При у —*0 и т-'->|1-р|. Но
Отсюда следует, ЧТО в критической точке Р= Ркр = 1, т —* оо.
На рис. 8.47 показаны кривые зависимости X от р при различных значениях у-
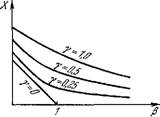
Рис. 8.47. Фазовый переход второго рода в автокаталитической химической реакции.
Отсюда
X ■■ ЬХ--
Эти аналогии, найденные Шлёглем, весьма поучительны. Поведение модельной химической системы, подобное фазовому пе
реходу, свидетельствует о ее кооперативных свойствах в истинном смысле этого слова, о переходах типа «все или ничего». Как мы видим, модели биологических систем, описывающие самоорганизацию, имеют именно такой характер. Это — триггерные системы, совершающие переходы в результате малых флуктуа - ций. Соответственно можно думать, что идея о неравновесных фазовых переходах как механизме биологических явлений является многообещающей. Уже получены некоторые интересные результаты. В работе [119] исследованы неравновесные фазовые переходы в системах ферментативных реакций при наличии субстратного ингибирования и диффузии. Показана возможность пространственного разделения фаз, соответствующих комплексам фермента с несколькими молекулами субстрата. Есть основания думать, что эти же представления окажутся весьма важными для понимания функционирования биологических регуляторных систем, в частности мембранных.
Как мы уже не раз подчеркивали, имеется далеко идущее сходство между химическими открытыми системами и системами экологическими — соответствие между моделями Лотка и Вольтерра (см. стр. 411). Посмотрим, каким образом аналогия с фазовыми переходами проявляется в моделях эволюционирующих популяций [120].
Рассмотрим менделевскую диаллельную популяцию диплоидных организмов с полным скрещиванием.
Цр-f v(l — р).
(8.141)
Аллель а отвечает дикому типу, b — мутантному. Можно определить коэффициенты приспособленности генотипов аа, ab, bb, равные соответственно wі, w2, как удельные скорости роста численности соответствующей популяции
Пусть частота прямых мутаций а —► 6 на поколение равна ц, частота обратных мутаций b —* а равна v. Как показывает динамическая теория популяций (ср. [121, 122]), динамика частоты р появления гена а описывается уравнением
(ші — w2) р + ІЩ — виз) р
![]()
Шір2 + 2ffi>2p (1 — р) + виз (1 — р):
Здесь время измеряется в числе поколений. При выводе уравнения (8.141) предполагалось, что [i, v< I; — w2, w2 — w3
(8.142)
W2. В этом случае вид формулы не зависит от того, что чему предшествует, — мутация отбору или наоборот. Перепишем уравнение (8.141) в виде
= R ' (Р) («о ~ aiP — а2р2 — ct3p3),
Где
R (р) = Wlр2 + 2®2р (1 _ р) + о>з (1 - р)2 > 0, (8.143)
/ а0 = vwu al = y, w1 — K, a2 = K(3q—l)/q,
А3 = х(1 — 2q)/q, k = w2 — w3. '
Величина q выражает степень доминирования аллели а в гете - розиготе ab, т. е. 0 < q = (w2 — w3)/(wi — ws) < 1. Выражения коэффициентов осі (см. (8.144)) получаются при условиях {3 w2,
Ц, V 1, V < ц.
В стационарном состоянии популяции р = const, и из (8.142) находим для стационарных значений р
А0 = f (Р) = «іР + а2р2 + а3р3. (8.144а)
Изменению условий существования популяции отвечает изменение параметров р, ц, v, определяющих, согласно (8.142), темп эволюции и, согласно (8.144а), ее конечный результат. Диаграмма стационарных состояний — зависимость f от р (8.144а)—■ совершенно подобна зависимости (8.123), представленной рис. 8.45. Эти «ван-дер-ваальсовы» кривые получаются при различных значениях к при условиях к < ци>і (aj > 0) и q < '/з (a2 < 0, a3>0). При этом кубическое уравнение (8.144а) имеет три вещественных положительных корня, совпадающих в критической точке, в которой
И одновременно
ЧцЛр 9(1 — 2q) (1 — 3(/ + 3q2) ' \%)кр Зш,? (1 - 2<?) '
При к > икр существуют три стационарных значения р! < < Рз < р2, причем рз — неустойчиво, а Рь р2 — устойчивы. Подобно реальному газу популяция способна пребывать в двух устойчивых стационарных состояниях, переход из одного состояния в другое аналогичен фазовому переходу первого рода. Переход вызывается достаточно большими флуктуациями численности и состава популяции.
Допустим, что популяция непрерывно расселена в своем ареале. Динамика популяции описывается уравнением, включающим миграцию особей (диффузию)
4F = iHp) + DV2p, (8.147)
Где г|з(р)—правая часть уравнения (8.142), а коэффициент диффузии D выражается через среднее расстояние г, на которое мигрируют особи за время жизни т, D = г2!т. Диффузия не нарушает устойчивости пространственно однородных стационарных состояний, представляемых решениями для нераспределенной системы (8.144). Однако при этом возможно появление устойчивого пространственно неоднородного распределения р(л). Могут возникать две пространственно разделенные фазы, каждая из которых отвечает устойчивому состоянию. Согласно (8.147) условие их устойчивого сосуществования находится путем минимизации функционала
W=^2?dr, (8.148)
Где лагранжиан 3? {р, Vp) равен
^ = V2D(Vp)2-^(p)dp. (8.149)
Минимизация (8.148) при постоянстве полного объема системы дает
Рг
Ф(Рі) = ЧФ2) = 0, J $(p)dp = 0. (8.150)
P.
Первое равенство (8.150) есть условие стационарности решений pi и р2, второе аналогично условию Максвелла для газа Ван - дер-Ваальса.
Аналогичные соотношения получены ранее Шлёглем для автокаталитической реакции (см. стр. 466), дополненной диффузией [117].
Пространственное разделение популяции есть первый этап на аллопатрическом пути видообразования. Дальнейшее существование аллопатрической формы приводит к накоплению в ней новых признаков и к биологической изоляции. Географическое разделение популяции оказывается подобным пространственному разделению при равновесном фазовом переходе первого ряда.
Структура популяции, эволюционирующей согласно уравнению (8.141), может претерпевать и переходы, подобные фазовым переходам второго рода, если при некоторых бифуркационных значениях параметров нарушается устойчивость стационарных состояний по отношению к малым флуктуациям. Такой переход происходит при обращении аі в нуль, т. е. при к = {iwi. Стационарная зависимость p(ai) имеет излом в точке ао = 0, характерный для фазового перехода второго рода— кривые p(ai), т. е. р(—к), совершенно подобны изображенным на рис. 8.47. Величины р, а0 и ai = \vw\ — х аналогичны, соответственно, намагничению, напряженности магнитного поля и отклонению от точки Кюри (Г — Тк)/Тк для перехода ферромагнетик — парамагнетик. Можно показать, что вблизи точки перехода резко возрастает время релаксации флуктуаций в устойчивом стационарном состоянии и восприимчивость системы к изменению параметров. В распределенной системе, описываемой (8.147), при дополнительном включении в нее случайных внешних воздействий объемные флуктуации и радиус корреляции флуктуаций возрастают с приближением к точке перехода. Переход к новой организации через точку потери устойчивости происходит флук - туационно — все большие объемы захватываются коррелированными флуктуациями, являющимися результатом малых внешних воздействий. Популяция приобретает при этом лабильность, которая может привести к быстрой эволюции, например, к вьн ходу в новую адаптационную зону (ароморфоз). Такое «вскрьк тие эволюционных резервов» происходит при низкой интенсивности избирательной элиминации. В эволюции этапы непрерывного развития в устойчивом режиме чередуются с переходными этапами, подобными фазовым переходам.
Таким образом, биологическое развитие оказывается связан* ным с нелинейными явлениями типа фазовых переходов. Даль-; нейшее построение соответствующей теории представляется мно^ гообещающим. Проблемы развития рассматриваются в следую^ щей, заключительной главе книги.