Электронный Парамагнитный резонанс в биологии
Ранни е эксгериые ггы
Для биохимика и биолога больший интерес представляют свободные радикалы, образующиеся в процессе обычных метаболических реакций, нежели свободныо радикалы, образующиеся при облучении (хотя исследования, связанные с облучением, приобретают все боЯъшее значение в таких областях, как, скажем, радиотерапия). В разд. 4.5 и далее мы рассмотрим динамическую концентрацию свободных радикалов, участвующих в метаболических процессах или ферментативных реакциях. Но поскольку впервые метод ЭПР был применен в биологии при исследовании свободных радикалов, образующихся под действием излучения высокой энергии, с них, по-видимому, и следует начать.
Первые исследования биологического материала методом ЭПР были выполнены в лаборатории Горди в 1955 г. Горди, Ард и Шилдс [5] подвергали аминокислоты и белки воздействию рентгеновского облучения и изучали возникающие при этом спектры. Некоторые из них представлены на фиг. 54. Все они получены при комнатной температуре на твердых образцах; поскольку образующиеся свободные радикалы, захваченные твердой матрицей, стабильны, их спокойно можно изучать и по окончании облучения. Следует отметить, что из-за отсутствия беспорядочного молекулярного движения ширина линии поглощения в этих спектрах очень велика по сравнению с той, которая наблюдается в растворах.
|
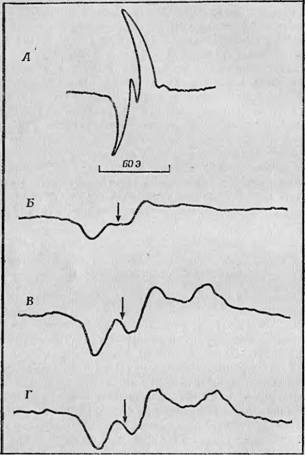
Фиг. 54. Спектры ЭПР, полученные на биологических объектах, подвергнутых рентгеновскому облучению [5]. А — шелк-сырещ Б — цистип; В — волос; Г — ноготь. |
При рентгеновском облучении шелка-сырца был получен простой спектр, состоящий из одного дублета (фиг. 54, А). Этот спектр был записан при двух различных частотах — 9 и 23 ГГц, и в обоих случаях получался один и тот же дублет с одинаковым расщеплением, равным 12 Э; следовательно, это расщепление действительно обусловлено сверхтонким взаимодействием, а не смещением g'-фактора. Наличие такого дублета, состоящего из линий одинаковой интенсивности, позволяет с уверенностью предположить, что неспаренный электрон взаимодействует с одним протоном. Обнаружив почти такой же спектр у облученного глицилглицина, Горди, Ард и Шилдс [5] первоначально предположили, что резонанс вызывается протонами, участвующими в образовании водородных связей в полипептидных цепях этих молекул.
В отличие от этого простого дублета, расположенного симметрично относительно g-фактора свободного электрона, спектры облученного цистина и различных кератиновых структур (их форма почти одинакова) сильно асимметричны относительно g-фактора свободного электрона (его положение обозначено стрелкой). Это означает, что должен существовать некоторый сдвиг в значении g'-фактора свободного радикала, обусловливающего этот спектр, а поскольку такой сдвиг в высшей степени необычен для органических свободных радикалов, его следует как-то объяснить. Вспомним, что значения g-фактора таких свободнорадикальных спектров почти всегда очень близки к значению g-фактора свободного электрона, так как у неспаренного электрона, находящегося на сильно делокализованной молекулярной орбитали, спин-орбитальная связь очень мала. Однако существуют два атома, электронная структура которых может вызывать довольно значительный сдвиг g'-фактора, если неспаренный электрон будет более или менее активно взаимодействовать с ними. Этими атомами являются атомы кислорода и серы. Если неспаренный электрон свободного радикала включает какой-либо из них в свою молекулярную орбиталь, g-фактор может сдвигаться очень сильно и достигать значения 2,05 [6]. Исходя из этого, Горди, Ард и Шилдс [5] предположили, что наиболее вероятным объяснением асимметрии спектров ЭПР цистина и кератинов является миграция неспаренных электронов и вакансий, образующихся под действием рентгеновского облучения, на атомы серы полипептидной цепи с последующей их локализацией на этих атомах.
Когда из молекулы под действием облучения выбивается электрон, участвующий в образовании связи, вакансия передвигается на атом серы, где она будет обладать наименьшей возможной энергией. В результате между этим атомом серы и другим, уже связанным с ним обычной двухэлектронной связью, образуется трех - электронная связь. Таким образом, после отдачи неспаренного электрона на группу, подвергнутую облучению, связь между атомами серы (тиоловая связь) не ослабляется, а усиливается. Такой быстрый перенос электронов и вакансий вдоль полипептид - ных цепей с образованием подобных S — S-связей может играть роль защитного механизма против радиационного повреждения; атомы серы служат как бы «электронными резервуарами» для' заполнения вакансий, возникающих при действии рентгеновского облучения. Судя по спектрам облученных кератинов (волосы и ногти), облучение вызывает в этих белках, по-видимому, те же повреждения, что и в молекуле цнстина, и эти спектры также молено объяснить миграцией на атомы серы.
Мы рассмотрели в качестве примера одну из самых раипих работ, посвященных исследованию биологического материала методом ЭПР. Конечно, в то время можно было провести лишь предварительный анализ полученных данных, и в более поздних работах некоторые аспекты интерпретации пришлось изменить. Тем не менее эти начальные эксперименты заложили основу для последующих более подробных исследований и послужили толчком для более глубокого изучения механизма защитной функции атомов серы нри радиационном поражении.