Электронный Парамагнитный резонанс в биологии
Применение метода ДЭЯР
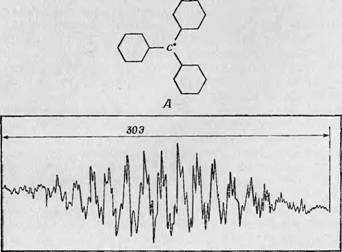
Вопрос о том, каким образом принцгп и. технику метода ДЭЯР,', описанные в разд. 3.8 и. 3.9, можно приложить к исследованию биохимических систем, лучше всего, по-видимому, рассмотреть на примере экспериментов с фталоцианином меди. Структура фталоцианина меди, очень близка к структуре некоторых биохими чески важных соединений, и. на нем была проведена серия специальных исследований методом ДЭЯР. В начале книги мы рассматривали. спектр ЭПР фталоцианина меди в качестве примера суперсверхтонкого расщепления; в этом веществе «том меди располагается в центре квадрата, образованного четырьмя атомами азота (фиг. 14, А). В спектре ЭПР фталоцианина на. каждую сверхтонкую линию, обусловленную атомом меди, накладывается девять суперсверхтонких линий, обусловленных атомами азота (фиг. 14, Б), и. на этом основании можно заключить, что волновая функция неспаренного электрона атома меди охватывает эти. атомы азота. Подробный анализ суперсверхтонкого расщепления, обусловленного атомами азота, позволяет точно характеризовать молекулярную орбиталь, связанную с атомом меди и. его окружением.
Система энергетических уровней фталоцианина меди, уже обсуждалась в разд. 6.3 и. была приведена на фиг 93. Неспаренный электрон локализуется на разрыхляющей орбитали Ве, Сразу над которош находятся разрыхляющие орбитали. B*g и Е*. Можно видеть, что орбиталь В*Ju образуется в результате гибридизации. dxz-vi - орбитали. центрального парамагнитного иона и. сг связей тигандных атомов. Волновая функция этой орбитали
Имеет вид
Ji
= N-dX2-y2 —(— Sj + s2 — s3+ s4) —
--^-(-Pi+Pz-P-S + Pi), (7.1)
Где N есть мера примеси от центрального атома меди, a %s и %р характеризуют распределение волновой функции неспаренного электрона по атомам азота, окружающим атом меди. Символами st, S2, S3, и Pi, P2, PЗ, Pi обозначены волновые функции 2s - и 2р-орбиталей четырех таких атомов азота.
Теоретическое выражение для значений g-фактора этого комплекса можно вывести способом, описанным в разд. 6.3; в это выражение будут также входить примесные коэффициенты для более высоких орбиталей и EJ. Однако значения Хя и Хр В выражении для волновой функции орбитали можно также определить непосредственно на основании величины наблюдаемого суперсверхтонкого расщепления, обусловленного атомами азота. Величина суперсверхтонкого расщепления в направлении, параллельном оси симметрии, проходящей через атом меди, может быть записана в виде
Аналогичное выражение можно вывести для расщепления в перпендикулярном направлении [8]. Отсюда ясно, что, измерив суперсверхтонкое расщепление, можно непосредственно определить коэффициенты Xs и Хр. Поскольку метод ДЭЯР позволяет измерять суперсверхтонкое расщепление несравнимо более точно, чем метод ЭПР, он может явиться источником дополнительной, очень точной и прнмой, количественной информации о природе химических связей.
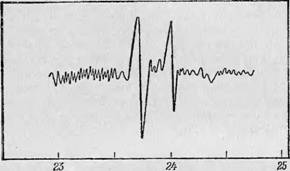
Фталоцианин меди является металлоорганическим соединением, которое уже исследовали с помощью ДЭЯР-спектроскопии [8] и суперсверхтонкое расщепление которого было определено именно этим методом. Спектр ДЭЯР, наблюдаемый на фталоциа - нине меди, приведен на фиг. 117. Из кривых такого типа величину суперсверхтонкого расщепления можно определить непосредственно, исходя из значения резонансной частоты, при которой снимается насыщение, а не из величины расщепления между пиками. Измеренная таким образом величина суперсверхтонкого расщепления оказалась равной 42 МГц [8]; подстановка этого значения в уравнение (7.2) дает числовые значения для и Хр, Хорошо согласующиеся с ожидаемой.^-гибридизацией орбиталей лигандных атомов.
Поскольку структура фталоцианина очень похожа на структуру гема, следует ожидать, что и по спектру ДЭЯР гема удастся получить точные сведения о распространении, волновой функции центрального атома железа на связанные с ним атомы азота. Попытки проведения таких экспериментов на кристаллах миоглобина и гемоглобина уже делались, но до сих пор не удалось непосредственно измерить суперсверхтонкое расщепление, обусловленное атомами азота. По всей вероятности, это объясняется
|
Частота ЯМР, МГц Фиг. 117. Спектр ДЭЯР фталоцианина меди. ЭПР-частота равна 8977 МГц, И = 3286 Э. |
Уширением, возникающим из-за хаотической ориентации, молекулярных осей; дальнейшие эксперименты при различных температурах, возможно, позволят выяснить правильность этого предположения. И все же при исследовании, этих соединений методом ДЭЯР удалось получить некоторые результаты: Айзен - бергер и Першан [9] наблюдали взаимодействие железа с протонами лигандного окружения гема.
Сначала все ДЭЯР-эксперименты проводились на монокристаллах, но в последние годы этот метод применили также для исследования свободных радикалов в растворах [10]. Основным условием, соблюдение которого необходимо строго контролировать при. проведении исследований методом ДЭЯР, является полное или. частичное насыщение поглощения ЭПР; поэтому очень важно, чтобы условия эксперимента всегда были оптимальными. При работе с растворами для достижения насыщения обычно требуются очень высокие уровни микроволновой мощности; как правило, наилучшие результаты получаются при температурах чуть выше температуры замерзания растворителя и при кон-
|
Б |
|
14 15 16 17 18 19 20 Фиг. 118. Спектры ЭПР и ДЭЯР трифенилметила [11]. |
|
Частота ЯМРМГц В |
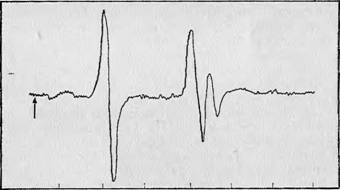
А — структурная формула трифенилметила; Б —- спектр ЭПР при высоком разрешении; В — спектр ДЭЯР, из которого сразу видны три основных типа взаимодействия (стрелкой указана ларморова частота свободного протона).
Центрациях порядка 10~3 М [И]. Но иногда насыщение достигается при микроволновой мощности, равной всего около 1 мвт, и. в этих случаях желательно использовать растворители с низкой диэлектрической проницаемостью, чтобы обеспечить максимальный коэффициент заполнения. Однако в большинстве случаев лучше использовать высокие входные значения микроволновой мощности [12, 13], так как, если температура растворителя сильно отличается от его температуры замерзания, время релаксации, становится очень малым.
Одно из важнейших преимуществ метода ДЭЯР лучше всего продемонстрировать на примере спектров свободных радикалов. Следует помнить, что в ароматических структурах, как правило, имеются две или несколько групп углеродных атомов, характеризующихся различной спиновой плотностью. ВследствивЧ этого возникают несколько групп сверхтонких линий с различной величиной расщепления в каждой группе; накладываясь друг на друга, эти линии, дают спектр с очень слояшой структурой. В качеству конкретного примера рассмотрим случай трифенилметила, структурная формула которого приведена на фиг. 118, А, А наблюдаемый спектр ЭПВе— на фиг. 118, Б. Этот СПектр состоит из большого числа линий, и интерпретация его довольно затруднительна. Но'ёсли использовать метод ДЭЯР, то вместо такого сложного спектра получается простая картина, показывающая, что все эти сверхтонкий! линии обусловлены тремя основными видами расщепления (фиг. 118, В) [11]. По наблюдаемым в спектре ДЭЯР трем «пиниям сразу можно определить величины расщепле-й ния. Таким образом, этот простой спектр содержит всю информацию, заключенную в спектре ЭПР^ и в тоГше время сильно упрощает анализ волновой функции.
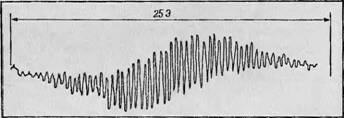
Все сказанное по поводу трифенилметила относится иж асимметричным молекулам. На фиг. 119, А изображено асимметричное производноежтрифенилметила, а на фиг. 119, Б — его спектр ЭПР. Как и в предыдущем случае, этот спектр очень сложен и состоит из множества линий с плавно меняющейся интенсивностью. Спектр ДЭЯР этого производного представлен на фиг. 119, В, И, хотя он содержит больше пиков, чем спектр исходного трифенилметила, найти величины расщепления непосредственно из этого спектра все и® гораздо проще, чем проводить сложный анализ самого спектра ЭПР. Кроме того, когда температура образца становится выше —20е С?>его спектр ДЭЯР существенно изменяется, что свидетельствует о каком-то конформационном изменении в исследуемом производном трифенилметила. Судя по тому, что некоторые соседние линии сливаются в одну с промежуточным значением g-фактора, при. более высокой температуре происходит обменное взаимодействие между двумя конформация - ми. Проанализировать изменения, вызываемые этим процессом в спектре ЭПР, крайне трудно, и это еще раз подчеркивает преимущества метода ДЭЯР, с помощью которого сверхтонкие взаимодействия можно исследовать непосредственно.
|
ГУ^ < у- с* ch,-sch, А
Б |
|
К 15 16 17 18 19 Частота ЯМР, МГц |
В
Фиг. 119. Спектры ЭПР н ДЭЯР асимметричного пронзводпого трифенплме-
Тила [11].
А — структурная формула производного трифенилметила; Б — спектр ЭПР; В — спектр ДЭЯР, показывающий, что в этом случае имеют место десять различных типов взаимодействия (стрелкой указана ларморова частота свободного протона).
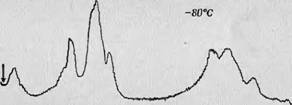
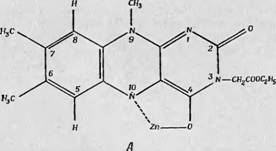
В качестве примера использования ДЭЯР-спектроскопии для исследования радикалов, участвующих в биохимических процессах, можно привести работу Хайда [11], посвященную хелатному цинковому производному радикала люмифлавина. На фиг. 120, А показана структурная формула этого вещества, а на фиг. 120, Б — Его спектр ЭПР [14]. Наличие в спектре сверхтонкой структуры из 14 линий (величина расщепления 3,5 Э) можно объяснить
|
|
|
|
__________ I_______ I_______ I_______ ;_______ I______________ I_
14 15 Ffi 17 18 19 20
Частота Я MP, МТц
Б
Фиг. 120. Спектры ЭПР и ДЭЯР радикала хелатиого цинкового производного люмпфлавина.
А — структурная формула этого вещества; Б — спектр ЭПР при содержании Zn"4, равном 99% [14]; В —спектр ДЭЯР (стрелкой указана ларморова частота свободного
Протона) [11]. См. текст.
Взахшодействием с эквивалентно связанными протонами метальных групп в положениях 7 и 9, с протоном в положении 5, а также с атомами азота в положениях 9 и 10 (фиг. 120, А).
На фиг. 120, В показан спектр ДЭЯР этого же радикала в растворе, полученный Хайдом. Здесь наблюдаются только две резонансные линии — при 18,843 и 18,526 МГц. Эти значения частоты соответствуют значениям константы связи 3,72 и 3,5 Э, что согласуется с наблюдаемым в спектре ЭПР сверхтонким расщеплением в 3,5 Э. На этом примере можно еще раз убедиться в ценности метода ДЭЯР как прямого метода измерения сверхтонкого расщепления. Совсем недавно это было еще раз подтверждено исследованиями дегидрогеназы [29].
Помимо измерений ДЭЯР-поглощения на свободных радикалах в растворе и на монокристаллах сейчас проводятся также эксперименты, в которых делается попытка применить метод ДЭЯР к спин-меченым биологическим молекулам [11]. В следующем разделе будет показано, что анализ спектров ЭПР стабплышх свободных радикалов, присоединенных к различным участкам биологической молекулы, может дать весьма интересную информацию.
ДЭЯР-спектроскопия этих спин-меток, как и ДЭЯР-спектро - скогшя обычных свободных радикалов, должна повысить точность получаемой информации. Исследования биологических молекул методом ДЭЯР и методом спин-меток еще только начинают развиваться, но следует ожидать, что в ближайшем будущей! в этих областях будут достигнуты значительные успехи.
Нужно упомянуть о том, что в настоящее время для исследования биологических молекул используют также метод, в известной степени обратный методу ДЭЯР. Он состоит в том, что снимается ЯМР-спектр исследуемого вещества и затем регистрируются изменения этого спектра в присутствии парамагнитных соединений. В недавних работах, выполненных с помощью этого метода [15], было показано, что на скорость спин-решеточной релаксации протонов воды и других протонов, содержащихся в биологическом объекте, очень существенно влияет присутствие неспаренных электронов. Наличие такого перекрестного взаимодействия дает возможность увеличить величину ЯМР-поглоще - ния на несколько порядков.
Этот вид двойного резонанса, часто называемый эффектом Оверхаузера, приобретает все большее значение в ЯМР-спектро - скопии. И хотя эти эксперименты относятся к области ЯМР-, а не ЭПР-спектроскопии, каждый исследователь, интересующийся механизмом спин-решеточной релаксации в биохимических соединениях, должен. знать о существовании этого метода, позволяющего исследовать электронно-ядерные перекрестные взаимодействия.
1/2 18-1182