Электронный Парамагнитный резонанс в биологии
ЭПР-исследоваиия негемового железа
При исследовании природы связи железа в биологических соединениях и белках наибольшее внимание уделялось железу, входящему в состав гема. Но существует ряд других биологически важных молекул, в которых тоже имеется железо, но не входящее в состав гема. Эти молекулы также исследуются методом ЭПР, и, хотя до сих пор такие работы еще не дали столь же точной и исчерпывающей информации, как и работы по гемсодержащим белкам, это направление, по всей вероятности, следует считать весьма перспективным.
Негемовое железо в белках обычно дает сигнал ЭПР, характеризующийся g-фактором 1,94; об этом сигнале мы уже говорили в разд. 5.7 при обсуждении железосодержащих ферментов. В том же разделе отмечалось, что природа иона железа, обусловливающего этот специфический сигнал, еще не выяснена, и в настоящее время существуют многочисленные теории относительно его пр оис хождения.
В определенных условиях железо, содержащееся в биологических объектах, дает сигнал ЭПР с эффективным значением g", равным 4,3. Впервые такой сигнал был описан Сандсом [29] в 1955 году при исследовании ЭПР-поглощения в стеклах. Происхождение этого сигнала можно объяснить следующим образом: в основном атомы железа находятся в высокоспиновом состоянии S — 6/2, но местоположение каждого из них обладает в большой степени ромбической симметрией. Вследствие этого имеет место значительное примешивание энергетических уровней трех пар спиновых состояний, и при измерении на обычных частотах Х-диапазона переходы наблюдаются при значении поля, соответствующем g — 4,3. Точно так же, как в случае кубической симметрии поля значение g8jM на самом деле не равно 6,0, а лишь кажется таким в определенных условиях, при ромбической симметрии gравное 4,3, в действительности вовсе не является истинным значением g-фактора. При интерпретации сигнала с таким g-фактором следует проявлять даже большую осторожность, чем в случае с сигналом g = 6: энергетические уровни в полях с высокой степенью ромбической симметрии легко изменяются в зависимости от длины волны, и поэтому в каждом случае очень важно измерять кажущиеся значения g-фактора при различных микроволновых частотах. Подробное изложение теории резонанса при g^S4>= 4,3 читатель, интересующийся этим вопросом, может найти у Блумберга [30[. Этот автор пришел также к выводу, что количество информации, которую можно получить об атомах железа этого типа, быстро возрастает с повышением используемой в эксперименте микроволновой частоты.
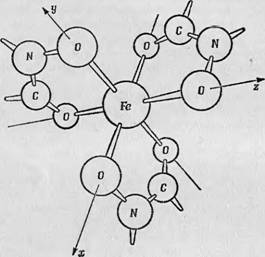
Вскоре после того как g-фактор, равный 4,3, был обнаружен в неорганических стеклах, он был описан также в различных биохимических соединениях [31, 32] и биологических образцах [33]. Хорошим примером может служить работа Уикмэна и сотр. [33] по исследованию ЭПР феррихрома — циклического гекса - пептида, выделяемого из гриба Ustillago sphaerogena. Как показал рентгеноструктурный анализ, центральный атом железа в этой молекуле окружен октаэдром из атомов кислорода. В первом приближении можно считать, что железо располагается на участке, характеризующемся кубической симметрией, но, как можно видеть из фиг. 113, связывание шести атомов кислорода приводит
|
Фиг. 113. Лигандное окружение атома железа в феррихроме. Ион Fe"+ окружен октаэдром атомов кислорода; связывание этих атомов происходит с образованием замкнутых циклов и вызывает сильное ромбическое искажение кубической симметрии. |
К значительному ромбическому искажению. Такой атом железа дает относительно широкие линни ЭПР-поглощения с центром у g' = 4,3. Уикмэн и др. [33] показали, что полученные ими результаты можно объяснить исходя из резкого изменения энергетических уровней, связанных с высокоромбическим полем, и что они хорошо коррелируют с данными рентгеноструктурного анализа того же соединения.
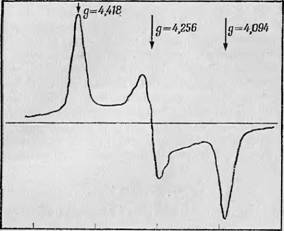
Спектры ЭПР того же вида с центральным значением g-фактора, равным 4,3, были получены и на других биологически важных соединениях, содержащих железо. На фиг. 114 в качестве примера приводится спектр поликрпсталлического комплекса Fe3 +— ЭДТА [34], содержащий три отчетливо выраженные
|
№0 /500 1550 №00 1650 Напряженность магнитного поля, Э А |
|
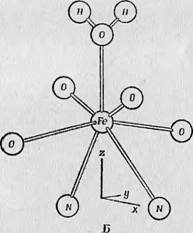
Фиг. 114. Спектр ЭПР комплекса Fe8+— ЭДТА [34]. Объяснение см. в тексте. |
Линии; по-видимому, они соответствуют величинам g-фактора для трех главных осей. Окружение атома железа для данного случая приводится на фиг. 114, Б; нетрудно заметить, что, как и в случае феррихрома, в первом приближении симметрию можно считать кубической, но имеет место сильное ромбическое искажение. Блумберг [30] рассчитал на основании этих данных константы
17—1182 расщепления D и Е; полученные им величины D = 0,769 см"1 и Е = 0,236 см-1 хорошо согласуются с теоретически ожидаемыми для данной конфигурации. Для анализа спектров ЭПР других биохимических соединений, содержащих железо нТ участках с низкой симметрией, та к^ке можно применить общий метод, предложенный Блумбергом Таким образом, молекулярное окружение центрального парамагнитного атома можно исследовать методом ЭПР даже в тех случаях, когда оно имеет сложную конфигурацию и относительно низкую симметрию. Более того, такого роде измерения можно проводить не только на монокристаллах, но и на поликристаллических или жидких образцах.