Электронный Парамагнитный резонанс в биологии
ЭПР и канцерогенная активность
В предыдущем разделе было показано, что методом ЭПР обнаруживаются высокие концентрации неспаренных электронов в некоторых веществах, обладающих канцерогенной активностью [52j, и это дает основание предполагать, что она так или иначе связана с присутствием неспаренных электронов. Хотя эти предварительные эксперименты не дали материала для построения какой-либо развернутой гипотезы о механизме канцерогенеза, они послужили толчком для возникновения ряда интересных предположений, связывающих канцерогенную активность с конкретной электронной конфигурацией молекулярных орбиталей исследуемых молекул.
Такой подход на электронном уровне к объяснению механизма канцерогенеза впервые предложили А. Пюльман и Б. Пюльман [53]. исходившие из той же теории, которую Хюккель [2] раньше применил к более простым молекулам, обсуждаишимся выше в разд. 4.2. Они постулировали, что взаимодействие канцерогенных ароматических углеводородов с компонентами клетки осуществляется через некоторые специфические участки углеводорода и может иметь место лишь при условии, что в образовании связей между углеводородом и клеточными структурами принимают участие делокалнзованные л-электроны молекулы углеводорода. В результате некоторые из этих связей оказываются двойными и общее электронное облако углеводорода приобретает хиноидную конфигурацию. Достоинство этой теории состоит в том, что она приложима ко всем углеводородным молекулам;
Имеющиеся в настоящее время экспериментальные данные [54] указывают на то, что связи между углеводородом и живой тканью действительно имеют хиноидкую природу.
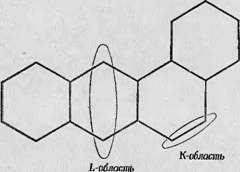
Представления А Пюльманда Б. Пюльмана [55] относительно того, какие ароматические углеводороды должны обладать кап! церогенной активностью и какие — нет, иллюстрирует фиг. 75, где обозначены два участка ароматической «олекулы — К-область и L-область. Согласно теории ПюльманаЛканцерогенньши свой ствами обладают такие молекулы, в которых имеется химически
|
Фиг. 75 К - и L-облаоти ароматических углеводородов. |
Активная К область (активная ароматическая связь)- iij отсутствует активная L-область (активные пара-Положения). Химическая активность этих двух участков может быть выражена количественно через «энергию локализации»*которая в свою очередь измеряет энергию ^активации химических реакций, протекающих на этих участках. Таким образом, эта теория получает прямое количественное обоснование. Установленные количественные соотношения позволяют объяснить, за очень небольшим исключением, канцерогенную активность (или инертность) всех исследованных полибензольных углеводородов
Истинное пороговое значение «энергии локализации» лучше всего выражать количественно в единицах обменного интеграла р (величины, получающейся прш расчетезЬаолекулярных орбита - лей). В теории Пюльмана утверждается, что необходимым условием. канцерогенности углеводорода является наличие в нем К-области с энергетическизк индексом менее 3,31 р. Если же в молекуле имеется еще и I-участок, то она будет канцерогенной лиш» в том случае, если индекс этого участка будет больше 5,66(5.
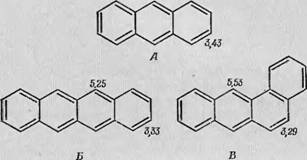
Типичный пример использования этой теории при рассмотрении ^'конкретных молекул' приведен на фиг. 76, где изображены различные производные антрацена. На фиг. 76,А представлена структурная формула самого антрацена и указаны соответствующие
значения активности К - и L-областей, выраженных через обменный интеграл. Можно видеть, что в молекуле антрацона индекс К-области больше чем 3,31, а индекс L-области меньше чем 5,66, поэтому эта молекула не канцерогенна. На фиг. 76,Б показана молекула нафтацена, образующаяся при линейном присоединении к молекуле антрацена одного добавочного бензольного кольца. В этой молекуле ни один из индексов для областей К и L также не удовлетворяет условию канцерогенной активности.
|
5,38
|
|
|
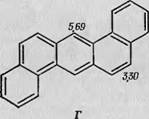
Фиг. 76. Энергетические индексы для различных углеводородов [55].
А — антрацен; Б — нафтацен; В — 1,2-бензантрацен; Г — 1,2,5,6-дибензантрацен;
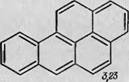
Д — 3,4-бепзпмрен.
Если, однако, добавочное кольцо присоединяется не линейно, а в боковое положение, как у 1,2-бензантрацена (фиг. 76,В), то индекс К -области становится меньше критической величины 3,31. Индекс L-области здесь возрастает, но не настолько, чтобы достигнуть критического значения 5,66, хотя очевидно, что добавление нового кольца в это положение способствует превращению молекулы в канцерогенную форму. Бензантрацен можно классифицировать как «пограничный канцероген».
|
|
Если в боковое положение добавляется второе бензольное кольцо (1,2,5,6-дибензантрацен; фиг. 76,Г), то индекс L-области увеличивается до 5,69, т. е. существенно превышает критическое
значение, а индекс К-области сохраняет еще значение ниже 3,31. Следовательно, в этой молекуле выполняются оба условия канцерогенное™; экспериментально обнаружено, что она действительно обладаетшчандепогенньшч свойствами. Нужно помнить, что в этой теории значение молекулярного орбитального обменного интеграла для L-области имеет смысл только при наличии такого участка в молекуле. В,,;этом отношении интересен случай, представленный на фиг. 76,Д где креходной молекуле антрацена присоединено еще одно добавочное бензольное Кольцо в таком положении, что L-участок полностью блокируется. Таким образом, это вещество (3,4-бензпирен) удовлетворяет первому условию, т. е. имеет очень активный К-участок, индекс которого существенно ниже 3,31, но совсем не имеет L-участка. Кз этого сльдует, что оно должно быть сильным канцерогеном; экспериментально показано, что это действительно так. Можно привести много подобных примеров, и почти всегда наблюдается хорошая корреляция между теорией и экспериментально наблюдаемой канцерогенно® активностью.
Следует подчеркнуть, что в этой теории измеряемые ^индексы относятся к обменным интегралам обычных молекулярных орби - талей спаренных электронов, а не орбиталей неспаренных электронов, как в стабильных радикалах (разд. 4.2). Таким образом, в этих молекулах совсем необязательно должны содержаться неспаренные электроны. Но в отсутствие неспаренных электронов они не будут парамагнитными и, следовательно, их нельзя будет обнаружить методом ЭПР. Большинство экспериментов с применением метода ЭПР [56, 68] действительно свидетельствует о том, что никакой закономерности в соотношении между содержанием неспаренных электронов в молекуле и ее. канцероген - ностью не существует.
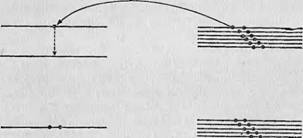
С другой стороны, были выдвинуты гипотезы, состоящие в том, что некоторые виды канцерогенной активности могут быть ^обусловлены более специфическими механизмами реакции, например переносом электрона 'или возбужденного состояния между ароматическими молекулами и биохимическими клеточными рецепторами. Так, согласно гипотезе Мэзона [57], .капцетюгышая активность проявляется в тех случаях, когда существует возможность электронных переходов с верхней'заполненной полосы системы энергетических уровней белка на один из незаполненных уровней связанного с ним углеводорода. Для того чтобы такой переход имел место, незаполненный уровень углеводорода должен соответствовать по энергии высшему заполненному уровню самого белка (фиг. 77). Предполагается, что в результате перехода электрона с белка на углеводород в системе энергетических полос белка появляется неспаренный электрон, который и обусловливает канцерогенную активность.
|
Белок |
Углеводород
Пустая полос а
Пустые уровни
Заполненная полоса
Высший
Заполненный
Уровень
Заполненная полоса А
|
Фиг. 77. Возникновение канцерогенной активности в результате переноса электрона между соответствующими энергетическими уровнями белка и углеводорода. А — до переноса электрона; Б — после переноса электрона. Объяснение см. в тексте. |
|
Б |
Таким образом, ключевым моментом в этой теории является соответствие двух систем энергетичесвдх уровней. Разница в энергии в системе энергетических полос белка'Измеряется величинами порядка от 1,10 до 1,18 единиц р (резонансный обменный интеграл в теории молекулярных орбиталей). Таким образом, для подтверждения правомерности этой теории существует простой и пря - моп^тест: нужно проверить, Имеется ли какая-либо определенная зависимость между канцерогенной активностью углеводородов и шириной запрещенных зон в их системах энергетических уровней. К сожалению, по этому вопросу существуют серьезные разногласия, и хотя сам Мэзон [57] утверждает, что получи®! экспериментальное подтверждение своей теории, другие авторы, например Пюльманы [58], показали, что такой связи не наблюдается.
Были предприняты попытки проверить эту теорию, используя другой критерий, а именно прчмые измерения ЭПР-поглощения [59] В этой серии экспериментов исследовались сами белки (в отсутствие углеводородов); их облучали ультрафиолетом различных длин волн, чтобы более прямым методом опредечить переходы между энергетическими уровнями белка. ЭПР^-йзмерения проводились не только с разными длинами вслн, но и при разной температуре; эти опыты показали, что при облучении ультрафиолетом, энергия которого соответствует критической величине запрещенной зоны, действительно возникают значительные концентрации неспаренных электронов. Вместе с тем стало ясно, что обнаруживаемые неспаренные электроны находятся не на самом высшем уровне, а попадают в ловушки на каких-то более низких уровнях, лежащих ниже основной полосы. Эти уровни, таким образом, можно рассматривать как аналоги примесных уровней в обычном неорганическом полупроводнике. Приведенные выше результаты ЭПР-измерений послужили убедительным доказательством правильности теории полупроводниковых проводящих полос в применении к белкам. Но поскольку ключевым моментом в теории М;;зона [57] являлась связь между канцерогенностью углеводородов и структурой их энергетических уровней, эти эксперименты с применением* ЭПР не смогли дать каких-либо определенных доказательств ни в пользу, ни против этой теории.
Другая теория, предложенная Бёрксом, [60], состоит в том, что злокачественный рост под действием сопряженных углеводородов обусловлен резонансным переходом энергии возбуждения с триптофана на канцерогенный углеводород с'последующим образованием специфического комплекса белок — канцероген. Таким образом, в этой теории предполагается, что механизм малигниза - ции основан на диполь-дипольном переносе энергии, а не на переносе самого электрона. Основны® параметром в теории Бёркса является, следовательно, значение интеграла перекрывания, соответствующего первому возбужденному сннглетному состоянию углеводорода. При экспериментальной проверке этой теории также возникли разногласия. Бёркс и его сотрудники [60, 61] утверждают, что существует отчетливая зависимость между канцерогенной активностью углеводородов и величиной их интеграла перекрывания, но, по мнению Пюльмана [62], на самом деле такой зависимости не наблюдается и, следовательно, эта теория не подтверждается экспериментально.
То обстоятельство, что теории Мэзона и Бёркса были поставлены под сомнение, вовсе не означает, что процесс переноса электрона не играет никакой роли в механизме канцерогенеза. Недавно Сент-Дьёрдьи с сотр. [63] показал, что многие канцерогены образуют с иодом комплексы с переносом заряда. Больше того, теоретические выкладки Пюльмана можно также интерпретировать с другой точки зрения, имея в виду распределение плотности заряда па молекуле канцерогена и, следовательно, способность канцерогена отдавать заряды на определенных участках своей молекулы. Следует также отметить, что были получены и некоторые положительные результаты по электронному парамагнитному резонансу. В ряде комплексов с переносом заряда, в том числе в комплексах с индолом и с иодом, наблюдались сигналы ЭПР. В частности, Элисон и Нэш [64] изучали комплексы, образованные различными капцерогенами (или соответствующими неканцерогенными молекулами) и тетрацианэтиленом, взятыми в экви - молярном соотношешш. Образцы помещались в стеклянные трубки в атмосфере азота, и трубки запаивались. Измерения проводились на.;100-кГц ЭПР-спектрометре при длине волны 3,2 см в условиях комнатной температуры. Полученные результаты приведены в табл. 2, где вещества расположены в порядке возрастания их донорной активности. При анализе этих результатов становится совершенно очевидным, что концентрация неспарен-
|
Таблица 2 Концентрации неспаренных электронов, измеренные методом ЭПР, ! в комплексах канцерогенов и родственных им неканцерогеииых соединений е тетрацианэтиленом [64]
|
Пых электронов, наблюдаемая в таких комплексах, возрастает пропорционально д опорной! активности исследуемых молекул,
В заключение следует заметить, что в настоящее время имеются веские доводы, как подтверждающие роль электронно-акцепторных и электронно-донорных взаимодействий в механизме канцерогенеза, так и опровергающие эту точку зрения. Но, каким бы пи был исход споров относительно механизма канцерогенеза, нет сомнения в том, что экспериментальные данные, полученные методом ЭПР, окажут очень большую помощь в установлении более определенных и точных фактов, ча которых могут быть основаны и проверены обе теории.