ПРОДУКТЫ СГОРАНИЯ ТОПЛИВА
ДЛя реШения технических задач, связанных с сжиганием топлива, неоШодимоГуметь-сводить материальные балансы по стехиометрическим уравнениям. Продуктами-полного сгорания топлИва является двуокись углерода—СОг, сернисТый газ БОз И ЭДдяиыеГ парыРШХ’’Кроме’ зрго, тоШбн^таМЖ проДуктов Сгорания Топлива являются азот ^содержавшийся в топливе и атмосферном воздухе, и избБ1Товдыи~1ислород Ог, Который содержится в продуктах сгорания топлива, потому процесс горения протекает не идеально и связан с необходимостью- подачи большего, чем теоретически необходимо, количества воздуха.
По уравнениям реакций окисления горючих элементов топлива, зная их молекулярную массу, плотность и объемы, можно найти массу и объем продуктов полного сгорания. Наиболее удобно проводить расчеты, исходя из значений массы молекул (молей), величины которых для горючих элементов топлива приведены в табл. 2-3.
При полном сгорании углерода образуется
С+02=С02; (2-11)
12,01 кг С+32,00 кг 02=44,01 кгС02
Или при сгорании
« л г 32 ■ /-V 44,61 рл
I КГ С-4- 12^01 кг 0»= 12701 КГ СО**
Чему соответствует
1 кгС+2,67 кг02=3,67 кгСОг. (2-12)
Для получения продуктов сгорания в объемных единицах разделим полученную массу на плотность каждого газа:
1 кгС + _ОТ°’==Т^С0*> или 1 кг С + 1.866 м* О, = 1,866 м* СО,,
(2-13)
Т. е. при сжигании 1 кг углерода требуется 1,866 м3 кислорода и образуется 1,866 м3 двуокиси углерода.
При неполном горении углерода таким же путем образуется:
С+-^=СО; (2-14)
12 кг С + 16 кг Ог = 28 кг СО; 1 кг С +1,33 кг О, =2,33 кг СО;
1 кгС+Т^°г==-ПЖС0; 1 кг С + 0,933 м*Ог= 1,866 м* СО, (2-15)
|
Молекулярная масса и плотность горючих
|
Т. е. при неполном сжигании 1 кг углерода в окись углерода требуется 0,938 м3 кислорода и образуется 1,866 м3 окиси углерода.
При горении серы аналогично получаем:
8+02=802; (2-16)
32,06 Кг 8 + 32,00 Кг 02 = 64,06 Кг Э02;
1 кгБ-р 1 кгО,=2 кгБ02;
1 Кгв-] ^428 О* = 2,858 ИЛИ
1 Кг 8 + 0,7 м* О,=0,7 м* 80*. (2-17)
Т. е. при полном сгорании 1 кг серы необходимо 0,70 м8 кислорода и образуется 0,70 м3 сернистого газа.
При окислении — горении водорода имеем:
2Нг+02=2Нг0; (2-18)
4,034 кгНг+32,00 кг 02=36,032 кгНгО;
1кг Н2+8кгОа=9 кг НЮ;
8^9
|
1 кгН2 + |
![]()
|
0,804 |
![]() Н20; 1 кгН2 + 5,6 м* 02 = 11,2 М*Н20, (2-19)
Н20; 1 кгН2 + 5,6 м* 02 = 11,2 М*Н20, (2-19)
Т. е. при полном сгорании 1 кг водорода требуется 5,60 м3 кислорода и образуется 11,20 м3 водяного пара.
Выполненные подсчеты позволяют перейти к определениЮ Теоретически - Крличества воздуха, помня о том, что
|
С Н-------- ~ В 1кг топлива содержится кг углерода, щт кг водорода, ^ кг серы |
10() ЮО 141
Летучей и имеется кг кислорода. В пересчете на рабочее топливо
Исходя из уравнений (2-11) — (2-19) суммарное количество необходимого, для горения кислорода, кг/кг, равно:
SHAPE \* MERGEFORMAT ![]()
|
Рр "100* |
|
(2-20) |
![]() Ог = 2,67^+1,00^ + 8 №
Ог = 2,67^+1,00^ + 8 №
100
Если вспомнить, что 1 м3 кислорода при нормальных условиях весит 1,428 кг, а в воздухе содержится по объему кислорода ^21 %, то, разделив каждый из коэффициентов в выражении (2-20) на величину 1,428*0,21-100^30, получим количество теоретически необходимого воздуха для сгорания 1 кг твердого или жидкого топлива, м3/кг:
|
(2-21) |
![]() 1/о _ о,0889Ср+0,265№+0,033 (вРп—Ор) .
1/о _ о,0889Ср+0,265№+0,033 (вРп—Ор) .
В случае сжигания газообразного топлива количество теоретически необходимого воздуха находят, исходя из стехиометрических уравнений
Таблица 2-3.
|
Элементов и продуктов сгорания топлив
|
Реакций горения компонентов газообразного топлива. При этом принимают, что объем одного моля компонентов, как и у идеальных газов, одинаков. Тогда при горении:
Окиси углерода
СО+0,502=С02; 1 м3СО + 0,5 м302=1 м3С02;
Водорода
Н2+0,5О2=НгО; 1 М3Н2+0,5 М302=1 М3Н20;
Сероводорода
Н28+1,502=Н20 + 502; 1 м3 Н25 +
+1,5 м302=1 м3Н20-Н м3БСЫ
Углеводородов
С„нт + (я+^-)о2-«со2+^- НА
1м3С„Нт+(я + -^) м80г=ям*-С02 + -|-м»Н20 и т. д.
Иначе говоря, исходя из реакций полного горения составляющих газообразного топлива, следует, что каждый 1 м3СО требует 0,5 м3 Ог и после реакции образуется 1 м*СОа.
Подобные рассуждения можно повторить и для всех других составляющих газообразного топлива и найти количество кислорода и воздуха, потребного для горения. Если помнить, что количество горючих газов в топливе выражено в процентах, потребное количество кислорода, м3/м3, будет:
0°, = 0,01 (0,5 СО + 0,5 Н2 + 1,5На8 + 2 (я -+ -£-) С„Нт - 02 и количество воздуха, м’/м3, составит:
V0 = 0,0476 (0,5 СО + 0,5Н2 +1,5 НД+ 2 (п + С„Нт - 02. (2-22)
Для полного сгорания топлива в топочные устройства подводят большее, чем теоретически необходимо, количество воздуха. Отношение действительно поступившего количества воздуха Уд к теоретически необходимому количеству V0 называют к о э Ф |ф и Цямтом бытка воздуха и обозначают через а:
А=Уд/У°. (2-23)
Величина коэффициента избытка воздуха для современных топочных устройств колеблется от 1,02 до 1,45—1,70.
Азот N2, вводимый с воздухом в топочное устройство, не участвует в процессе горения топлива, но при высоких температурах, близких к температуре горения топлива и температуре газов на выходе из топочной камеры, и при определенных соотношениях Ыг/Ог дает весьма ток - сичные окислы азота, вредно действующие «на биосферу. Если пренебречь в первом приближении образованием окислов азота, то можно написать следующее отношение:
|
|
Содержание азота Ы2 в воздухе, поступившем в топочную камеру, можно представить как сумму Ы2=№2 + Ы*, где №г — теоретическое, а Ы* — избыточное количество азота, выраженное в процентах.
Тогда коэффициент избытка воздуха можно представить как
(2-25)
Выражая величину содержания азота в полном количестве воздуха через количество избыточного кислорода, получаем:
02 21 79 ~
——=-^г и соответственно N =^02.
К« 79 2 21 2
Тогда коэффициент избытка воздуха, поступающего в топочное устройство, будет:
А =------- =--------------- ^-о-. (2-26)
N,--21-0, 21—79 N7
При полном сгорании топлива состав сухих дымовых газов (без водяных паров) можно определить по уравнению
100 % =С02+ БОгЧ - О2+N2 или 100 % =
=И02+ 02+N2, откуда
N2=100—(И02+02) где Н02=С02 + 502.
Подставляя в выражение (2-26) величину N2 = 100—< (И02 + 02), получаем уравнение следующего вида:
21
(2-27)
О
2
|
100—(И02 + 02) |
![]() 21 — 79 ■
21 — 79 ■
Содержание С02, Э02 и Ы2 в сухих продуктах сгорания выражают в процентах и определяют с помощью газоанализаторов. Анализ состава продуктов сгорания в газоанализаторах волюмометрического типа основан на последовательном контакте дымовых газов с реактивами, в результате которого поглощаются двуокись углерода, сернистый газ, кислород. Водород и другие горючие газы и менее точно окись углерода определяют методом дожигания. Горючие газы могут находиться в дымовых газах лишь при неполном сгорании топлива, и содержание их целесообразно находить с помощью приборов, дающих более точные и быстрые результаты. К ним в первую очередь следует отнести хроматограф.
В хроматографе производится разделение газовой смеси на компоненты путем ее пропуска вместе с г азом-носителем через колонку, заполненную твердым адсорбентом. Вводя периодически анализируемую смесь газов в поток газоносителя, можно вследствие разных изотерм адсорбции при контактировании с адсорбентом получить разделение смеси на составляющие. При пропускании газа-носителя с отделенной частью смеси через детектор можно найти процентное содержание окиси углерода, метана, водорода, обычно входящих в состав продуктов неполного горения.
Если в продуктах неполного сгорания содержится в основном окись углерода СО, то состав сухих дымовых газов будет: 100=Ы2 + И02+! + О2+СО. При замене СО потребным для его полного сгорания кисло - 4* 51
Родом, равным 0,500, можно получить следующее выражение для определения содержания азота в полном количестве воздуха, поступающего в топочное устройство: Ыг=100—(ИОг+Ог—0,5СО).
Выражение для определения коэффициента избытка воздуха при наличии в дымовых газах СО будет:
А = Ог—О. бСО 79 0,-0,5СР <2‘28)
Г1 ~~ 'у 2 1 21 100 — (<*02 + 02 + СО
При наличии в продуктах сгорания, кроме окиси углерода, водорода, метана и других тяжелых углеводородов, что может иметь место при неполном сжигании природного или нефтепромыслового газа, жидких и твердых топлив, если знать их содержание в процентах, расчетное выражение для определения избытка воздуха принимает вид:
1
(2-29)
79 О* — 0,5 (СО + Н8) — 2СН4
1 — 21 №
N. - 0,431 - р - - 0*0., + СО + СН4)
Где СО, Нг, СН4 — их содержание в процентах, а /(Р=СР+0,3758РЛ, ®/0.
При полном сгорании топлива дымовые газы содержат лишь продукты полного окисления горючих элементов топлива — углерода, водорода и серы — С02, НгО и БОг; азот топлива и внесенный с воздухом N2; неисцользованный при горении кислород воздуха Ог; водяной пар НгО, полученный за счет окисления водорода топлива, испарения влаги, содержащейся в топливе, и внесенный с влажным воздухом. При паровом распыливании жидкого топлива также вносится некоторое количество НгО в продукты сгорания.
Полный объем продуктов сгорания твердого и жидкого топлива при - коэффициенте избытка воздуха, большем единицы, (м3/кг), будет состоять из перечисленных слагаемых:
+ + ^ + (2-30)
Продукты сгорания (м3/кг) принято подразделять на сухие газы и водяные пары:
Так как в приборах волюмометрического типа, с помощью которых определяют состав дымовых газов до анализа, конденсируются водяные пары, а содержание трехатомных газов С02+502=Н02 дается совместно.
При полном сгорании 1кг углерода 'образуется 1,866 м* СО, 1СМ. стр. 48, 49), а 1 кг серы—0,7 м* БО,. В 1 кг рабочего топлива содержится углерода
Щ и серы щ кг, что дает при сгорании топлива следующий объем трех - атомных газов, м*/кг:
>,но.=1,со1+1'8о.=;1.866^+0,7^=1.866 (2.3|)
При сжигании топлива с теоретически необходимым количеством воздуха (а=1) содержание кислорода в сухих дымовых газах будет равно нулю, их объем — минимальным или теоретическим и будет состоять из объема трехатомных газов и азота — из объемов азота, содержащегося в топливе, и азота, внесенного с воздухом.
.52 '
Объем азота, содержащегося в топливе, м3/кг, равен:
Мт — !__ о 008ЫР
^ * 100 1,251 ’ ^ •
Объем азота,- внесенного с воздухом, в котором содержание азота по объему равно 79%, м3/кг:
, Ы2=0,79У°+0,008№. | (2-32)
Обычно последним слагаемым в выражении (2-32) можно пренебречь и считать, что
УК2=0,791Л>. (2-33)
При этих допущениях теоретический объем сухих газов, полученных от сгорания 1 кг твердого или жидкого топлива, м3/кг, составит:
У°с-Г=УЯОг +УМ§ = 0,0187 (СР+0,3755РЛ) + 0,79Г. (2-34)
Полный объем сухих газов будет больше теоретического на количество избыточного воздуха (а—1) V0, м3/кг. Следовательно, полный объем сухих дымовых газов, м3/кг, равен:
^с. г =^°с. г + (« — 1) У°=0,0187 (Ср+0,375БРЛ) + 0,791/°+ (а - 1) Vе, или
Ус. г = 0,0187/Ср+0,79У’+(а - )У°, (2-35)
Где
= Ср+0,3758рл.
При сжигании топлив в продуктах сгорания, кроме сухих газов, содержатся и водяные пары, их количество, полученное в результате окисления водорода топлива, м3/кг, составит:
V1------------ —__ _9№_ о ц щр
Н, о 100-0,804 80,4 •
В формуле:
9 — количество воды, полученной при окислении 1 кг водорода, кг;
0,804 — плотность 1 кг водяных паров при нормальных условиях, кг/м3 (см. табл. 2-3).
Количество водяных паров, полученных от испарения влаги топлива, м3/кг, составляет:
У, г — Ц7Р __ ГС7” _в 0124$ф
Н*о Ю0-0.804-'80,4
Количество влаги, содержащейся в воздухе, принимают равным 10 г на 1 кг воздуха. При а=1 количество водяных паров, м3/кг, будет равно:
Т/П1 __ <^,°Рвзд ___ 10-1,293 |^0___ о П1й11/°
Нао 100-0,804 804 — и’и1и** •
Количество влаги, вносимой в топку в виде водяных паров (например, для распыливания жидкого топлива), при расходе, кг/кг, топлива определяет дополнительный объем водяных паров, м3/кг:
Полный теоретический объем водяных паров в дымовых газах от сжигания 1 кг твердого или жидкого топлива, м3/кг, является суммой указанных величин и равен:
|
(2-36) |
![]() 1Г°На0 = 0,111 Нр + 0,016IV0 + 0,01241Гр + 1,241Гф.
1Г°На0 = 0,111 Нр + 0,016IV0 + 0,01241Гр + 1,241Гф.
Действительный объем водяных паров в дымовых газах будет больше только за счет влаги, внесенной с избыточным воздухом. Представляя выражение (2-36) в виде ^н, о=^н, о +0,0161 V0, получим, что действительное количество водянцх паров в дымовых газах при сжигании твердого или жидкого топлива, м3/кг, составит:
|
(2-37) |
Выше расчеты объемов воздуха и дымовых газов велись на 1 кг топлива. Иногда целесообразно определять, какое количество углерода следует сжечь для получения 1 м3 двуокиси углерода. Возвращаясь к выражению (2-13), можно видеть, что для получения 1 м3 двуокиси
Углерода требуется =0,536 кг углерода; тогда
|
Срт, Ср2 Ср : 53,6 *53,6 53,6* |
|
Се, |
|
СР |
|
V — |
|
Соа—Ю0.0,536 ““53,6 При неполном горении 1 кг топлива, когда часть углерода образует лишь окись углерода, по выражению (2-15) также получается |
|
СР Со 53,6 |
|
1,866 м3СО, т. е. V |
|
М3/кг. |
|
0,3758рл |
|
53,6 |
 |
|
|
|
|
|
|
|
|
|
|
|
|
(2-39) |
![]() При неполном горении объем сухих газов, м8/кг, будет: ^со. + ^со+^с,= °,+ 0-3га5Р--'(Р
При неполном горении объем сухих газов, м8/кг, будет: ^со. + ^со+^с,= °,+ 0-3га5Р--'(Р
|
53,6 |
![]() 53,6е
53,6е
Далее можно подсчитать содержание в объемных процентах каждого из рассматриваемых выше (компонентов >в сухих газах:
|
100 и т. д. |
|
С. Г Кр |
|
Можно написать: |
|
Со 53,6' КР |
|
53,6 део2 + СО) |
|
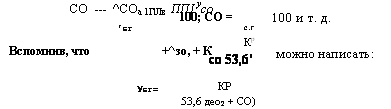
100; СО = Г с. г Вспомнив, что +^зо, + К Ус. г= |
|
СО ---- ^СОа 1Г|Лв ППІ усо |
 |
|
|
|
И С02-(-802 = Шг. При неполном горении топлива
Ш2+со=-7с°.+У8°>+1/со . юо.
•'с. г
При полном горении 60 = 0 и Ус г= 53^0 • (2-41)
На работающем котлоагрегате величина ИОг в процентах определяется с помощью газоанализатора. Если бы горючими в топливе были только углерод и сера, а кислород в топливе не содержался, то при полном сгорании указанного топлива с коэффициентом избытка воздуха а=1 процентное содержание трехатомных газов составило бы примерно 21 %, т. е.
1?02=-^-100^21«/в.
У с. г
При количестве кислорода в топливе, достаточном для окисле-
О*3
Ния всего водорода топлива, т. е. - д-= Нр и при|а = 1 получается,
О?
Что ЕОг£=210/в. Но так как Нр—8“>-0, то обычно К02<21%. Отсюда
Видно, что для каждого топлива в зависимости от его элементарного сбстава можно подсчитать максл мальное количество трехатомных газов ГО!?акс, образующихся при полном сгорании данного топлива. Пренебрегая очень малой величиной содержания азота в топливе, величину КО“3*0 для ’твердых и жидких топлив, ®/,, можно определить из следующей формулы:
И°Г= 2.37НР-0.1260Р- (2-42)
СР + 0,375БРл
О, о НР —0.1260Р
Входящую в формулу величину 2,37 ■ -ф 0 375§рд » зависящую только
От состава топлива, принято обозначать через р. Тогда
Шгс=ттт • (2'43)
Значение р для большинства твердых топлив лежит в пределах от 0,035 до 0,150; для сланцев и мазута, содержащих много водорода,—
От 0,20 до 0,35. Для характерных топлив величина р приведена
В табл. 2-4.
|
Таблица 2-4 Величины Р И Доз““ для некоторых топлив
|
Знание значения величины {?0^*кс позволяет при испытаниях определить ориентировочное значение а при полном сгорании топлива, так как
Ц0макс
, (2-44) '
Полный объем продуктов сгорания твердого и жидкого топлива, м3/кг, может быть определен из выражения
Уг=УС'Т + УН10 = 0,0187Кр + 0,79У° + V0 (а - 1) +
* + (2-45>
Состав продуктов сгорания газообразного топлива может быть найден исходя из тех же соображений, что были использованы ранее для определения V0. Пользуясь уравнениями горения для составляющих газообразного топлива, можно написать, что объем трехатомных газов,. м3/м3, будет:
Уко>=0,01 (СО, + СО + НгЗ + СН4),
Что справедливо при условии, что суммарное содержание в топливе этана, пропана и бутана меньше 3% объема и что газ состоит в основном, лишь из метана.
Объем азота в продуктах сгорания
У°Ы5=0,79У°+0,0Шр
И сухих газов
У°о,=Упо,+[1]°^ (2-46>
Теоретический объем водяных паров в продуктах сгорания газа У°н,0 = 0’01 (Нг + Н,8 + 2 4- С„Нт + 0,1244г, Т)+0,0161 У. (2-47>
Где С? г.т — Влажность газообразного топлива, г/м3.
Суммарный теоретический объем продуктов сгорания топлива, м3/м3:
V г = ^с. г Н-^н, о=^о, Н“УМ,+Ун,0. (2-48)
В том случае, если из анализа дымовых газов известно содержание в продуктах сгорания СОг, СО и СН4, объем сухих газов, м3/м3, составит:
Изложенные формулы позволяют определять количество воздуха, потребного для горения, и объемы дымовых газов при известном избытке воздуха. Избыток воздуха при расчете выбирается на основе опытных данных (табл. 2-5), в зависимости от типа горелок и топочного устройства, элементов котельного агрегата и установки.
Таблица 2-5
Значения коэффициента избытка воздуха в топке
Избытки воздуха в топке ат для топлива
|
^Наименование топочного устройства |
|
Антрацитов и полуан - трацитов |
|
Газооб Разного |
|
Бурых Углей |
|
Дре Весины |
|
Слан Цев |
|
Каменных Углей |
|
Торфа |
|
Жидкого |
|
'1*0, |
|
Топка с цепной решеткой........................... То же и шахтой для топлива. . . То же и пневматическим забрасывателем топлива........................................................... То же с пневмомеханическим забрасывателем и обратным ходом Топка с наклонно переталкивающими колосниками.................................................. Камерные топки с твердым удалением шлака........................................................... То же с жидким удалением шлака Камерные тонки для мазута и других жидких топлив............................................... То же для природного р нефтепромыслового газа........................................... |
|
1,5—1,6 |
|
1.3- 1,4 1.3— 1,4 |
|
1.3— 1,4 1.3— 1,4 |
|
1,4 1,2 |
|
1,25 1,2 |
|
1,2 1,2 |
|
1,2 1.2 |
|
Н, о |
|
И Рн>о = |
|
V, |
|
Н, о |
|
І? о, |
|
Гяо,—‘ выше |
|
'Ц, о— Уг |
|
При указанных (кгс/м2), будут: |
|
Условиях парциальные |
|
1,02—1,10 |
|
1.Ю |
|
1,25 |
|
1,2 |
|
Неподвижная решетка с ручным Забросом топлива....................................... Неподвижная решетка с пневмоме - . ханическим забросом топлива. . Шахтная топка с наклонной решеткой......................................................................... . Топка с зажатым слоем топлива (скоростная топка В. В. Померанцева) .. |
|
1,30—1,35 1,6—1,7 |
|
1.3— 1,5 1.4— 1,5 |
|
1.3— 1,4 1.4— 1,5 |
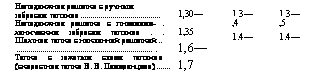 |
|
|
|
|
|
|
|
 |
|
|
|
|
|
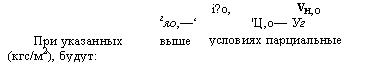 |
|
|
Таблица 2-5а
Присосы воздуха в топках, газоходах и других частях котельной установки»
|
Наименование |
![]() Работающей под разрежением
Работающей под разрежением
Величина присоса воздуха
|
0,10 0,05 0,03 0,05 0,10 0,03 0,10 0,08 ,02 на каждую ступень 0,2 То же 0,1 . 0,07 . 0,03 . 0,15 , 0,05 . 0,10 0,01 0,05 0,05 |
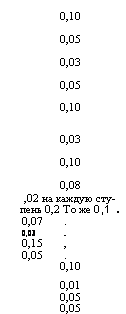 Слоевые и камерные топки без гидравлического уплотнения шлаковой шахты Камерные топки для газа и мазута и для твердого топлива с гидравлическим уплотнением шахты Камерные топки с металлической обшивкой (для всех топлив) и циклонные топки Первый пучок котельных труб котлоагрегатов с 0^9,31 МВт (8 Гкал/ч) или 3,3 кг/с (12 т/ч)
Слоевые и камерные топки без гидравлического уплотнения шлаковой шахты Камерные топки для газа и мазута и для твердого топлива с гидравлическим уплотнением шахты Камерные топки с металлической обшивкой (для всех топлив) и циклонные топки Первый пучок котельных труб котлоагрегатов с 0^9,31 МВт (8 Гкал/ч) или 3,3 кг/с (12 т/ч)
Второй пучок котельных труб котлоагрегатов с <3<;9,31 МВт (8 Гкал/ч) или 3,3 кг/с (12 т/ч)
Г азоходы:
В перегревателе за топкой, в опускной шахте и переходной зоне
Водяного экономайзера чугунного водяного экономайзера стального для котлоагрегатов с С < 9,31 МВт (8 Гкал/ч) или
3.3 кг/с (12 т/ч)
Для котлоагрегатов с С >9,31 МВт (8 Гкал/ч) или
3.3 кг/с (12 т/ч)
Воздухоподогревателя чугунного из ребристых плит то же из ребристых труб воздухоподогревателя стального пластинчатого я „ трубчатого
Регенеративного воздухоподогревателя Золоуловитель батарейный, жалюзийный, циклон, скруббер Золоуловитель-электрофильтр Газоход длиной Юм: стальной
Из кирпичных боровов Пылеприготовительная система с молотковыми мельницами л мельницами - вентиляторами
Кроме объемов, в ряде случаев при сжигании твердых и жидких топлив бывает необходимым знание массы дымовых газов топлива, кг/кг, которую можно определить из следующего выражения:
|
(2-52) (2-53) |
![]() Ог = 1- 0,01Лр+ 1,308а1/0 + ф
Ог = 1- 0,01Лр+ 1,308а1/0 + ф
Для газообразного топлива, кг/м3, из формулы
(5г = рсг. т + °>00Ыг. т+Ь306аУ°,
Где Рсг. т — плотность сухого газа, а С1Г, т — содержание влаги в топливе, кг/м3.
Часто необходимо знать концентрацию золы в дымовых газах, г/м3 или кг/м3:
10
|
(2-54) |
![]()
|
Или |Л.= |
![]() Уи
Уи
Где аУн — доля золы топлива, уносимая дымовыми газами.
Результаты расчета по приведенным формулам и выражениям Для Их последующего применения целесообразно сводить в табл. 2-6.
|
Таблица 2-6 Объемы 'газов, их доли и концентрации золы по газоходам
|