Характеристика и способы производства важнейших носителей
Катализаторы могут быть изготовлены как на носителях с малой удельной площадью поверхности (диатомит, пемза, асбест), так и с высокоразвитой поверхностью (y-A1203, MgO, сили - кагель, глины, алюмосиликаты) [123].
Рассмотрим некоторые наиболее часто используемые в промышленности носители.
Пемза [44, 124]. Природный материал, пористая разновидность вулканического стекла. Представляет собой смесь силикатов натрия, калия, кальция, алюминия, магния, железа и имеет следующий состав, % (масс.):
Si02 60—70 СаО 2—3
А1203 15—20 Fe203 1—3
К20 + Na20 3—4
Пористость1?. 60 %, удельная площадь поверхности 10 м2/г.
Перед использованием из пемзы кислотами удаляют примеси железа и алюминия. Пемза (крупные частицы размером 2—8 мм) является непрочным, легким носителем.
Асбест — группа минералов, имеющих волокнистое строение [123, 124]. По химическому составу асбестовые минералы представляют собой различные водные силикаты магния, железа, кальция и натрия.
Малогидратированный (голубой) асбест обладает высокой жаропрочностью, легко подвергается обработке, устойчив к химическим воздействиям, имеет развитую поверхность (до 150 м2/г). Перед пропиткой его очищают от нежелательных примесей растворами кислот. Асбест применяют сравнительно редко в качестве носителя тонкодисперсных металлов.
Диатомит (кизельгур, инфузорная земля) — горная порода, состоящая преимущественно из панцирей диатомовых водорослей
[125], что обеспечивает носителю большую пористость и легкость. Состав, % (масс.):
TOC \o "1-3" \h \z Si02 70—90
Fe203 2—10
CaO + MgO 4
Пористость 50—80 %, удельная площадь поверхности 10— 50 м2/г.
Диатомит механически не прочен, используется в виде крупных зерен.
Металлокерамика [126] — спрессованные микросферические шарики металла с высокой теплопроводностью. Регулируемая пористая структура зависит от размера исходных микрошариков и давления прессования. Пористость ее — до 40 %, поверхность невелика. Основной недостаток — трудно наносить на нее активные соединения. Однако ввиду большой прочности металлокерамика может быть использована для катализаторов кипящего слоя.
Активный уголь (АУ) [127]. Применение АУ в различных отраслях промышленности в качестве сорбентов, катализаторов, носителей обусловлено их высокой пористостью (около 60—70 %), значительной электрической проводимостью и химической природой поверхности. Технический АУ содержит в зависимости от исходного сырья и условий приготовления 88—98 % углерода.
Активные угли, выпускаемые промышленностью, в зависимости от областей их применения делят на три основные группы: 1) осветляющие; 2) рекуперационные; 3) угли газового типа. Наибольшее применение в качестве катализаторов и носителей нашли угли третьей группы. Ниже приведены основные марки и характеристики этих углей (табл. 3.2).
|
129 |
В общем случае угли обладают мультидисперсной пористой структурой, имеющиеся в ней разновидности пор образуют единую древовидную систему [128]. Их готовят из различного вида органического сырья: твердого топлива различной степени метаморфизма (торф, антрацит, бурый и каменный уголь), древесины,
|
Таблица 3.2 Параметры пористой структуры активных углей газового типа
|
|
АГ-2 |
0,60 |
0,60 |
0,30 |
0,05 |
0,25 |
33 |
|
Скт |
0,42 |
0,98 |
0,51 |
0,20 |
0,27 |
108 |
|
СКТ-2Б |
0,49 |
0,75 |
0,45 |
0,09 |
0,21 |
60 |
|
КАД-иодный |
0,38 |
1,00 |
0,34 |
0,15 |
0,51 |
110 |
|
БАУ |
0,26 |
1,50 |
0,23 |
0,08 |
1,19 |
57 |
|
9 П/р И. П. Мухленова |
|
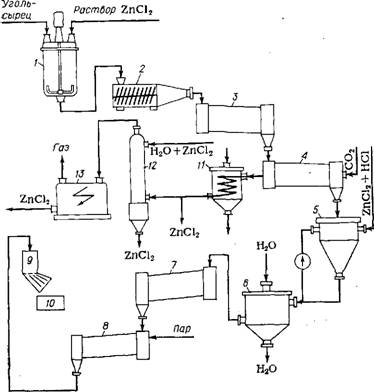
Рис. 3.13. Схема производства ЛУ хлорцинковой активации: 1 — смеситель твердой и жидкой фаз; 2 — формовочная машина; 3, 7 — сушильные печн; 4, 8 — печи для активации; 5 — экстрактор; 6 — промывочный чан; 9 — классификатор; 10 — тара; 11 — конденсатор; 12 — абсорбционная колонна; 13 — электрофильтр |
Отходов кожевенной промышленности, скорлупы орехов, костей и др.
Вначале получают уголь-сырец термообработкой сырья без доступа воздуха. Далее уголь-сырец активируют водяным паром, диоксидом углерода и некоторыми другими соединениями (карбонатами, сульфатами, хлоридом цинка). Активацию диоксидом углерода ведут при температурах около 900 °С. При этом часть углерода выгорает: С + С02 = 2СО. Долю угля, выгоревшего при активации, называют «степенью обгара». Наиболее часто в качестве носителя активной составляющей используют гранулированный уголь хлорцинковой активации, получающийся по следующей схеме (рис. 3.13) [127]. Раствор ZnCl2 плотностью 1,8 г/см3 и пылевидный уголь-сырец перемешивают в течение 3 ч при 90 °С в смесителе 1, следя, чтобы отношение массы безводного активатора к массе сухого исходного углеродистого материала '(коэффициент пропитки) лежало в пределах 1,0-=-1,4.
Пластичную пасту после охлаждения формуют методом экструзии в формовочной машине 2. Полученные цилиндрические гранулы (размер которых может колебаться от 2 до 6 мм) сушат при 180 °С во вращающейся печи 3. Далее уголь активируют во вращающейся печи 4 при 600—700 °С в противотоке с бескислородным газом. Отходящие газы содержат пары и аэрозоль ZnCl2, которые частично рекуперируют после охлаждения газа. Доля увлекаемого с газами хлорида цинка составляет 30—60 % от исходного количества. Для увеличения степени улавливания соли после конденсатора И устанавливают абсорбционные колонны 12, орошаемые разбавленным раствором ZnCl2, и электрофильтры 13.
Насыщенный хлоридом цинка уголь поступает в вертикальный экстрактор 5, через который циркулирует разбавленный раствор ZnCl2, подкисленный НС1. В нижней части аппарата остаток соли вымывают горячей соляной кислотой. Рекуперированный ZnCl2 возвращают в процесс. Экстракция продолжается несколько часов, далее уголь промывают водой в аппарате 6 до требуемой кислотности промывных вод. Отмытые гранулы сушат во вращающейся печи 7 и подвергают дополнительной активации водяным паром в печи 8. В процессе активации из угля удаляются остатки соляной кислоты. Продукт рассеивают по фракциям на классификаторе 9 и загружают в тару 10.
Силикагель [129] — аморфный оксид кремния, характеризуется высокой устойчивостью структуры, возможностью в широких пределах регулировать пористую структуру, негорючестью. Наибольшее применение как носители получили: силикагель и высокодисперсные порошки — аэросилы или белая сажа.
По химической природе это слабые кислоты. Гель построен из тетраэдров (Si04), образующих непрерывную трехмерную сетку, в которой каждый атом кремния связан с четырьмя атомами кислорода, каждый атом кислорода — с двумя атомами кремния [129 ].
Превращения геля протекают по механизму поликонденсации: nSi (ОН)4—Sin02n_m и (2п—т) Н20. Поликонденсация приводит к образованию частиц коллоидных размеров (2—20 нм) сферической формы. При высушивании гидрогель сохраняет структурную сетку из связанных между собою сферических частиц. С увеличением числа частиц и возникновением прочных связей между ними образуется жесткий кремнекислородный каркас. Поры представляют промежутки между частицами, размер пор и их объем определяется размером частиц и плотностью их упаковки [127].
Формирование структуры силикагеля идет по такой схеме. Первичные частицы золя размером примерно 4 нм защищены ион - носольватной оболочкой, препятствующей их слиянию в более крупные агрегаты. Для образования концентрированного и стабильного золя достаточно наличия одного-четырех ионов натрия на 10 нм3 первичных частиц. В таком золе происходит только переконденсация, приводящая к выравниванию размеров глобул за счет исчезновения более мелких. Защитное действие ионно-
сольватной оболочки продолжается до конечной стадии сушки геля.
В процессе сушки под действием капиллярных сил идет принудительное сближение глобул. Соприкосновение глобул приводит к образованию мест с мениском отрицательной кривизны и резко пониженной растворимостью кремниевой кислоты. Идет перемещение кремниевой кислоты с более выпуклых частей поверхности глобул под действием оставшейся воды, ионов натрия и повышенной температуры. Варьируя воздействие этих факторов, можно изменить размер частиц, образующих структуру конечного геля, а следовательно, и его поверхность.
Таким образом, ионы натрия оказывают двойственное влияние на поверхность силикагеля: сначала натрий повышает защитное действие гидратной оболочки и предотвращает слияние первичных глобул, в условиях же сушки после разрушения гидратных оболочек — повышает растворимость кремниевой кислоты и ускоряет рост размеров глобул в результате их слияния.
Адсорбционные и химические свойства силикагеля в значительной степени определяются группами =Si—ОН. Группы ОН" занимают в основном вершины тетраэдров, выходящие на поверхность скелета силикагеля.
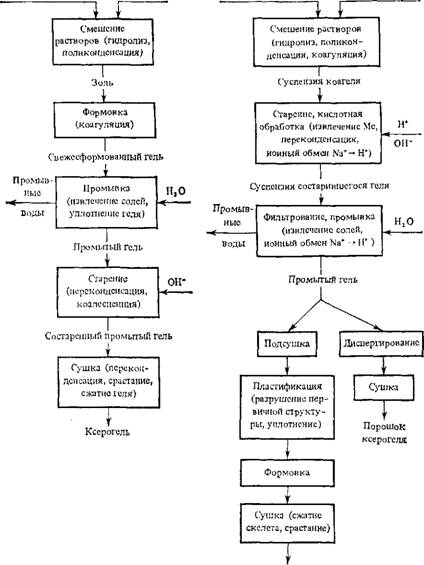
Силикагель получают взаимодействием щелочного силиката с кислотами и кислыми солями, гидролизом четыреххлористого кремния и другими методами [130]. На рис. 3.14 представлены принципиальные варианты получения силикагеля.
Согласно 1-у варианту полученный при взаимодействии исходных составляющих золь кремниевой кислоты коагулирует, образуя студень, т. е. во всем объеме геля защемляется вся жидкость исходных растворов. Это дает возможность осуществить формовку крупных сферических гранул, совмещая ее с коагуляцией путем дробления струи золя на крупные капли. Такой метод не требует сложного оборудования для формовки, промывки и старения геля.
Во 2-м варианте в качестве коагулятора используют не только кислоту, но и соли сильной кислоты и слабого основания или другие коагуляторы. Это приводит к увеличению скорости коагуляции, выпадению кремниевой кислоты в виде рыхлого аморфного осадка, образующего подвижную суспензию, легко разделяемую фильтрованием. После сушки получают ксерогель в виде порошка или рыхлых непрочных кусочков. Для получения гранул требуются пластификация и формовка.
На пористую структуру силикагелей влияют:
1) рН при получении и промывке гидрогеля. Увеличением рН от 2 до 8 изменяют удельную площадь поверхности геля от 800 до 350 м2/г при одновременном изменении объема пор от 0,3 до 0,8 см3/г;
2) изменение глубины старения геля, полученного в нейтральной среде, при помощи стабилизирующих агентов;
Вариант 1 Вариант 2
|
Раствор кислоты, Раствор Na; О ■ jiSiO, Кислота Раствор Na20-/iSi02 соли, коагулятор
КсерогсЛЬ Рис. 3.14. Принципиальные варианты получения силикагеля |
3) пропитка гидрогеля перед сушкой минеральными кислотами-
4) замена интермицеллярной воды органическими жидкостями;.
5) гидротермальная обработка гидрогеля кремниевой кислоты в автоклаве при разных температурах;
6) прокалка ксерогеля при высоких температурах в присутствии водяных паров или минерализаторов [129].
Оксиды алюминия [131J. а-А1203 — корунд, наиболее устойчивая форма оксида алюминия, содержащая примерно 99 % А1203 и небольшое количество примесей оксидов титана и кремния. а-А1203 получают обжигом гидроксида алюминия при температурах до 1200 °С. При нагревании вплоть до температуры плавления (свыше 2000 °С) он не подвергается никаким превращениям. Корунд — механически прочный теплопроводный носитель, стоек к воздействию кислот и щелочей. Пористость его колеблется от 5 до 25 %; удельная площадь поверхности невелика (около 1 м2/г).
Активный оксид алюминия (y-A1203) нашел широкое применение в таких процессах нефтепереработки, как риформинг, гидроочистка, гидрокрекинг, где используют катализаторы, содержащие до 80—99 % 7"А1203 [2]. Его получают прокаливанием гидроксида алюминия в тригидратной (гиббсита, байерита, нордстран - дита) или в моногидратной (диаспора, окристаллизованного бе - мита и псевдобемита) форме. Поверхность, объем и размер пор - получающегося оксида зависят от кристаллической модификации исходного гидроксида, остаточного содержания в нем воды, наличия оксидов щелочных и щелочноземельных металлов, а также от условий термической обработки.
По прочности 7"А1203 уступает корунду, но является более пористым материалом: объем пор составляет 50—70 %, удельная площадь поверхности — 120—150 м2/г. Все технологические схемы производства y-A1203 основаны на получении А1 (ОН)а переосаждением глинозема. Сущность процесса переосаждения заключается в растворении глинозема в кислоте (H2S04 или HN03) или щелочи с последующим гидролизом при нейтрализации соответственно основанием или кислотой. Так, процесс переосаждения через среднюю соль идет по реакциям:
2А1 (ОН)3 + 3H2S04 ^ Al2 (S04)3 + 6НаО, Al2 (S04)3 + 6NaOH 2А1 (ОН)3 + 3Na2SO«.
Выпадающий осадок имеет псевдобемитную структуру. Процесс переосаждения связан с большими затратами кислот или оснований (2—4 т на 1 т оксида алюминия), которые практически невозможно регенерировать. Осадок отфильтровывают и промывают. Формовка влажной пасты приводит к получению малопрочных гранул. Поэтому пасту предварительно высушивают, измельчают и таблетируют.
При щелочном способе приготовления 7"А1203 иногда получают две его модификации раздельным осаждением при разных температурах: «холодное» осаждение при 20—25 °С, «горячее» — при температурах до 100 °С. Далее эти модификации смешивают. Осаждение проводят при рН = 9,3^-9,5. При этом образуются хорошо отмывающиеся и отфильтровывающиеся осадки, обеспечивающие получение таблеток высокой механической прочности с насыпной плотностью 0,5—0,65 г/см3.
Разработана технология y-A1203 в виде гранул сфероидальной формы [127]. В этом случае отмытый от примесей осадок псевдо - ■бемита пластифицируют азотной или соляной кислотой, взятой в количестве 0,15—0,2 моль на 1 моль А1203. Суть пластификации заключается в разрыве жестких полимерных нитей трехмерной структуры псевдобемита на короткие участки, свободно перемещающиеся друг относительно друга. Введение кислоты приводит к замещению гидроксильных групп, ответственных за ориентацию и сочленение звеньев полимерной цепи.
Образуется однородная пластичная и подвижная суспензия, которую подают на формующую головку с фильерами, выполненную из оргстекла. Пройдя через фильеры, суспензия свободно падает в колонну, верхняя часть которой заполнена керосином. Образовавшиеся шарики собираются в нижней части колонны, заполненной аммиаком, где происходит нейтрализация основной соли алюминия и закрепление полимерной структуры 1132]. В грануле остается некотороеколичествохлоридаалюминия (примерно0,2моль на 1 моль А1203), который удаляется в процессе прокаливания.
Сфероидальный y-A1203 содержит в качестве примесей, % (масс.): Na20 — 0,1—0,6; Si02 — 0,1—1,0; Fe203 — 0,1—1,0. Средний диаметр гранул составляет 3—4 мм, насыпная плотность— 0,6—0,9 г/см3, общая пористость — 0,4—0,7 см3/г, преобладающий радиус пор — 3—4 нм.
Пористый корунд. Полиморфное превращение у-А1203 в а-А1203 осуществляется обычно при температуре более 1100 °С. по схеме: 7"А1203 -»- 0-А12О3 а-А1203 [133] — и сопровождается ростом размеров первичных частиц с 3—9 нм для у-А1203 до примерно 70 нм для а-А1203. Применяя минерализаторы, сдвигают процесс формирования а-А1203 в область более низких температур. Минерализаторами могут быть оксиды хрома, молибдена, железа, азотная и плавиковая кислоты.
Изменение фазового состава, удельной площади поверхности, пористой структуры и прочности оксида алюминия определяется совокупным влиянием температуры, продолжительности прокаливания и дозы минерализатора [134]. В присутствии минерализатора полиморфное превращение в а-А1203 осуществляется при 800—900 °С и происходит скачком, минуя стадию образования 0-А12О3. Особенный интерес в качестве минерализующей добавки при получении пористого корунда представляет фторо - водород, который может быть использован в этом процессе многократно, являясь своеобразным катализатором.
Пористый корунд получают по следующей схеме [134]. В верхнюю часть двухзонной печи загружают исходный гранулированный активный оксид алюминия и порошок фторида аммония, который используют в качестве минерализатора. Распределение температур в печи таково, что при прохождении через нее сверху вниз гранулы постепенно нагреваются от 20 до 1000 °С в первой зоне и от 1000 до 1400 °С — во второй. Время термообработки регулируется выгрузкой продукта из печи. По мере продвижения продукта в печи идут следующие процессы:
1. Разложение фторида аммония: NH4F ->- NH3 + HF.
2. Хемосорбция HF на поверхности у-А1203 при температурах около 700 °С.
3. Полиморфное превращение у-А1203 в а-А1203 с одновременной десорбцией HF с поверхности полученного продукта (700— 1000 °С).
4. Упрочнение пористого корунда (1000—1400 °С).
В условиях синтеза у-А1203 переходит в пористый корунд с сохранением суммарного объема пор. Полученный носитель а-А1203 имеет следующие характеристики:
Размер сферических гранул, мм. . . 2X3
Насыпная плотность, г/см3...................... 0,75
Удельная площадь поверхности, м2/г 10
Суммарный удельный объем пор, см3/г Примерно 0,55
Преобладающий размер пор, нм. . . 1000
Прочность на раздавливание, МПа Около 6