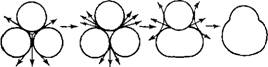
СОЗДАНИЕ ОПРЕДЕЛЕННОЙ ПОРИСТОЙ СТРУКТУРЫ КАТАЛИЗАТОРОВ
|
|
|
Рнс. 2.14. |
Тип структуры катализатора прежде всего обусловливает выбор способа его создания. Что касается наиболее распространенных глобулярных структур, то они, как уже указывалось, дискретны и образованы частицами, расположенными определенным образом [51, 65]. Создание определенной пористой структуры различных катализаторов осуществляется, как правило, на той стадии приготовления, когда исходные компоненты находятся в подвижном состоянии [41, 51]. Аморфные катализаторы со структурой ксерогелей образуются путем коллоидно-химического осаждения гелеобразных пористых тел, которое реализуется через следующие стадии: образование золя, переход его в гидрогель или коагель и обезвоживание, приводящее к получению ксеро-
|
|
|
S, Iи2/г |
|
0,8 |
|
2 |
|
JO |
|
2 |
|
Рнс. 2.15, Зависимость изменения удельной площадн поверхности снлнкагеля от рВ Среды осаждения [77] |
|
6 |
|
10 |
|
5 |
|
Рн |
|
Ph |
Рнс. 2.16. Зависимость изменения объема пор снлнкагеля от рН среды осаждения [77}
Геля [651[5]. Последней стадией получения катализаторов (адсорбентов) такой структуры является прокаливание. Параметры каждой стадии влияют на конечные характеристики продукта. Так, данные работы [77] показывают, что удельная площадь поверхности и объем пор силикагеля изменяются в зависимости от рН среды осаждения (рис. 2.15, 2.16). Образцы, полученные при низких значениях рН, обладают высокоразвитой поверхностью. По мере повышения рН осаждения поверхность уменьшается, содержание катионов в геле возрастает, из-за чего происходит частичное обезвоживание. При этом глобулы сближаются, образуя агрегаты, которые при сушке коалесцируют, чем и обусловливается снижение поверхности.
Влияние рН на объем пор является более сложным, так как объем пор представляет собой функцию упаковки и размера частиц (глобул).
Из минеральных адсорбентов (носителей) и катализаторов наряду с силикагелем широкое применение нашел гидроксид алюминия. Кристаллизующийся гидроксид алюминия достоит из глобулярных частиц аморфной структуры, внутри которых находятся кристаллы гидроксида. Во время сушки кристаллическая часть гидроксида образует жесткий скелет, противостоящий сжатию под действием капиллярных сил, аморфная же часть легко деформируется; и характер упаковки частиц гидроксида алюминия зависит от соотношения аморфной и кристаллической фаз. Это соотношение обусловлено условиями осаждения. Низкая температура, небольшие значения рН среды и быстрое смешение компонентов благоприятствуют увеличению содержания аморфной фазы [65]. Чем выше степень окристаллизованности гидроксида, тем меньше плотность упаковки и тем более крупнопористой структурой будет обладать готовый продукт.
Наиболее распространенными системами среди адсорбентов (носителей) и катализаторов являются двухкомпонентные системы на основе кремниевой кислоты и гидроксида какого-либо металла. На пористую структуру таких «смесей» оказывают влияние как факторы, воздействующие на индивидуальные оксиды, так и ряд дополнительных, а именно: состав смеси, воздействие друг на друга гидроксидов в процессах созревания и обезвоживания. Совместное осаждение приводит к изменению размера глобул, а, следовательно, к изменению характера пористости и значения удельной площади поверхности смешанной системы. При осаждении бинарных систем, одним из компонентов которых является Si02, а другим — гидроксид металла, кристаллизующийся со временем, защитное действие оказывает кремнезем, препятствующий кристаллизации [65]. Бинарные оксидные системы, например алюмосиликагели, применяют в качестве катализаторов процессов химической и нефтеперерабатывающей промышленности [2, 43, 51].
Регулировать пористую структуру можно также при синтезе катализаторов методом «склеивания» исходного материала, пронизанного тонкими порами. Таким путем могут быть получены бидисперсные материалы [20, 51 ].
Особое место среди адсорбентов, носителей и катализаторов занимают синтетические и природные цеолиты и цеолитсодержащие материалы, которые нашли применение за последние двадцать лет [65, 78, 79].
В настоящее время наряду с «чистыми» синтетическими цеолитами все шире используют смешанные системы: цеолит—аморфное пористое тело (силикагель, алюмогель, алюмосиликагель и др.) [80]. Аморфный компонент цеолитсодержащего катализатора называют матрицей. Обычно в аморфную матрицу вводят до 20 % цеолита типов X или Y, чаще в виде водородной или редкоземельной формы. По мере повышения количества цеолита в образцах возрастает объем мезопор и резко увеличивается объем пор с диаметром выше 150 нм.
Для катализаторов нанесенного типа формирование нужной пористости сводится к регулированию макроструктуры твердого тела. В настоящее время разработаны методы геометрического модифицирования частиц высокодисперсного непористого кремнезема — аэросила — и частиц, образующих скелет пористого кремнезема — силикагеля, алюмосиликагеля и др. Геометрическое модифицирование приводит к росту частиц, сглаживанию их поверхности и получению весьма однородных пор [81]. Так, при прокаливании и обработке паром можно изменить пористую структуру алюмосиликатов [51, 81 ]. Однако эти два фактора оказывают различное влияние на структуру. При прокаливании удельная площадь поверхности А1—Si сокращается пропорционально уменьшению общего объема пор, при этом размер пор существенно не изменяется. При обработке паром объем пор уменьшается медленнее, чем удельная площадь поверхности, а размеры пор резко увеличиваются.
Трансформация структуры при прокаливании и обработке паром происходит из-за изменения размеров, формы и взаимного расположения первичных частиц в результате диффузии. Этот перенос может происходить как за счет поверхностной диффузии вещества геля в местах срастания первичных частиц, так и при испарении этого вещества в одном месте и конденсации в другом [81 ].
При создании катализаторов нанесенного типа значительный интерес для использования в качестве модификаторов структуры представляют соединения, которые достаточно широко применимы как компоненты ряда контактных масс, например соединения ванадия [2, 51, 82, 83], фосфора [84] и др.
После пропитки катализаторы подвергают, как правило, термообработке, при которой имеют место топохимические реакции, т. е. реакции, в которых как минимум один реагент и один продукт находится в твердой фазе. Реакции локализуются на поверхности раздела твердых фаз (реагента и продукта реакции). В начале такой реакции происходит образование ядер новой фазы — фазы твердого продукта. Эти ядра растут в ходе реакции, их поверхность увеличивается и одновременно возрастает наблюдаемая скорость реакции. Затем ядра начинают перекрываться, поверхность раздела фаз уменьшается и вместе с ней снижается скорость реакции. Таким образом, характерной особенностью топохимических реакций является дифференциальная кинетическая кривая с максимумом.
При описании кинетики топохимических реакций в изотропных частицах, близких по форме к сферическим, часто используют уравнения Рогинского—Шульц. Первое описывает образование сплошной оболочки слоя продукта на сферической глобуле, т. е. восходящую часть топокинетической кривой, а второе — уравнение «сжимающейся сферы» — движение фронта реакции в глубь глобулы, соответствующее нисходящей части топокинетической кривой.
Метод модификации пористой структуры активными компонентами реализован при синтезе нанесенных катализаторов окисления диоксида серы: КС, ЛТИ-Ц, АС, ВЛТ. Катализаторы получены путем пропитки носителей аморфного алюмосиликата [51 ], силикагеля [75], цеолит - и асбестсодержащего алюмосиликата (а. с. СССР 929211) [83] раствором солей ванадия с последующей их термической обработкой. Механизм формирования пористой структуры всех перечисленных катализаторов в основе своей одинаков [51 ]. Рассмотрим его на примере катализатора с использованием алюмосиликатного аморфного носителя. Как известно, последний является материалом^ имеющим вполне определенную, сформировавшуюся глобулярную пористую структуру [51, 65]. Радиус большинства пор составляет доли единиц и единицы на
|
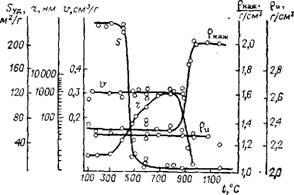
Рис. 2.17. Структурные характеристики катализатора, прокаленного при разной температуре |
Нометров. При прокаливании пропитанного соединениями ванадия (например, KV03) алюмосиликата структура его изменяется следующим образом: радиус т пор увеличивается на 1—3 порядка при пропорциональном уменьшении удельной площади поверхности 5УД; суммарный же объем пор v изменяется очень незначительно. Результаты, свидетельствующие о трансформации структуры алюмосиликата, представлены на рис. 2.17. Данные отражают средние результаты многочисленных серий опытов.
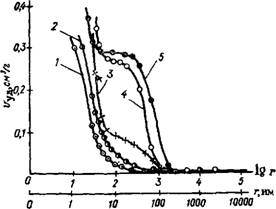
С ростом концентрации V205 в пропиточном растворе (рис. 2.18) и температуры прокаливания непрерывно увеличивается средний радиус пор, при этом удельная площадь поверхности уменьшается (см. рис. 2.17). Начиная примерно с 950 °С, происходит усадка зерен — суммарный объем пор уменьшается,
|
Рис. 2.18. Зависимость структуры пропитанного и прокаленного (і ~ 650 °С) алюмосиликата от концентрации модификатора Концентрация V2Oe, г/л: / — 14; 2 — 30; 3 — 43; 4 — 94; 5 — 160 |
|
Рис. 2.19. Схема трансформации структуры алюмосиликата |
А кажущаяся плотность ркаж возрастает. При 1000 °С усадка прекращается, вместо пористой дисперсной системы получается структура, близкая к монолиту.
При выявлении динамики перехода одной структуры в другую и вскрытии механизма этого явления проведены следующие исследования. Смесь, состоящую из KV03 и шариков алюмосиликата, помещали в муфельную печь на 20 ч при 750 °С. После окончания опыта оказалось, что алюмосиликат полностью растворился в KV03. Описанный эксперимент модельно отражает то, что происходит в объеме пропитанного носителя при его термообработке.
После пропитки носитель представляет собой систему, состоящую из тугоплавких зерен алюмосиликата и легкоплавкой примеси KV03. По мере повышения температуры образуется эвтектический расплав, который постепенно за счет капиллярных сил распространяется по всему объему, втягивая во взаимодействие новые участки поверхности. Наконец наступает момент, когда весь KV03 переходит в жидкость, и процесс идет по механизму твердожидкостного спекания [51, 521. Схема механизма переформирования структуры представлена на рис. 2.19. В результате появления расплава глобулы агломерируются, образуя при этом более крупные зазоры (поры) между собой, удельная площадь поверхности уменьшается, а суммарный объем пор изменяется незначительно.
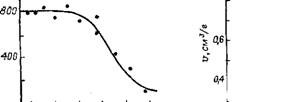
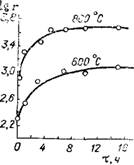
Трансформация структуры носителя, пропитанного солями ванадия, зависит, как уже указывалось, от концентрации соли, температуры и времени термической обработки. Кинетика, характеризующая изменение радиуса пор во времени при определенной температуре, представлена на рис. 2.20. Каждому температурному режиму соответствует конкретная пористая структура, отражающая изменения концентрации насыщенных растворов алюмосиликата в KVOj.
Таким методом может быть получена макроструктура с широким диапазоном параметров, описывающих ее. Она в свою очередь может выступать в качестве жесткого скелета, являясь подложкой для нанесения иных активных компонентов [51]. Когда наличие большого количества (5—10 %) соединений ванадия нежелательно, часть их может быть экстрагирована (отмыта), например водой. При модифицировании скелет носителя сохраняет свою макроструктуру. f
Как указано выше, одним из условий, которому должен отвечать искомый модификатор, является возможность последнего служить одновременно катализатором. К числу потенциальных
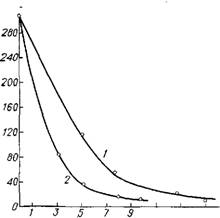
Модификаторов, удовлетворяющих поставленному условию, можно отнести и соединения фосфора, которые достаточно широко используются как компоненты ряда контактных масс [2, 51 |. Алюмосиликат, пропитанный солями фосфорной кислоты типа КН2Р04 и К2НР04 и прокаленный соответствующим образом, изменяет свою структуру. На рис. 2.21 показано, как уменьшается удельная площадь поверхности в зависимости от количества Р2О5 (Ср2о5)* вносимого в скелет носителя. Причем видно, что соль К2НРОф является более сильным модификатором.
При малой концентрации пропиточных растворов (до 100 г/л) эта зависимость может быть выражена следующими уравнениями для раствора КН2РО4 при Cp2os < 3,5 % (кривая 1, рис. 2.21):
- 40СР „ , ' (2.69)
S„ = 308-
Для раствора К2НРО4 при Ср2оЕ < 2,5 % (кривая 2, рис. 2.21):
S„ = 308-?0CPiOi. (2.70)
При более высоких концентрациях кривые удовлетворительно описываются уравнениями гиперболы:
Sy«=a/CP2o6- (2-71)
Здесь а и п — постоянные (га = 2, а = 2950 для раствора КН2Р04; га = 2, а = 900 для раствора К2НР04).
Достаточно гибко можно менять пористость, изменяя температуру прокаливания, сохраняя постоянным содержание Р206.
Возможность исполь - г
|
Различных |
|
Рис. 2.21. Зависимость изменения удельной площади поверхности алюмосиликата от содержания в нем модификатора Р205: |
|
|
|
;/ із 15 Ср^Ммасс.) |
|
Рис. 2.20. Кинетика изменения среднего эквивалентного радиуса пор при Температурах |
Зования модифицирован - ных соединениями фосфора 320\ алюмосиликатов в качестве носителей при синтезе
/ — раствор КН2Р04; 2 — раствор К2НР04
Иных контактных масс или адсорбентов будет определяться, во - первых, степенью извлечения модификатора Р205 и, во-вторых, сохранением той структуры, которая получена после трансформации.
Установлено, что соединения фосфора удается практически полностью экстрагировать водой или 10 % раствором H2S04, сохраняя при этом измененную структуру носителя.
Характер структурных изменений, происходящих в силика - геле, в основном идентичен таковым в алюмосиликате, а именно: удельная площадь поверхности уменьшается до нескольких квадратных метров на грамм, а средний эквивалентный радиус пор соответственно увеличивается. Уменьшение удельной поверхности сопровождается снижением суммарного объема пор в среднем на 40 % от исходного, тогда как в алюмосиликате суммарный объем пор изменяется незначительно. В практических целях для трансфэрмации структуры лучше использовать соль К2НР04, так как в этом случае образуется более равномерная квазиглобулярная структура при минимальном количестве Р205. Как и в случае алюмосиликатов, модификатор из силикагеля экстрагируется хорошо, а структурные преобразования необратимы.
Таким образом, свойство фосфорных соединений как модифицирующих добавок в сочетании сих каталитическим началом может быть реализовано при синтезе различных контактных масс с заданными характеристиками.
Изучение закономерностей, связывающих скорость течения каталитического процесса со структурой контакта, позволяет объяснить оптимальность пористой структуры, которая отвечает максимальной степени превращения реагентов.
Накопленный экспериментальный материал позволил вскрыть механизм формирования и трансформации макроструктуры различных носителей и катализаторов, что может способствовать сознательному поиску путей управления структурой катализаторов нанесенного типа.
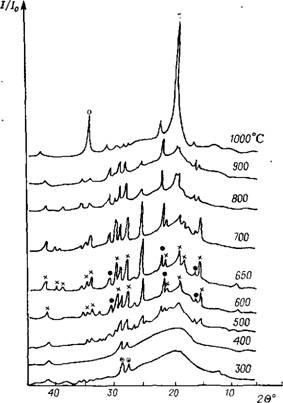
Наряду с формированием определенной пористости, важно чтобы образовывалась соответствующая микроструктура, обеспечивающая максимум активности. Такое создание фазового состава можно четко проследить при формировании катализатора ЛТИ-Ц. Последний отличается прежде всего тем, что в качестве носителя используется цеокар-2. Это цеолитсодер - жащий алюмосиликат, содержащий 10—15 % (масс.) цеолита типа У в редкоземельной форме, равномерно распределенный в аморфной матрице. По мере роста температуры термообработки пропитанного носителя интенсивность дифракционных линий поли- ванадатов калия и редкоземельных элементов растет, достигая максимума при 600—700 °С (рис. 2.22). Таким образом, максимальное количество компонентов, обеспечивающих максимум активности, образуется при 600—700 °С. Интересным обстоятельством является то, что не только с точки зрения формирования
|
Рис. 2.22. Формирование микроструктуры катализатора ЛТИ-Ц в процессе термообработки Обозначения: X — K3VsO,4; © — K2S04; О — крнстобалнт; • — (РЗЭ) V04. Химического состава область температур 600—700 °С является оптимальной, но и в отношении пористости это также благоприятный температурный интервал [51, 83]. При 1000 °С имеет место образование (ї-кристобалита (см. рис. 2.22), что является одной из причин термической инактивации катализатора *. I аким образом, при синтезе катализаторов необходимо подбирать такие технологические параметры, которые обеспечили бы создание оптимальных химического состава, микро - и макроструктуры, соответствующих максимуму активности. |