ГЕТЕРОГЕННЫЕ КАТАЛИЗАТОРЫ НА ОСНОВЕ ХРОМОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Хроморганические соединения, хемосорбированные на активированном (дегидратированном) силикагеле S1O2, образуют высокоэффективные катализаторы полимеризации этилена и сополимеризации этилена с другими а-олефинами [123—125].
Разработке высокоэффективных хроморганических катализаторов фирмы «Юнион Карбайд» предшествовали работы фирмы «Филлипс» по активации силикагеля - носителя и приготовлению на нем окиснохромового катализатора [126]. С использованием окиснохромовых катализаторов этой фирмой были созданы промышленные производства полиэтилена и сополимеров этилена с другими а-олефинами.
Для создания процессов производства ПЭ газофазным методом фирмой «Юнион Карбайд» разработаны высокоэффективные хроморганические однокомпонентные катализаторы на силикатных носителях. К этим катализаторам относятся хромоцен [дициклопентадиенилхром (CsHsbCr], нанесенный на активированный силикагель, и бис (трифенилсилил) хромат, восстановленный алюми - нийалкилом и нанесенный на активированный силикагель [125, 127, 128].
Активность катализатора в процессе полимеризации определяется удельной поверхностью носителя, объемом пор и их средним диаметром, а также температурой дегидратации носителя и условиями взаимодействия хроморганического соединения с носителем.
Хромоценовый катализатор с высокой активностью был получен с использованием аморфной окиси кремния с удельной поверхностью 285 м2Д, объемом пор 1,2 см3/г и средним диаметром пор около 10 нм. Так как физические свойства силикагеля зависят от условий его приготовления, выбор марки Si02 является важным условием получения катализатора требуемой активности. От условий синтеза и особенно активации силикагеля зависит и химический состав этого соединения, в частности, содержание остаточных гидроксильных групп, взаимодействием с которыми осуществляется химическая связь хромоцена с носителем [123, 129]. Поэтому весьма существенным параметром синтеза хро- моценового катализатора является температура дегидратации силикагеля. Так, с повышением температуры дегидратации с 200 до 300 °С при одной и той же концентрации нанесенного хромоцена выход полимера при полимеризации этилена в среде растворителя увеличивается почти в 2 раза. Дальнейшее повышение темпе - атуры дегидратации до 400—670°С приводит к уменьшению содержания хромоцена в катализаторе и снижению выхода полимера. Однако относительная активность, характеризуемая выходом полимера на еди
Но ницу массы хромоцена, значительно возрастает (с 232 до 1671 кг/моль).
Чтобы предотвратить образование циклических структур при взаимодействии хромоцена с гидроксильными группами носителя, необходимо обеспечить минимальное содержание гидроксильных групп в носителе. Это достигается дегидратацией силикагеля при высоких тем - тературах (600—800°С).
Полярографическим методом установлено, что в хро - моценовом катализаторе в основном содержится Сг2+ и небольшое количество Сг3+. Механизм образования АЦ на этом катализаторе пока не ясен. Предполагают [123], что АЦ является адсорбированный на силикагеле двухвалентный хром, связанный с циклопентадиениль - ным лигандом.
Хромоцен без носителя совершенно неактивен в процессе полимеризации этилена. Активность он приобретает в результате хемосорбции на силикагеле. Полимеризация этилена начинается, вероятно, с включения молекул этилена в связь Сг—О. Рост полимерной цепи по-видимому, идет по связи Сг—С согласно общепринятому механизму Циглера—Натта. Энергия активации процесса полимеризации на хромоценовом катализаторе близка к энергии активации на классических циглеровских катализаторах и равна 42 кДж/моль.
При полимеризации этилена на хромоценовом катализаторе получают полимер со сравнительно узким ММР, вероятно, в результате необычайно высокой скорости переноса цепи на водород, характерной для этого катализатора [125J. Так, если для обычных катализаторов Циглера — Натта /гн/^м = 2,1 • 102, то для хромо - ценовых /їн/Ам — 3,8- 103 (где и kn — константы скоростей переноса цепи на мономер и водород). Молекулярную массу ПЭ, синтезируемого на хромоценовых катализаторах с помощью водорода можно регулировать в весьма широких пределах.
Каталитическая активность бис(трифенилсилил) хромата (БТФСХ), нанесенного на Si02, в процессе полимеризации этилена при низком давлении (1—2 МПа) значительно возрастает при обработке его алкилалюми - нием. Лучшим восстановителем является диэтилэтокси - алюминий. По-видимому, природа алюминийорганиче - ского соединения оказывает существенное влияние как на число АЦ, так и на свойства получаемого полимера [127].
Широкое ММР получаемого на этом катализаторе ПЭ свидетельствует об образовании каталитической системы, содержащей неоднородные АЦ, каждому из которых соответствует своя константа скорости роста и обрыва цепи.
Предполагают [127], что активный центр БТФСХ может иметь следующую структуру:
■ XR
Где L — лиганд хрома, структура которого точно не установлена; R — алкильный радикал от алюминий - алкила.
Рост полимерной цепи на этом катализаторе, подобно полимеризации на хромоценовом катализаторе, протекает через предварительную координацию этилена на восстановленном ионе хрома с образованием я-ком - плекса по обычному механизму катализаторов Циглера—Натта [127]:
L L
Iі Iі
I—Сг—R + СН2=СН2 -------- I—Сг—СН2—СН2—R
Так же, как и для хромоценового катализатора, активность нанесенного на активированный силикагель БТФСХ зависит от температуры дегидратации носителя, которая лимитирует содержание гидроксильных групп. Для БТФСХ активацию Si02 проводят при 400—600°С.
Высокоэффективные хроморганическне катализаторы были предназначены прежде всего для газофазного процесса. Однако основные закономерности процесса полимеризации этилена были изучены и при проведении реакции в среде растворителя. Они оказались идентичными закономерностям газофазной полимеризации этилена.
Характер температурной зависимости скорости полимеризации этилена и влияния на скорость процесса давления мономера такой же, как при полимеризации на классических катализаторах Циглера — Натта. Темпе
ратурная зависимость скорости процесса в среде растворителя в интервале температур 30—100°С для хро - моценового катализатора проходит через максимум при 60°С, а затем при повышении температуры наблюдается резкое снижение скорости.
Повышение давления вызывает резкое увеличение скорости реакции полимеризации. Изучение влияния давления на процесс полимеризации этилена показало, что при температуре 90°С и времени полимеризации 1 ч (концентрация хромоцена 0,055 ммоль на 0,4 г БЮг, температура дегидратации 600°С) образование полимера наблюдается при давлении не менее 0,7 МПа. Повышение давления до 2,1 МПа увеличивает выход полимера в 8—10 раз. Если давление повысить до 2,8 МПа и более, скорость увеличивается настолько, что контроль температуры вызывает большие затруднения [130].
|
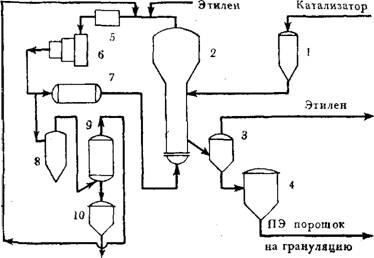
Рис. 3.15. Принципиальная технологическая схема промышленного процесса полимеризации этилена газофазным методом фирмы «Юнион Карбайд»: 1 — расходная емкость для катализатора; 2— реактор; 3 — приемная емкость; 4— продувочная емкость; 5—фильтр; 6 — компрессор; 7—холодильник; 5 — цнклон; 9 — сепаратор; 10 — сборник низкомолекулярных продуктов.
|
|
1ІЗ |
Молекулярно-массовые характеристики синтезируемых полимеров зависят от многих факторов, влияющих
на состав и активность катализаторов: от состава и структуры носителей, температуры дегидратации, температуры и длительности взаимодействия хроморгани - ческого соединения с носителем в процессе синтеза хроморганического соединения, а для БТФСХ, нанесенного на активированный силикагель и от состава алкилалкоксиалюминия.
Применение хроморганических катализаторов позволило получать широкий ассортимент марок ПЭ по ПТР с плотностью 940—965 кг/м3 и как с узким, так и с широким ММР. Материал перерабатывается всеми методами переработки.