Содержание гидроксильных групп на одном квадратном нанометре
В настоящее время, по-видимому, уже установилась общая точка зрения, что. на сглаженной, непористой, термически стабилизированной аморфной поверхности кремнезема, которая
полностью гидроксилирована [15], содержится 4—5 групп SiOH на 1 нм2[16] (или на площади 100 А2), причем такие группы сохраняются, когда образец кремнезема прогревается при 120—150°С.
|
Тип групп |
|
Одиночные ОН-группы на поверхности Парные ОН-группы на поверхности, связанные водородными связями Внутренние ОН-группы, связанные водородными связями Молекулярная вода |
Это значение поверхностной концентрации гидроксильных групп цитируется в большинстве обзорных статей [4—13]. Такая поверхность кремнезема получается после прогревания порошка или силикагеля до повышенной температуры с целью удаления удерживаемых внутри частиц молекул воды и групп ОН, перекрывания микропор и последующей регидратации образца кремнезема в воде.
Армистед и др. [61] показали, что на регидратированном пирогенном кремнеземе на поверхности содержится 4,6 ОН-груп- пы/нм2, причем из них 1,4 ±0,1 составляют свободные гидро - ксильные группы, не связанные водородными связями с соседними группами, а 3,2±ОД взаимно связаны попарно водородными связями. Кроме того, существуют внутренние группы SiOH в количестве 1,6 ОН-групп/нм2, которые необратимо удалялись при прокаливании. Ниже представлены данные по ИК - спектрам:
Идентифицируемая полоса поглощения, см-1
3750 3540
3650
3400, 1627
Атомы дейтерия тяжелой воды вступают в обмен с атомами водорода только поверхностных гидроксильных групп, но не групп ОН, находящихся внутри кремнезема. Журавлев и др. [62] сравнили потери массы, получаемые в результате прокаливания образца кремнезема, с содержанием групп SiOH на поверхности, найденным методом дейтерообмена. Эксперимент проводился на образце силикагеля с удельной поверхностью 340 м2/г и диаметром пор 110 А. Авторы нашли, что полное со
держание воды в образце было больше, чем связанной, представляющей собой поверхностные гидроксильные "группы, причем поверхностная концентрация групп ОН оказалась равной 5,2 ОН-групп/нм2.
|
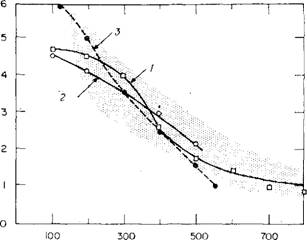
Температура °С Риє. 6.3. Зависимость концентрации ОН-групп на поверхности кремнезема от Температуры прокаливания образцов Si02. Затененная площадь — область экспериментальных данных, полученных для различных типов кремнезема Давыдовым, Киселевым н Журавлевым [43]. Дегидратация прокаленного (700 °С) и затем регидратированного кремнезема осуществлялась: 1 — на воздухе; 2 — в вакууме (по данным Тейлора, Хоки и Петика [84]); 3 — данные для образцов кремнезема, предварительно не прокаленных (на основании результатов, полученных Уиттер- ховеном и др. [83], Фрипья и др. [47], Журавлевым и Киселевым [85], Тейлором, Хоки и Петикой [84, 86]). |
Результаты, полученные методом дейтерообмена, были обобщены Давыдовым, Киселевым и Журавлевым [43] и сопоставлены с данными химических методов, в которых использовались LiCH3 и MgCH3I; эти данные представлены на рис. 6.3 и табл. 6.1. Позднее Агзамходжаев, Журавлев, Киселев и Шенге - лия [63] применили этот метод на серии гидроксилирозанных силикагелей, аэрогелей и других видах кремнезема, имевших различные размеры пор, и обнаружили, что поверхностная концентрация групп ОН менялась в интервале 4,2—5,7 ОН-групп/нм2. Используя подобный метод, Мэдели и Ричмонд [64] установили, что на четырех образцах кремнезема с удельной поверхностью в интервале 374—701 м2/г концентрация групп ОН на поверхности составляла только 4,27—4,63 ОН-групп/нм2 без заметного отклонения. Эти данные свидетельствуют; по-видимому, о возможностях выбранного метода, так как дейтерообмен, несомненно, ограничивается поверхностью. Удельную поверхность лучше всего определять по адсорбции криптона методом БЭТ, так как природа поверхности в этом случае меньше сказывается на результатах, чем при использовании азота в качестве адсорбата. Смесь Н20—D20, полученная после обмена, анализируется с помощью масс-спектрометра [17].
Вирцинг [50, 65] показал, что число групп ОН может быть также определено по адсорбции на них воды с одновременным измерением получающейся, единственно возможной при подобных исследованиях ИК-полосы поглощения 5265 см-1. Исследовался хорошо спеченный образец кремнеземного порошка фирмы «Мэллинкродт», который многократно нагревался до 800°С, охлаждался и каждый раз повторно регидратировался. Его удельная поверхность составляла 166 м2/г; очевидно, образец не имел микропор. После высушивания при 120°С образец содержал 5,2 ОН-групп/нм2, как показал метод прокаливания до высоких температур, или 4,0 ОН-групп/нм2 по определению методом ИК-спектроскопии. На образце аэрогеля было найдено значение концентрации гидроксильных групп на поверхности, равное 4,4 ОН-групп/нм2.
Согласно данным де Бура и Влеескенса [66], на исходном кремнеземе, который не подвергался термической обработке, содержалось 6,2 ОН-групп/нм2, но после повторного увлажнения, нагревания и высушивания поверхность образца выравнивалась на молекулярном уровне, и достигалось значение 4,6± ±0,2 ОН-групп/нм2. На таком высушенном образце при полностью гидроксилированной поверхности примерно половина из имеющихся силанольных групп присутствует в виде попарно связанных водородными связями групп ОН. При беспорядочном, произвольном распределении поверхностных групп представляется очевидным, что многие группы SiOH будут находиться на поверхности в виде одиночных, неспаренных групп [67].
Согласно данным Андерсона и др. [68], на гидроксилированной поверхности в присутствии адсорбированной воды могут находиться два типа молекул воды и два типа групп SiOH. Мономерная молекула Н20 может быть связана с одиночной группой SiOH. Кластер, состоящий из молекул Н20, может образовывать сетку, связанную водородными связями. Группы SiOH могут быть несвязанные и связанные с молекулами Н20.
Бермудец [69] использовал протонный ядерный магнитный резонанс для определения числа поверхностных силанольных групп даже при условии покрытия поверхности адсорбированной водой толщиной вплоть до трех монослоев. Силикагель имел удельную поверхность 800 м2/г, а найденная концентрация силанольных групп составила 7-10~6 моль/м2 или 4,2 ОН-групп/нм2.
Как будет обсуждено в связи с процессами дегидратации и регидратации поверхности кремнезема, многие из упоминавшихся данных, показывавших более чем 4,6 ОН-групп/нм2, вероятно, являются следствием присутствия в образце внутренних групп SiOH, которые, как это принималось авторами, были отнесены к поверхностным.
Согласно данным Боема [8], определение числа гидроксильных групп ОН на поверхности химическими методами дает противоречивые результаты. Он указал, что при проведении большинства химических реакций, таких, например, как этерификация или хлорирование, в подобную реакцию вступает только примерно около половины всех присутствующих на поверхности групп ОН от известного полного числа, равного 5 ОН-групп/нм2, определенного эффективным методом водородного обмена или по потере воды.
Возможно, что подобные замещающие группы слишком велики, чтобы размещаться на каждом исходном центре SiOH. Когда замещающая группа (например, этоксильная группа, или атом хлора) всего лишь ненамного больше группы ОН, то примерно только каждая вторая группа ОН сможет заместиться, поскольку положение лежащих ниже атомов кремния фиксировано. Однако метильная группа оказывается достаточно небольшой и способна присоединиться к каждому центру SiOH. Как сообщалось в другом разделе данной книги, к поверхности кремнезема на площади 1 нм2 могут присоединяться от четырех до пяти метоксигрупп. Именно поэтому использование таких реактивов, как СНзЬі и CHsMgl, в работе Фрипья и др. [47] оказалось успешным. Другим веществом, содержащим метальные группы, является составное соединение, в котором присутствуют диметилцинк и тетрагидрофуран (ZnMe2-2 ТГФ). Это соединение использовал в своей работе Ханке [70], который измерял концентрацию групп ОН на поверхности аэросила по определению объема выделяющегося метана СН4.
Единственным другим эффективным заместителем достаточно малого размера, позволяющим замещать полностью все группы ОН на поверхности, представляется атом фтора, но оказалось трудным создать поверхность типа SiF без того, чтобы не разрушить структуру Si02.
Лифландер и Штобер [71] использовали раствор триизобу - тилалюминия в гептане с целью проведения реакции с поверхностными группами SiOH. После промывания образца гептаном для удаления избыточного количества реактива поверхность кремнезема удерживала после гидролиза 5,7 мкмоль А1:
SisOH + A1R3—SisOAl (OH)2 + 2RH
Теоретическая величина концентрации поверхностных гидроксильных групп
Расчет числа силанольных групп на поверхности может быть осуществлен различными способами. Простейшим является способ, предложенный Айлером [3], полностью основанный на геометрических рассмотрениях и учете плотности аморфного кремнезема. Этим способом, описанным в гл. 1, определено, что 7,8 атома кремния должно содержаться на 1 нм2 на поверхности или очень близко к поверхности. Автор первоначально допускал, что на поверхности должно содержаться 7,8 SiOH-групп/нм2. Однако Боем [8] указал, что поскольку не все атомы кремния точно находятся на границе раздела фаз, а могут располагаться выше или ниже этой границы, то только половина всех поверхностных атомов кремния должна нести группы ОН, и поэтому поверхностная концентрация таких групп должна быть равной только 3,9 ОН-групп/нм2.
Так как плотность и показатель преломления аморфного кремнезема близки к соответствующим величинам кристобалита и тридимита, то Айлер предположил, что концентрацию поверхностных гидроксильных групп можно было бы оценить по этим кристаллическим структурам. Исследование кристаллической грани {100} p-кристобалита, которая была выбрана автором, привело к заключению, что на каждом участке площади поверхности, равном 50,2 А2, имелось два более низко расположенных уровня атомов кремния, не несущих гидроксильных групп, и два выше расположенных уровня атомов кремния, в которых каждый атом Si удерживал по две группы ОН. Это давало концентрацию 8 ОН-групп/нм2. Аналогичные расчеты для поверхности тридимита дали концентрацию 4,6 ОН-групп/нм2. Пери и Хенсли [67] продолжили рассмотрение кристобалита и отметили, что если выбирается грань {100}, то действительно каждый атом кремния должен удерживать две группы ОН, давая значение концентрации ~8 ОН-групп/нм2. Если бы такие гидроксильные группы могли попарно удаляться произвольным образом, то, согласно расчету, выполненному по методу Монте-Карло, на поверхности должно было бы оставаться 4,56 ОН-групп/нм2 в виде либо парных групп ОН (две группы на одном атоме Si), либо смежных, вицинальных групп ОН (одна группа на одном атоме Si, но две группы ОН расположены рядом).
Так как ранее полученные экспериментальные данные (табл. 6.1) давали значение концентрации около 8 ОН-групп/нм2, то принималось, что полученные в теоретических расчетах более высокие значения концентраций групп ОН были более вероятными. Такое положение получило некоторую поддержку
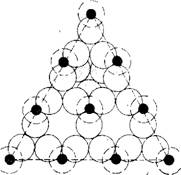
в связи с появлением работ Беляковой, Джигит и Киселева [72] и Жданова и Киселева [73], которые определили, что концентрация ОН составляет до 12 мкмоль/м2, или до 7,2 ОН-групп/нм2. Однако де Бур и Влеескенс [74, 75] позже указали, что поскольку p-кристобалит кристаллизуется в виде октаэдра, то концентрация гидроксильных групп должна подсчитываться на ок- таэдрической грани {111}. Такая поверхность показана на рис. 6.4. Рассчитанное значение концентрации гидроксильных
|
Рис. 6.4. Расположение атомов на октаэдрической грани [111] кристобалита, содержащей 4,55 SiOH-группа/нм2. |
|
/ V |
Большие кружки — атомы кислорода; маленькие кружки — атомы кремния на поверхности; штрих-кружки — положение гидроксильных групп на поверхности, присоединенных к нижележащим атомам кремния. Масштаб размеров атомов не сохранен.
Групп составляет 4,55 ОН-групп/нм2. Экспериментальные определения подтвердили этот результат.
Из данных, которые появились к настоящему времени, следует, что термически стабилизированная поверхность аморфного кремнезема действительно очень напоминает октаэдрическую грань и что значение концентрации 4,6 ОН-групп/нм2 стало обычно наблюдаемым экспериментально значением для регидра - тированных образцов кремнезема, которые были «сглажены» и прокалены при высокой температуре, а затем полностью регид - ратированы и высушены.