Работы Оккерса
Посредством измерения скорости убывания мономера при различных концентрациях кремнезема и разных рН Оккерс [29]
Определил кажущийся «порядок» полимеризации. Уравнения для второго и третьего порядков реакций выражаются как
|
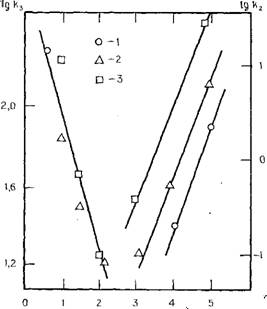
Рнс. 3.39. Зависимость скорости убывания мономері в процессе полимеризации от рН при различных молярных концентрациях Si02 (по данным Ок- Керса [29]). 1 — 0,0128 М Si02; 2 — 0,0417 М; 3 — 0,0641 М и 0,834 М; кг и ft2 —константы скорости Полимеризации ниже и выше рН 2,2 соответственно. |
|
РН |
|
Ы и —константы скорости реакций при данном рН, Сt и С0 — концентрации мономера в моменты времени t T — 0 соответственно. Полученные автором значения для констант скоростей при различных рН представлены на рис. 3.39. Важно подчеркнуть, что константа скорости «третьего» порядка реакции ниже рН 2 не менялась с изменением концентрации кремнезема, тогда как константа скорости «второго» порядка реакции понижалась выше рН 2 в том случае, когда кон- |
С t 1 — k^t - j - Со СГ2 = 2k%t - f Cq 2
Центрация кремнезема составляла менее 0,06 М (0,036 %). Автор отмечал, что величина рН елияєт на скорость, но не посредством прямого каталитического действия ионов Н+ или ОН~, а за счет генерирования ими положительных или отрицательных ионов на поверхности реакционноспособных разновидностей кремнезема, которые затем вступают во взаимодействие с неио - низированными частицами. Однако это еще не объясняет, почему только в случае реакции «второго» порядка при включении в систему отрицательных ионов выше рН 2 сказывалось действие концентрации кремнезема.
Как описывается ниже, причина подобного поведения может быть связана с индукционным периодом, отмечаемым при низкой концентрации кремнезема. Когда начальная реакция может протекать только с участием ионизированной формы мономера или димера, то скорость убывания мономера будет очень мала. Последующее образование некоторых полимерных разновидностей с более кислыми группами SiOH, способных ионизироваться более сильно, чем мономер, ускоряет процесс полимеризации и увеличивает константу скорости реакции. При низких концентрациях кремнезема эта стадия достигается более медленно.
Айлером [87] ранее было показано, что полимеризация при рН<2 катализировалась не ионами Н+, a HF. Тем не менее Оккерс выразил сомнение, что фторид-ион присутствовал в исследуемой им системе, поскольку в исходном силикате натрия невозможно было обнаружить какие-либо «следы» фтора. Хотя Айлер и отмечал, что ионы фтора оказывали воздействие при их содержании ниже 0,0002 %, тем не менее в настоящее время кажется маловероятным, что подобное количество фтора могло присутствовать во всех изучаемых системах.
Богданова [146] наблюдала, вероятно, аналогичный эффект, когда при рН < 3 скорость деполимеризации поликремневой кислоты при значительном разбавлении суспензии определялась кислотным каталитическим действием, т. е. возрастала с понижением рН. Эта скорость в разбавленной суспензии не зависела от концентрации SiC>2 в интервале 0,003—0,056 % при 20°С. Так как поликремневая кислота была получена из природного нат - ролита, то, возможно, в ней присутствовали следы фтора. Как было показано Айлером, фтор повышает рН, при котором наблюдается минимальная скорость полимеризации, с 2 до 3.