Гидроксилированная поверхность
Так как атомы кремния на поверхности аморфного кремнезема находятся по определению не точно в регулярном геометрическом порядке, то очевидно, что гидроксильные группы, присоединенные к соответствующим атомам кремния, не будут в точности на равном расстоянии друг от друга (рис. 6.1).' Сле
довательно, не все гидроксильные группы эквивалентны по своему поведению в отношении адсорбционных явлений или химических реакций.
Н
НоО
TOC \o "1-3" \h \z ® Рч © П2'
/Н *V /HVH
9 I 7nV І Поверхность
-Si г--------- >Si — ru S-. - - Sir--------------
О71^о/|Чо с/Iчо I 0 ,
0 0 0 0
|
t |
Выше 175° С
Н н и н
/• \ / \ /• /
0 0 0 0 о
1 I I I / N
|
Поверхность |
—Si—Si—Si—Si----- Si—Si—
|
0 0 0 |
О'о'о'о' 0 ~
0%°
HO OH 0
|
© |
H Si H n-Si-n
ООО О ~
9 Поверхность Si-Si—Si Si
— Si - _ -
|
0 0 0 0 |
|
О 0 / \ J - Si — Si------------------ Si - |
/ l\/l\ /|\ / I \ / I 0 ' 0 1 0 k 0 " 1
A?\u,/9 Поверхность ■Si— Si— Si-— Si
О О 1 О 1 О 1 О 1 О 1 о ' о и О О 0и О 0 о о и
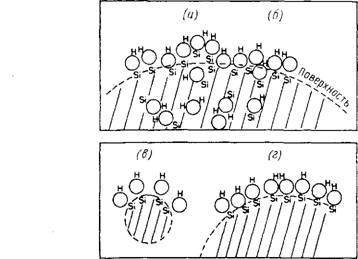
Рис. 6.1. Схемы расположения возможных типов гидроксильных групп на поверхности аморфного кремнезема. а — смежные, расположенные рядом (вицинальные), гидратированные; б — смежные (вйцинальные), безводные; в — силоксановые группы, дегидратированные; г — гидроксилированная поверхность; д — одиночная (свободная) гидроксильная группа; е — парные и строенные гидроксильные группы; ж — смежные, взаимно связанные водородными
Связями.
Примечание. Типы групп е и ж, вероятно, не существуют на высушенной поверхности.
Кроме того, можно представить, что в водном растворе дополнительные молекулы монокремневой кислоты могут конденсироваться на поверхности, причем к атомам кремния могли бы присоединиться две или даже три гидроксильные группы (как это показано на рис. 6.1 в положениях е и ж). Хотя существованием таких групп, как было постулировано, объясняются некоторые данные, вероятно, что они впоследствии конденсируются и на высушенной поверхности остаются только SiOH-группы.
При высушивании кремнезема молекулы воды, связанные водородной связью, как показано на рис. 6.1, удаляются при обычной температуре в вакууме или при 150°С на воздухе.
Концентрация силанольных групп, силанольное число, т. е. число гидроксильных групп, находящихся на единице поверхности, было предметом многих исследований и дискуссий.
Белякова и др. [6] нашли, что концентрация силанольных групп оказывалась примерно одинаковой для различных типов
|
Рис. 6.2. Факторы, влияющие на число гидроксильных (силанольных) групп, находящихся внутри и на поверхности первичной частицы кремнезема и способных образовывать молекулы воды. а — подповерхностная гндрокснльная группа искривляет поверхность, что способствует появлению на ней парных и строенных силанольных групп; б — гидроксильная группа, расположенная вблизи поверхности, удерживается более прочно и поэтому вызывает увеличение числа групп на единице поверхности; в — число гидроксильных групп на частицах кремнезема очень небольшого размера (менее 100 нм) в расчете на единицу поверхности понижено; г — гидроксильные группы на частице большего размера располагаются ближе друг к другу и способны образовывать более прочно удерживаемые пары гидроксильных групп, связанных между собой водородными связями. |
Кремнезема. С другой стороны, довольно различающиеся результаты были сообщены другими исследователями. Как указали Дубинин, Беринг и Серпинский [22] в 1964 г., на поверхности образцов аморфного кремнезема, полученных различными путями, упаковка тетраэдров, состоящих из атомов кислорода и одного атома кремния, не является регулярной и может изменяться. Когда частицы кремнезема образуются в воде, то на число ОН-групп можно воздействовать несколькими путями, как это показано на рис. 6.2;
1. Подповерхностные неконденсированные «захороненные» SiOH-группы, расположенные ниже поверхности силоксановой
Сетки, увеличивают искривления иа поверхности. Когда они находятся более глубоко в объеме, то могут быть удалены только при высокой температуре.
2. Некоторые SiOH-группы могут быть расположены как раз в пределах поверхности, поэтому они увеличивают среднюю плотность упаковки ОН-групп на единице поверхности, как это показано на схеме б.
3. На частицах с очень небольшим радиусом кривизны наличие искривлений с положительным радиусом приводит к тому, что SiOH-группы удерживаются на большем расстоянии друг от друга, так что могут образовывать более слабые водородные связи между собой. Поэтому такие группы удаляются более легко при повышенной температуре, как это имеет место в случае в по сравнению с г.
4. В зазорах — в точках контакта между частицами, где имеется отрицательный радиус кривизны, например в микропорах,— поверхностные ОН-группы, наоборот, расположены ближе друг к другу, и поэтому дегидратация более затруднена.
5. В частицах, образованных при низкой температуре и низком значении рН из еще меньших по размеру частиц путем их агрегации, имеются микропоры или субмикропоры, как это описано в гл. 4, с гидроксилированными поверхностями, в которых сильно удерживается вода. Величина таких поверхностей не измеряется методом БЭТ из-за того, что молекулы азота не могут проникать в микропоры, и поэтому концентрация ОН-групп на квадратный нанометр кажется аномально высокой.