Деполимеризация в кислом растворе
Изучение деполимеризации низкомолекулярных полимеров подтверждает тот факт, что степень конденсации в объеме трехмерных полимеров зависит от температуры, при которой они приготовлялись или до которой они нагревались. Еще более важна зависимость от рН среды, так как скорость внутренней конденсации в трехмерных полимерных единичных образованиях определяется концентрацией ионов ОН~. Даже в области рН 2—3 имеется заметное различие в скоростях конденсации, а при рН 8 скорость на много порядков больше. В итоге скорость, при которой полимерные единичные образования данного размера деполимеризуются в молибдатном реактиве, заметно ниже, когда полимер подвергается действию более высоких температур или при более высоких значениях рН.
Штаде и Викер [109] исследовали деполимеризацию поликремневой кислоты. Они приготовили раствор поликреМневой кислоты с минимальным содержанием мономера путем растворения порошка (ЫгБЮзК в разбавленной кислоте при 0°С. Образцы раствора разбавляли затем в воде при рН 1,3—5,5 до содержания 0,0012 % БіОг, после чего проводили деполимеризацию до мономера при различных рН и температурах. Периодическим отбором образцов растворов и их анализом на содержание мономера с помощью молибдатного метода Александера [24а] устанавливали скорость деполимеризации. Одновременно также измеряли скорость, с которой остающийся в растворе полимер вступал в реакцию с молибдатом.
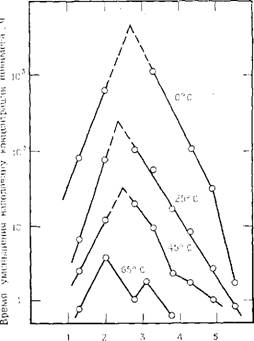
Экспериментальные данные изображены на рис. 3.18. Видно, что время уменьшения наполовину концентрации полимера в воде при содержании 0,0012 % Si02 максимально и соответственно скорость деполимеризации минимальна при рН~2,5. Однако зависимость довольно сложная. Вероятно, это происходит из-за одновременного протекания двух различных реакций.
В том случае, когда поликремневая кислота образуется при низких рН и при 0°С, происходит формирование полимерных частиц. Однако внутренние SiOH-группы не все конденсируются полностью. Но когда подобный золь нагревается и/или рН поднимается выше 2, то происходит дальнейший процесс внутренней конденсации. Поэтому логично ожидать, что если золь разбавляется при 0°С, то происходит только деполимеризация. Однако при повышении температуры н увеличении рН происходят уже два процесса: деполимеризация или растворение частицы и конденсация в ее объеме с образованием еще большего числа силоксановых связей, которые в дальнейшем должны разорваться, образуя мономер, вступающий в реакцию с молибдено-
|
Рн Рис. 3.18. Зависимость скорости деполимеризации кремнезема в растворе, содержащем 0,0012 % Si02, в интервале температур 0—65 °С (по данным Штаде И Викера [109]). |
Вой кислотой. Таким образом, скорость реакции с молибденовой кислотой значительно понижается.
Доказательством такого поведения системы служит то, что константа скорости реакции для полимера, приготовленного и разбавленного при 0°С, составляла 0,046 мин-1, тогда как при разбавлении полимера при 25°С значение константы через 5 мин падало до 0,03 мин-1. Дополнительным доказательством может являться то, что, когда деполимеризация прослеживалась при 0°С, т. е. когда никаких внутренних изменений в полимере не происходит, а только идет процесс деполимеризации, скорость последнего в области рН 3—5 была строго пропорциональна концентрации ионов ОН-.