Вторичная переработка пластмасс
Термодеструкция
Термодеструкция в инертной атмосфере или в вакууме определяет предельную стабильность полимера в отсутствие других факторов, стимулирующих деструкцию. Она соответствует условиям, при которых химические связи в полимере приобретают достаточно энергии для того, чтобы самопроизвольно разрываться со значительной скоростью.
Термодеструкция редко встречается в приложениях, требующих длительного срока службы полимера; в этих случаях доминируют окислительные реакции из-за контакта с воздухом. Однако она играет важную роль при определении возможности переработки и производстве изделий. Термодеструкция может приводить к появлению в полимере функциональных групп, которые влияют на окраску и долговременную стойкость к окислению. Кроме того, она является основой некоторых технологий вторичной переработки полимерных отходов, которые включают пиролиз в инертной атмосфере для восстановления химических соединений или получения энергии
Чистая термодеструкция включает в себя реакции при высокой температуре в твердом теле или очень вязкой жидкости, и она всегда контролируется диффузией за исключением очень тонких пленок. Поскольку первичные продукты реакции захватываются полимером при высокой температуре, обычно имеют место вторичные реакции, и продукты пиролиза (и их распределение) могут очень сильно отличаться в зависимости от условий протекания реакции. Тем не менее можно выделить три основных механизма термодеструкции, которые мы рассмотрим ниже.
Разрыв цепей с деполимеризациеи
Многие полимеры с углеродным скелетом и другими простыми цепями, такие как полиацетали (полиэфиры), производятся посредством цепной реакции полимеризации или полимеризации по двойными связями, или полимеризации с раскрытием цикла. Суть полимеризации — многократное добавление мономерной молекулы к активному центру.
В принципе, любая такая реакция является равновесной и может быть записана в форме: ^
Р* + М=^: к(1
Где Рп и Р*+1 представляют продолжающуюся цепь реакций с п и м+1 мономерными единицами соответственно, а /г} и к(1 — константы скорости при полимеризации и деполимеризации. Для больших величин п (обычно п > 3-4) кр и к(! не зависят от п.
Энергии активации для реакций полимеризации и деполимеризации связаны соотношением-
Где АЕР — теплота полимеризации.
Скорости продолжения и распада растут с температурой, но, поскольку Е(1 всегда больше, чем скорость распада растет быстрее. При некоторой температуре скорости выравниваются и выше этого «потолка» Тс деполимеризация развивается быстрее, чем полимеризация. Тс — это верхний предел, при котором полимер и мономер могут сосуществовать в равновесии в присутствии активных центров. Поскольку АН[) зависит от состояния полимера и мономера, это должно отражаться в определении Тс. В табл. 2.1 приведены типичные значения Тс для распространенных полимеров [1].
Если полимер нагревается или сдвигается при температуре разрыва связей, то при этом образуются радикалы Если свободные радикалы образуются при
|
Таблица 2.1. Максимальные температуры кристаллизации распространенных полимеров
|
Температурах близких или превышающих Т, то можно ожидать быстрой деполимеризации с выходом газообразного мономера. Выход мономера при термолизе некоторых полимеров показан в табл. 2.2. Стоит отметить, что ПММА — единственный из распространенных полимеров, который полностью распадается до мономера. У других полимеров выход мономера варьируется от нуля до значительной доли в общем выходе летучих продуктов.
Причина в том, что свободные радикалы, образующиеся при разрывах цепей, также включаются в передачу цепи, как правило, с отбором водорода. Поскольку энергия активации для продолжения цепной реакции намного меньше, чем для передачи цепи, передача обычно является второстепенным процессом в химии полимеризации. Хотя энергия активации для распада выше, чем для продолжения, участие высокой температуры означает, что скорости деполимеризации и передачи цепи для большинства полимеров сравнимы при температурах термодеструкции. Вследствие этого как только образуется радикал, он включается в передачу цепи, ведущую к сложной смеси низкомолекулярных летучих продуктов. Во многих случаях эта передача цепи является внутримолекулярной «откусывающей» реакцией, приводящей к исключению короткоцепных фрагментов цепи. Существует лишь несколько полимеров, в которых передача цепи ограничена отсутствием легко отделяемых водородных атомов, распадаются чисто.
Большинство полимеров стабильно при температуре выше Тс, потому что энергия активации разрыва цепи достаточно высока, чтобы радикалы могли возникать лишь в ходе термораспада при повышенных температурах. Если радикалы генерируются в полимере при температуре выше Т у то деполимеризация может происходить очень быстро.
|
Таблица 2.2. Типичный выход мономера при пиролизе полимеров
|
Кинетика реакции деполимеризации весьма сложна; подробно она рассмотрена в [2]. В принципе, деполимеризация инициируется терморазрывами связей скелета с возникновением пары распадающихся радикалов. Таким образом, энергия активации должна быть связана с энергией диссоциации слабейшей связи в скелете, и она должна быть характерным и неизменяемым параметром полимера. На практике часто оказывается, что энергия активации растет с температурой, и она становится равной самой низкой энергии связи С—С скелета при высокой температуре. Такое поведение объясняется присутствием более слабых связей, чем средняя прочность связей, и они могут инициировать генерацию радикалов распада ири более низких температурах. Самым важным пунктом этих «слабых звеньев» является наличие концевых групп, связанных с инициатором, с передачей цепи или с остановкой. Управление этими термочувствительными группами составляет важный элемент разработки полимеров.
Статистический разрыв без распада
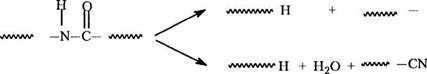
Если в полимере с углеродным скелетом происходит разрыв связей, образующиеся радикалы могут передать цепь и погибнуть слишком быстро, чтобы произошла заметная деполимеризация. В результате разрыв цепи ведет к незначительной потере молекулярной массы или потери вообще нет. Подобным образом, если полимер имеет функциональные группы в главной цепи, что типично для полимеризации по ступенчатой реакции или цепной полимеризации гетероциклических мономеров, эти группы часто являются слабейшими звеньями и могут участвовать в реакциях, которые не дают радикалов. Для таких полимеров типична термодеструкция без значительного выхода летучих продуктов. Примерами могут служить полиэфиры, полиамиды и полиуретаны; у всех термолиз идет посредством молекулярной реакцией по функциональным группам (схема 2.1).
О
Н
'ЛЛЛЛЛЛСН2—СН2—С—О—СН2‘ЛЛАЛЛ^ —► ,лллллл СН2—СН2—СООН + Н2С:=СНЛЛЛ^'
|
«ЛЛЛЛЛЛЛ ^__ 0 0. |
|
|
|
Ллллллл_ЫСО + НО-тЛЛЛЛЛЛЛ |
|
N00 |
Статистический разрыв также типичен для деструкции полимеров при взаимодействии связей цепей с другими реагентами. Гидролитическая и прочие химические реакции, а также биологическое воздействие часто дают чисто статистические разрывы благодаря тому, что доступность цепи для агрессивного агента не ограничена, скажем, кристалличностью.
Термическая реакция без разрыва цепи
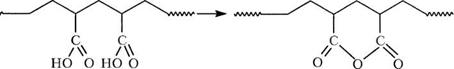
В любом полимере химические изменения, происходящие с наибольшей скоростью при данной температуре, будут самой главной причиной изменения его свойств. Часто это реакции с разрывом цепей, которые обсуждались выше. Однако имеется много примеров тому, что реакции заместителей происходят до разрыва или конкурируя с ними. В этих случаях степень полимеризации остается той же самой, но по полимерной цепи формируются новые структуры. Например, в полимерах, содержащих группы карбоновой кислоты, происходят реакции присоединения с образованием ангидридов при сравнительно низких температурах. Образование ангидрида может быть как внутримолекулярным, так и межмолекулярным; в последнем случае возникает сшивка.
|
Схема 2.2 |
Возможно, что наиболее частой заместительной реакцией в полимерах с углеродным скелетом является реакция удаления с образованием двойной связи. Классический и наиболее важный пример — дегидрохлорирование ПВХ, который формально выглядит следующим образом:
НС1
С1 С1 С1 С1 С1
Схема 2.3
Существенной чертой является образование полиеновых последовательностей посредством последовательных исключений. Они поглощают видимый свет, отчего полимер желтеет и, в конечном счете, становится черным. Подобные реакции имеют место во многих полимерах, в частности, в поливинилацетате и эфирах целлюлозы, и они играют важную роль для полимеров, которые могут удалять воду (например, поливиниловый спирт и целлюлоза). Если реакции удаления позволяют идти до высокой степени конверсии, то полимер обуглива-
Ется (карбонизируется), и в такой форме может быть весьма термостабильным. Другим примером полимера, который дает окрашивание, является полиакршто - нитрил. Этот эффект обычно относят к образованию сопряженных, циклических структур в результате внутри - и мсжмолскулярных реакций нитрильных групп.
Дегидрохлорирование ПВХ является важным процессом, поскольку это основной путь деструкции производимого в больших количествах полимерного материала; при этом выделяется вызывающий коррозию химически активный газ. Деструкция ПВХ многократно описана [3, 4]; реально ее механизм намного сложнее, чем предполагается приведенным выше уравнением. Деструкция инициируется реакционно активными дефектами цепи, а катализатором служит выделенная соляная кислота. До настоящего времени продолжается дискуссия об относительной важности ионного и свободнорадикального механизмов. Реактивные ячейки включают участки исходного полимера, такие как акриловые или третичные атомы хлора, образовавшиеся в результате передачи цепи или остановке реакции во время полимеризации, а также гидропсроксигруппы, возникающие при термодеструкции по время производства.