ТЕХНОЛОГИЯ МИНЕРАЛЬНЫХ УДОБРЕНИЙ
О РОЛИ ПРИМЕСЕЙ В ПРОЦЕССЕ ВАКУУМ-УПАРКИ ФОСФОРНОЙ КИСЛОТЫ*
Выделение соединений фтора в газовую фазу при кон-^ центрировании растворов экстракционной фосфорной кис4 лоты от 27—30 до 50—54% Р2О5 является одним из наибо - лее распространенных методов извлечения и утилизации этого ценного компонента природного фосфатного сырья. Однако вакуум-упарку фосфорной кислоты, которая может быть получена при переработке бедных доломитизированных^ фосфоритов и характеризуется высоким относительным содержанием примесей соединений магния, считают невозможной [1—3], поскольку такие растворы уже при концентраций 38—4з% Р2О5 способны превращаться в вязкую малоподвиЖ' ную массу [4, 9]. Показано, что причиной загустевания яв-J ляется образование в процессе упарки коллоидного раствора фторида магния в фосфорной кислоте, превращающегося при охлаждении в структурированный гель. Последнее наблюдали [5] при сравнительно высоких концентрациях магния (мае. отношение MgO:P205~0,l и более).
В растворах экстракционной фосфорной кислоты, получаемых при переработке доломитизированных фосфоритов, наряду с соединениями магния, присутствуют примеси соединений и других металлов, которые, судя по имеющимся данным, также оказывают существенное влияние на парциальное давление паров фтористых соединений [6, 8], кристаллизацию твердых фаз [7] и физические свойства растворов [10]. Данных, позволяющих количественно оценить влияние всех указанных примесей на показатели вакуум - \ парки, в литературе не имеется.
Нами изучено влияние примесей соединений алюминия, железа и магния на выделение фтора в газовую фазу при вакуум-упарке модельных растворов, а также определена вязкость фосфорной кислоты концентрации 51—54% Р2О5. Для приготовления исходных растворов использовали термическую фосфорную (ч), серную (х. ч.), кремнефтористо - водородную (ч) кислоты, окись (ч) и сульфат (х. ч.) магния, гидроокиси железа (ч) и алюминия (х. ч.). Концентрации примесей варьировали в диапазоне (мае. %): MgO — 0.5—3,1, Р2Оз — 0,5—2,7, S042- — 0—7,6. Указанные пределы соответствуют возможному диапазону изменений состава экстракционной фосфорной кислоты, которая может быть получена, например, при переработке фосфоритов Каратау.
Методика проведения опытов следующая. Навеоку исходного раствора, содержащего около 30% Р2О5, упаривали при остаточном давлении 34,8-103—21,3-103 Па в термостатированном стальном реакторе (внутренняя поверхность реактора защищена пленкой напыленного фторопласта) до концентрации 51—54% Р2О5 Затем раствор выдерживали под вакуумом в течение 60 мин, добавляя воду для поддержания примерно постоянной концентрации.
Растворы упаренной кислоты анализировали на содержание Р2О5, фтора и соответствующих примесей по известным методикам [11, 12], а также определяли их кинематическую вязкость при 25, 40, 60 и 80 °С. Кроме того, фиксироівали поведение растворов (наличие или отсутствие загустевания) при их длительном (в течение 20—30 сут) хранении.
Усредненные данные по влиянию примесей полуторных окислов на процесс вакуум-упарки растворов фосфорной кислоты (табл. 1) показывают, что соединения железа даже
|
Таблица 1 Влияние примесей соединений алюминия и железа на выделение фтора в газовую фазу при вакуум-упарке и вязкость образующихся растворов Фосфорной кислоты
|
При значительных концентрациях (2,7% Fe203 в исходной и соответственно 4,6% в упаренной кислоте) не уменьшают степени выделения фтора (Кг) в газовую фазу — последняя составляет 96% (при упарке растворов, не содержащих примеси полуторных окислов, Кг равна 97%). В отличие о-в этого соединения алюминия заметно повышают остаточное (после упарки) содержание фтора в кислоте и снижают era выделение в газовую фазу. Так, при наличии в исходной кислоте 1,2—2,6% А1203 степень выделения фтора при упарке уменьшается до 81—77%. Такая же величина К? получена при концентрировании раствора, содержащего одновременно 0,9% Fe203 и 0,9% А1203. Очевидно, указанное влияние соединений алюминия обусловлено образованием достаточно прочных ионов A1F2+ [7, 10], способствующих снижению парциального давления паров SiF4 и HF над фосфорнокислот - ными растворами. Аналогичное предположение высказано в работе [13] на основе данных о выделении фтора при барботаже воздуха через нагретые до 100—130 °С растворы смесей фосфорной и кремнефтористоводородной кислот, нейтрализованных ионами Ca+Z, Fe+3, А1+3.
Примеси соединений железа и алюминия заметно увеличивают вязкость упаренной кислоты. Например, кинематиче - екая вязкость растворов, охлажденных до 25°С (см. табл. 1), возрастает в ~3,8 (при 2,7% Fe203 в исходной кислоте) и в ~4,8раза (при 2,6% А1203) по сравнению с вязкостью кислоты, не содержащей ионов Fe+3 и А1+3. Отметим, что в упаренных растворах, содержащих ~4,8% Fe203, при охлаждении до 18—25 °С имело место выделение игольчатых (/=60—120 мим, Ь — 2—3 М'КМ) кристаллов фосфатов железа. В отличие от этого в алюминийсодержащих растворах (~4,2% А1203) наблюдали образование очень мелких кристаллов лишь при длительном (более 2—3 сут) хранении. Однако загустевания кислоты при охлаждении и длительной выдержке в обоих случаях не отмечено.
При изучении влияния примесей соединений магния для приготовления исходных растворов использовали сульфат магния MgS04-7H20 (табл. 2, № 1—5) либо окись магния и серную кислоту (см. табл. 2, № 6—15). В последнем случае варьировали мольное отношение Mg0/S03.
Как видно из представленных в табл. 2 данных, сравнительно небольшие (до 1,7% в пересчете на MgO) добавки сульфата магния практически не оказываются на степени выделения фтора в газовую фазу. Величина Kf заметно уменьшается (от 96—98 до 90%) лишь при содержании MgO, равном 3,1. Однако и в этом случае степень выделения фтора значительно больше, чем полученная ранее [5] в опытах по упарке фосфорнокислотных растворов кремне - фторида магния с добавками окиси магния.
Таким образом, наличие в растворе ионов S042- одновременно с катионами Mg2+ уменьшает отрицательное воздействие последних на выделение фтористых соединений в газовую фазу. Это подтверждается, например, результатами опытов с растворами, содержащими 1,8% MgO и различное количество S042- (см. табл. 2, № 12—15). Как видно, в отсутствие сульфатов степень выделения фтора при упарке раствора составляет всего 81%, а введение серной кислоты повышает Ky на 11—14% (до 92—95%)- Однако при высоких концентрациях примеси магния даже наличие сульфат-иона в упариваемых растворах не позволяет достигать достаточно полного выделения фтора (см. табл. 2, № 5, 11).
На рис. 1—2 сопоставлено влияние исследованных примесей на степень выделения фтора и реологические свойства концентрированной фосфорной кислоты, содержащей 4—5% S042-. Как видно из рис. 1, при одинаковой степени нейтрализации 1-го водородного иона фосфорной кислоты (вели-
|
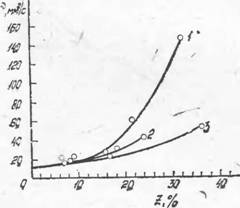
Рис. 1. Влияние степени нейтрализации фосфорнокислотных растворов соединениями железа (/), магния (2) и алюминия (3) на выделение фтора (Кр. %) в тазовую фазу при вакуум-упарке |
|
Рис. 2. Зависимость кинематической вязкости (v, мм2/с) упаренных растворов от степени нейтрализации фосфорной кислоты соединениями магния (1), железа (2), алюминия (3) |
Чина z, %, рассчитана без учета наличия серной кислоты в упариваемых растворах) примесь алюминия в наибольше? мере снижает степень выделения фтора в газовую фазу, Введение в исходную кислоту соединений железа, так ж«
|
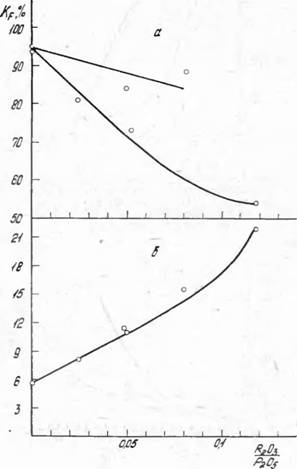
Рис. 3. Совместное влияние соединении магния и железа (/), магния и алюминия (2) на степень выделения фтора (а) при вакуум-упарке н вязкость (б) концентрированной фосфорной кислоты |
Как и небольших количеств соединений магния (2^10%), практически не сказывается на величине Кт - При дальнейшем повышении степени нейтрализации кислоты примесью магния (от 11 до 30%) /(F резко снижается (от 95 до 80%)- g отличие от этого соединения алюминия заметно уменьшают степень выделения фтора уже при сравнительно небольших степенях нейтрализации фосфорной кислоты.
Сопоставление влияния примесей на реологические свойства концентрированных растворов (см. рис. 2) показывает, что при степени нейтрализации до 16—18% все они примерно одинаково повышают кинематическую вязкость v, мм2/с (от 15 до 22 мм2/с).
При дальнейшем увеличении степени нейтрализации очень резко возрастает вязкость магнийсодержащих растворов, достигающая при г—32% более 150 мм2/с. Несомненно, в данном случае сказывается появление фторида магния. Это подтверждается тем, что при введении сульфата магния увеличение вязкости по мере повышения отношения MgO: Рг05 еще более значительно (см. табл. 2, № 1—5).
На рис. 3 и в табл. 3 представлены данные о совместном влиянии соединений магния и железа, магния и алюминия на вязкость концентрированной фосфорной кислоты и на выделение фтора при упаривании. Как видно, даже при сравнительно небольших концентрациях примеси магния
(массовое отношение MgO: Р205 =0,06) увеличение содержания ионов алюминия резко уменьшает выделение фтора — Кг при 2,4% А1203 (А1203: P20s~0,08) снижается до 54%. В отличие от этого совместное присутствие соединений железа и магния в упариваемой кислоте приводит к сравнительно небольшому снижению степени выделения фтора в газовую фазу. Так, при отношениях MgO: Р205~0,06 и Ре2Ъ3: Р205~0,09% Kf=89%, т. е. уменьшение выделения фтора в газовую фазу происходит только за счет наличия в кислоте примеси магния.
Кинематическая вязкость упаренных растворов, содержащих 3,1—3,2% MgO, увеличивается по мере повышения концентрации как Fe203, так и А1203 примерно в равной степени. При отношении R203: Р205, равном 0,11, вязкость кислоты при 25°С достигает ~467 мм2/с, что в ~15 раз больше вязкости растворов, не содержащих этих примесей.