Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ВОЗГОНКИ ФОСФОРА ИЗ ФОСФАТОВ КАЛЬЦИЯ
Суммарная реакция восстановления трикальцийфосфата углеродом выражается уравнением 47>48:
Са3(Р04)2 + 5С = Р2 + 5СО + ЗСаО(— 418,9 ккал)49 (—413,0 ккал)50 (1)
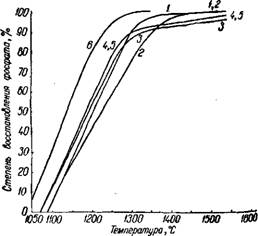
Реакция начинается (без флюсов) при 1100° и при 1400° завершается в течение 1 ч (рис. 260) 51~60.
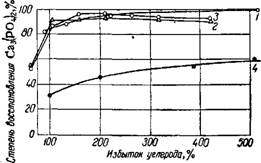
С увеличением количества углерода степень восстановления трикальцийфосфата растет (рис. 261 ) 49, 61 При высоких температурах (1500— 1550°) влияние избытка углерода менее заметно52. Большое значение имеет природа углерода. Чем мельче кристаллики графита, тем выше его химическая актив
Ность 51, 52, 61, 62_ По возрастанию восстановительной способности углеродистые материалы располагаются в ряд: кокс нефтяной, графит, антрацит, кокс металлургический, древесный уголь.
|
Рис. 260. Влияние температуры иа степень восстановления фосфатов кальция (в течение 60 мин): /—синтетический Саз(Р04)2; 2 —синтетический Ca5(p04)3F; 3 — апатито-нефелииовая руда; 4 — вятский фосфорит; 5 —фосфорит Каратау; 6 — синтетический Са4Р209. |
На практике возгонку фосфора осуществляют с введением В шихту кремнезема в качестве флюса. Исследовалось также
применение глинозема и алюмосиликатов60. Влияние флюсов объясняется тем, что они, связывая окись кальция, смещают равновесие реакции в сторону образования фосфора. Процесс восстановления в этих случаях может быть представлен следующими уравнениями: Ca3(P04)2+5C + 2Si02 = P2 + 5C0 + Ca3Si207(—368,9 ккал)49 (—348,8 ккал)50 (2) Са3(Р04)2 + 5С + ЗА1203=Р2 + 5С0+3(А1203- СаО) (—386,0 ккал)50 (3)
В присутствии кремнезема восстановление идет при более низких температурах49-61: от 1000 до 1200—1300°. Установлено52-63 что при восстановлении трикальцийфосфата образуется преимущественно трикальцийдиси - ликат Ca3Si207, другие же силикаты, в частности ме- тасиликат CaSiCb, могут образовываться в результате вторичных реакций.
Кремнезем, введенный в шихту в количестве большем, чем нужно для образования трикальций - дисиликата и не прореагировавший с последним — возгоняется, загрязняя фосфор64. Степень восстановления трикальцийфосфата возрастает с увеличением отношения Si02:Ca0 в шихте. Влияние SiC>2 становится мало заметным (особенно при температурах выше 1300°) при количестве SiC>2, большем чем в трикальцийдисиликате49-61.
В присутствии SiC>2 облегчается также удаление из печи извести, которая в этом случае выпускается в виде легкоплавкого шлака— силиката кальция. На рис. 262 видно, что температура плавления шлака зависит от соотношения в нем Si02: СаО. О составе шлака судят по показателю кислотности—отношению весового содержания Si02 и СаО. Например, для метасиликата кальция, плавящегося при 1540° и содержащего 51,7% Si02 и 48,3% СаО, показатель кислотности равен 1,07. Шлаки с меньшим показателем кислотности, содержащие больше СаО, чем метасиликат, называются основными, а шлаки с большим показателем кислотности кислыми.
Основные и кислые шлаки, показатель кислотности которых меньше или больше 1,07, плавятся при температурах более низких, чем метасиликат кальция.
|
Рис. 261. Влияние избытка углерода на увеличение степени восстановления трикальцийфосфата. Продолжительность нагрева 60 мин: 1 — Саз(Р04)2 + хС, 1400°; 2 - Са3(Р04)2 + хС + 3 Si02, 1300°; 3 — Са3(Р04)2 + яС 4- 2 Si02, 1300°; 4-Са3(Р04)2+ + xC + 3Si02, 1200°. |
Глинозем и алюмосиликаты также положительно влияют на восстановление трикальцийфосфата, но в меньшей степени, чем
кремнезем61> 65~67. Для восстановления имеет значение и природа флюсов. Аморфные двуокись кремния или глинозем дают при прочих равных условиях более высокую степень восстановления, чем кристаллические61,66-69. Щелочные соли повышают степень восстановления трикальцийфосфата углеродом, особенно при низких температурах 65,70~73.
Приведенные выше суммарные уравнения реакции восстановления трикальцийфосфата углеродом не дают представления о механизме процесса, взгляды на который различны 74~91.
Установлено, что при термическом получении фосфора из шихты апатита и углерода в присутствии Si02, последняя не может вытеснять Р4Ою из апатита даже при 1400°. При температуре выше 1000° апатит реагирует с Si02, образуя CaSi03 и Са3(Р04)2 с выделением Н^О и SiF4. Затем Са3(Р04)2 восстанавливается углеродом (легче, чем апатит), а избыток окиси кальция реагирует с Si02, образуя легкоплавкий шлак.
|
1000, |
|
Рис. 262. Диаграмма плавкости в системе Si02—СаО. |
Восстановление фосфатов водородом, природным газом и другими газообразными реагентами протекает значительно медленнее, чем твердым
Углеродом. Показано92, что в присут ствии природного газа при температурах до 1250° (до оплавления шихты) восстановление идет преимущественно углеродом, отлагающемся при пиролизе метана на поверхности и в порах фосфорита; при температурах выше 1300° — водородом, образующимся при пиролизе метана. Для промышленных процессов, протекающих при 1400— 1450°, продувание шихты метаном нецелесообразно, так как восстановление за счет водорода идет медленнее, чем металлургическим коксом. В то же время выделившийся при пиролизе метана углерод обладает большей восстанавливающей способностью, чем кокс. Взаимодействие природных фосфатов с газообразными восстановителями ускоряется в присутствии солей натрия и магния, снижающих температуру плавления шихты93. Из щелочных солей наиболее активно действует94 добавка Na2S'04. Максимальное влияние флюсов наблюдается при температуре плавления шихты (- 1300°).
Восстановление фосфатов газами связано с необходимостью применения большого избытка восстановителя (20—30-кратного количества) и громоздкой аппаратуры95.
Скорость реакции восстановления трикальцийфосфата углеродом лимитируется диффузией реагирующих компонентов 52-60'96. Опытные данные подтверждают, что факторы, ускоряющие диффузию в твердых телах, повышают степень восстановления трикальцийфосфата углеродом. Степень восстановления возрастает с уменьшением размера частиц шихты. Особенно показательно положительное влияние брикетирования шихты. Скорость диффузии, а следовательно и восстановления, растет с увеличением температуры. Введение в шихту флюсов, образующих полиэвтектические смеси, ускоряет процесс. Температура превращения кремнезема в менее плотные модификации совпадает с начальной температурой восстановления трикальцийфосфата в присутствии кремнезема (900— 1000°). Ускорение диффузии может быть объяснено внутрикристал - лическими превращениями. Взаимодействие между фосфатом и коксом в присутствии кварца, сопровождающееся кристаллохими - ческими превращениями с образованием соединений промежуточных степеней окисления фосфора, протекает главным образом в расплаве90. Только до его появления идет прямое восстановление фосфата окисью углерода и углеродом в результате диффузии в твердых фазах.
В процессе возгонки протекают побочные реакции. При температуре выше 1600° и большом избытке углерода происходит образование фосфида и карбида кальция: •
Са3(Р04)2 + 8С = С. а3Р2 + 8СО Са3Р2 + 6С = ЗСаС2 + Р2
Содержащаяся в фосфатах окись железа связывает часть фосфора в фосфиды железа, например:
Fe203 + ЗС = 2Fe + ЗСО
4Fe + P2 = 2Fe2P
Они выпускаются из печи в расплавленном виде и застывают в чугунноподобную массу — феррофосфор.
Существенное значение имеет возгонка щелочей и выделение фтористых соединений:
2CaF2 + Si02 = 2СаО + SiF4
Четырехфтористый кремний при конденсации фосфора поглощается водой с выделением кремневой кислоты, которая загрязняет продукт. Содержащиеся в сырье сульфиды и сульфаты образуют сероводород. Идет также разложение карбонатов; выделяющаяся при этом двуокись углерода восстанавливается до окиси. Имеющаяся в шихте влага реагирует с фосфором, образуя фосфористый водород и фосфористую кислоту, что снижает выход фосфора. Для уменьшения потерь фосфора сырье подвергается иногда предварительной прокалке.