Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
СОЛИ ХРОМА
Из соединений хрома наибольшее промышленное значение приобрели натриевые и калиевые соли хромовых кислот, в особенности соли двухромовой кислоты — хромпики — ЫагСггО; • 2Н20 и К2СГ2О7, а также хромовые квасцы и основные сульфаты хрома (сухие хромовые дубители), хлорный хром, окись хрома и хромовый ангидрид. Современная технология этих продуктов разрабатывалась в СССР главным образом в Уральском научно-исследовательском химическом институте и на предприятиях и наиболее полно отражена в монографии
Физико-химические свойства
Хром образует с кислородом окислы СгО, Сгг03, СгОг, Сг03 и перекиси Сг04, Сг05; из них наибольшее практическое значение имеют Сг203 и Сг03 и их соединения.
Закись хрома СгО черного и красного цвета, не растворима в воде и в разбавленных кислотах. Гидрат закиси хрома Сг(ОН)з желто-коричневого цвета, разлагается в воде и при нагревании; растворим в концентрированных кислотах.
Окись хрома Сг203 зеленого цвета кристаллизуется в гексагональной системе, имеет плотность 5,21 г]см3, плавится при 2435°2. Температура кристаллизации окиси хрома несколько изменяется в зависимости от условий ее получения3. Состав гидратов окиси хрома окончательно не установлен. По разным данным гидраты окиси хрома могут содержать от одной до девяти молекул воды, в зависимости от условий получения4. Разноречивы и данные о температурных интервалах существования отдельных гидратов5-10. Так, например, по одним данным8 в системе Сг203—Н20 существуют три стабильные фазы: Сг(ОН)3, СгООН и а-Сг203; граница между Сг(ОН)3 и СгООН лежит при ~55°, а между СгООН и а-СггОз при ~540° и мало смещается при повышении давления.
По другим данным 9 стабильной является и Сг203 • 5Н20, устойчивая между 68 и 85—95°, а Сг(ОН)3 устойчива до 150°, СгООН образуется при 320—360° под давлением 320—350 ат. Данные других авторов отличаются от приведенных. Прокаленная окись хрома в воде не растворима и плохо растворяется в кислотах. Гидроокись хрома растворяется в кислотах с образованием солей трехвалентного хрома, а с сильными основаниями образует хромиты: Сг(ОН)3 + 3NaOH - Cr(ONa)3 + 3H20
Зеленая или фиолетовая окраска солей трехвалентного хрома, их кристаллическая форма и свойства зависят от возникновения тех или иных комплексных структур. Например, гексагидрат хлорного хрома СгС13-6Н20 имеет две структуры — зеленую [СгС12(Н20)4]С1 • 2Н20 и фиолетовую (называемую также серой) [Сг(Н20)б]С1з п'12- Безводный хлорный хром образует красно-фиолетовые кристаллы (Tasi 1152°), легко возгоняющиеся в токе хлора; начинает реагировать с кислородом при 350° (СгС12 — при 404°); при 514° восстанавливается водородом до СгС12; перегретым водяным паром при 350—450° разлагается на Сг203 и НС113. Растворимость СгС13 в воде очень мала (почти не растворим), но увеличивается в присутствии следов СгС12. Растворимость зеленого СгС13 • 6Н20 при 15° около 130 г в 100 г воды. Гидролиз СгС13 в водных растворах приводит к образованию при 20—30° Сг(ОН)С12, а при 40—50° Сг(ОН)2С1,4>15 • О Na3CrCl6, К3СгС16, К3Сг2С19 см. 'е.
Сульфат хрома, получаемый растворением гидроокиси хрома в серной кислоте, выделяется из раствора в виде темно-фиолетовых кристаллов Cr2(S04)3 • 18Н20 17>18. Они плавятся при 80—85° с отщеплением 10 молекул воды; остальные 8 молекул воды удаляются при 110—115°. Сообщают также19, что Cr2(S04)3 • 18Н20 при нагревании отщепляет только 16 молекул воды, при дальнейшем же обезвоживании выделяется S03 и образуется основная соль Cr20(S04)2 устойчивая в интервале температур 460—640°. По другим данным 20 фиолетовый сульфат хрома, полученный введением » эквивалентного количества H2S04 в охлажденный раствор Cr(N03)3, имеет состав Cr2(S04)3 • 15Н20; при 90—95° он переходит в девятиводный, при 120° — в шестиводный кристаллогидрат, а полная дегидратация протекает при 400° и не сопровождается гидролизом. Разложение обезвоженного сульфата до Сг203 протекает при 700—735°.
Зеленая модификация сульфата Сг3+ получается при восстановлении Gr03 в сернокислом растворе. При этом обычно образуется пересыщенный раствор, превращающийся при выпаривании в темно-зеленую 21 вязкую массу, а после высушивания ее в стекловидное вещество состава Cr2(S04)3 • 8Н20. Эта соль теряет 2,6 молекулы воды при 120—125°, остальная вода удаляется только при 440—445°18. Описаны22 кислые сульфаты трехвалентного хрома
3Cr2(S04)3-S03, Cr2(S04)3-S03, 3Cr2(S04)3-2H2S04-3H20 серо - зеленого цвета, не растворимые в воде, выделяющиеся в мелкокристаллическом виде при кипячении с серной кислотой бихроматов К, NH4 и окиси хрома.
Хромовые квасцы — двойные соли сульфата трехвалентного хрома и сульфатов Na, К, NH4 и других — имеют состав M2S04 • Cr2($04)3 • 24Н20. Растворимость квасцов в воде резко возрастает с повышением температуры. Они кристаллизуются в виде темно-фиолетовых октаэдров. Водные растворы также имеют фиолетовую окраску, но при нагревании они становятся зелеными вследствие диссоциации двойных солей (для хромово-калиевых квасцов выше 78°). При выпаривании растворов выделяется аморфная зеленая масса. Калиевые квасцы имеют плотность 1,84 г/см3, плавятся при 89°; в 1 л насыщенного водного ра:тсора содержится при 25° 243,9 г K2SO4 • Cr2(S04)3 • 24Н20 (аци 1Г5,1 г безводной соли). Аммониевые квасцы имеют плотность 1,72 в/слг3, Разлагаются при 100°; растворимость при 25° 21,2 г в 100 в воды.
Описано получение некоторых аммиакатов трехвалентного хрома - [Cr(NH3)e]2(S04)r2H2S04-3H20, [Сг(NH3)6}2(S04)3 • H2SO<, [Сг (NHS) e]2 (S04) 3 • 5Н20, [СГ (NH8) 5Н20] (N03) 3, [СГ (NH3) 5H20]C1s. • СиС12. Последний, в отличие от нитратного комплекса, устойчив при хранении. Осажденная аммиаком из хромовых квасцов гидроокись хрома при нагревании в течение 1 ч до 40—45° образует раствор аммиаката 23.
В системе Сг203—S102 установлено существование соединения Сг203 • 3Si02, плавящегося без разложения при 1995°; имеются две эвтектики — при 1750° (65 мол. % Cr2Os) и при 1680° (5 мол. % Сг203)
Хромовый ангидрид Сг03 красного цвета кристаллизуется в ромбической сингонии, имеет плотность 2,7 г/см3, при 170° незначительно разлагается в твердом состоянии, в связи с чем плавится при непостоянной температуре в пределах 180—202°; расплавленный склонен к переохлаждению и затвердевает около 170°8. Является сильным окислителем. Растворимость в воде при 0° 61,7%. при 100° 67,46% Сг03 25. При растворении в воде образует хромовую кислоту Н2Сг04, в свободном виде неизвестную. В системе Cr03—H2S04—H20 существуют твердые фазы Сг03 и Сг03 • S03 2б.
При растворении СЮ3 в разбавленной серной кислоте (до ~30% H2S04) протекают процессы полимеризации с образованием иона Сг20^" и ассоциации с образованием иона HCr2Oj и не- Диссоциированной двухромовой кислоты:
2НОСГ СГ2027- + Н20 Сг202- + Н+ HCrjOf HCr2Of + Н+ H2Cr207
В растворе, содержащем от 30 до 55% H2S04, кроме двухромовой кислоты, образуется, по-видимому, также хромосерная кислота 27 •
Сг03 + H2S04 H2CrS07
Предполагают, что в растворах с концентрацией больше 55% H2S04 идет дальнейшее присоединение серной кислоты к хромосер - ной кислоте
H2CrS07 + H2S04 Cr02(HS04)2 + H20 Дальнейшая полимеризация
2Н2Сг207 + H2S04 H2Cr40I3 + H2S04-H20 H2CrS07 + H2Cr2Or H2Cr3S0I3 + H20
И дегидратация хромосерной кислоты:
2H2CrS07 + H2S04 2(Сг03 • S03) + H2S04 • 2Н20
В растворах, содержащих H2S04-2H20, т. е. при концентрации, большей 73% H2S04, хромовый ангидрид неустойчив. Цвет таких растворов постепенно из оранжевого переходит в зеленый. Вообще при взаимодействии с сильными кислотами при нагревании Сг09 образует зеленые или фиолетовые соли этих кислот, например Cr2(S04)3. При нагревании водного раствора хромовой кислоты до 300—325° в закрытом сосуде (при равновесном давлении кислорода 50—200 ат) она разлагается с образованием осадков Сг02 и HCr02 29.
При термическом разложении хромового ангидрида при нормальном давлении образуются: декахромат хрома Сг2(Сг10О31)3 =■ = CrO2>906, бихромат хрома Сг2(Сг20?)3 = Сг02>625 и монохромат хрома Сг2(Сг04)3 = Сг02,4о, а также твердые растворы в пределах от Сг03 до Сг02,98 и от CrOi,54 до CrOi, B0. Под давлением образуется также двуокись хрома Сг028>30'31. О перекисях и перекис - ных соединениях хрома см. 32~34.
Оксихлорид хрома Сг02С12, или хлористый хромил, — темно - красная жидкость с плотностью 1,911 г/см3 при 20°, плавится при '—96,5°. Давление пара в (Ммрт. ст.): 10 при 13,8°, 100 при 58°, 400 при 95,2°, 760 при 117,1° (TK). Водой, а также на свету и при нагревании разлагается. Образуется при взаимодействии газообразного НС1 и Сг03 или при обработке концентрированной серной кислотой смеси бихромата и хлорида.
В системе Сг03—HF—Н20 при 0° существуют две твердые фазы— Сг03 и Cr02F2 35. Последний плавится (под давлением) при 31,6".
Соли хромовой кислоты имеют желтую окраску, двухромовой — оранжево-красную. Концентрированные растворы Na2Cr04 и К2Сг04 имеют рН 9, Na2Cr207 и КгСггО? — около 4 зб. Кислая Реакция двухромовокислых солей обусловлена взаимодействием
Ч2-
Иона Сг207~с. водой с образованием ионов Н+ и Сг04 .причем уст. навливается равновесие:
|
Cr2Of" + Н20 |
|
2НСг07 |
2Н+ + 2СгО?~
При прибавлении к раствору какой-либо кислоты (ионов Н+) равновесие сдвигается влево; при прибавлении какой-либо щелочи
(ионов ОН")—вправо. Это позволяет переводить монохроматы в бихроматы и наоборот путем изменения рН раствора. В кислой среде бихроматы являются сильными окислителями; при их восстановлении образуются соединения трехвалентного хрома.
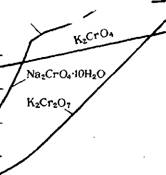
Хромат (монохромат) натрия Na2Crl04 кристаллизуется из водных растворов до 19,52° в виде моноклинных сильно гигроскопичных (расплывающихся на воздухе) кристаллов декагидрата Na2Cr04 • ЮН20 с плотностью 1,483 г/см3-, в пределах от 19,52 до 26,6° (25,9°) кристаллизуется гек - сагидрат Na2Cr04 • 6Н20, от 26,6 до 62,8° — Na2Cr04 • 4Н20. Выше 62,8° образуются ромбические кристаллы безводного a-Na2Cr04, переходящие при 413° в гексагональные p-Na2CrC>4, плавящиеся при 792°. Растворимость хромата натрия в воде 24,2°/о при 0°, 44,3% при 20° и 56,1% при 100° (рис. 168). В системе Na2Cr04— Na2S04—Н20 при 15° твердая фаза представляет собой непрерывный ряд смешанных кристаллов декагидратов хромата и сульфата натрия, а при 25° кристаллизуются твердый раствор Na2S04-10H20—Na2Cr04 • 6Н20, безводный Na2S04 и Na2Cr04 • 6Н20 (рис. 169 ) 37-38. В системе Na2Cr04— Na2C03—Н20 при 35° кристаллизуется Na2Cr04 • 4Н20, Na2C03- • Н20 и твердый раствор беркеитового типа, образуемый двойной солью 2Na2Cr04• Na2C03 и исходными безводными солями39.
|
90 |
|
NazCrA |

|
Na2CrO« Na2Cr04 • 4Н;0 |
|
80 |
|
70 |
|
60 |
|
20 40 ВО 80 Температура,"С |
|
NaiCr04-6H|tQ^ |
|
6 50 |
|
5 I. 40 о «о £ G Зо Е. |
|
20 |
|
Ю |
|
100 |
|
168. Растворимость хроматов и бихроматов в воде. |
|
Рис. |
Хромат калия К2Сг04 кристаллизуется безводным. Ниже 669° устойчива ромбическая модификация, выше этой температуры — гексагональная. Плотность при 18° 2,73 г/см3; плавится при 975°. Растворимость в воде 37,1% при 0°, 45,2% при 100° (рис. 168). В системе К2Сг04—K2S04—Н20 при 25° выделяется одна твердая
фаза изоморфных солей. В системе К2Сг04—Na2Cr04—Н20 при 25° выделяются три твердые фазы: Na2Cr04 • 6Н20, ЗК2Сг04 • Na2Cr04 (хромовый глазерит) и К2Сг04. Хромовый глазерит, в отличие от сернокислого, образует двусторонний твердый раствор с пределами концентраций 3,16К : Na и 2,39К : Na. В системе КгСг04—Na2S04—Н20 при 25° имеется пять полей кристаллизации: 1) непрерывного твердого раствора хромата и сульфата калия, 2) сложного тетрагенного твердого раствора глазерита, 3) твердого раствора Na2S04 • ЮН20—Na2Cr04 ■ 6Н20, 4) безводного Na2S04 и 5) Na2Cr04- . 6Н20 38-40. При 208—220° К2Сг04 взаимодействует с расплавленным СгОз с образованием К2Сг207. При 270—280° К2Сг04 реагирует с продуктом разложения СгОз— бихроматом хрома:
3K2Cr04 + Сг2(Сг207)3 =
= ЗК2Сг207 + Сг2(Сг04)3
При этом выход К2СГ2О7 по Обеим реакциям составляет 80— 85%. Для полного превращения хромата в бихромат требуется избыток Сг03 против стехиометрического количества 4l. О свойствах безводных систем, содержащих хроматы и гидроокиси, сульфаты, нитраты, фториды натрия и калия, см.42-45.
Хромат аммония (NH4)2Cr04 выделяется из водных растворов в форме моноклинных кристаллов; плотность при 12°— 1,917 г/см3. Выше 180° и в горячих водных растворах разлагается. Растворимость в воде при 30° 28,8%.
Хромат кальция существует в пяти модификациях: СаСг04, СаСг04-0,5Н20, СаСг04-Н20, а - и p-CaCr04-2Н20. Наиболее растворим в воде а-дигидрат (14,75% СаСг04 при 0°), наименее - растворим безводный хромат кальция (4,3% СаСг04 при 0°). С увеличением температуры их растворимость несколько уменьшается. Безводный хромат кальция образуется выше 400°, двухводные гидраты — ниже 25°.
|
50- |
|
Рис. 169. Изотерма растворимости в системе NaaCr04—Na2S04—Н20 при 25°: / — твердые растворы Na2S04 * 10Н2О и, Na2Cr04 • 6Н20; 11 - Na2S04: /// — Na2Cr04 ■ 6Н20. |
Бихромат натрия Na2Cr207 кристаллизуется выше 84,6° в безводном виде, а ниже этой температуры — с двумя молекулами воды (Na2Cr207 • 2Н20) в виде моноклинных призм или тонких игл,, имеющих плотность 2,35 г/см3. Сильно гигроскопичен, на воздухе расплывается. Безводный плавится при 357°; при 400° разлагается с выделением кислорода. Растворимость Na2Cr207 в воде при 20°" 73,18%, при 100° 91,43%. Растворимость в присутствии Na2S04 ». NaCl см.46. Существуют три - и тетрахроматы натрия Na2Cr3Oi0 и.
Na2Cr40I3, которые плавятся (соответственно) при 232 и 168° и разлагаются при 337 и 320°47.
Бихромат калия КгСг207 кристаллизуется из водного раствора безводным в триклинической системе, негигроскопичен, плотность при 25° 2,68 г/см3. Существует в трех модификациях — устойчивая при обычной температуре модификация А превращается при 269° в модификацию С с увеличением объема на 5,2%; последняя при охлаждении переходит в метастабильную при обычной температуре модификацию В, которая при нагревании до 255° переходит в С с уменьшением объема на 0,1% 48. Плавится при 398°.
Бихромат калия до 800° практически не разлагается. Изополи - хроматы К2СГ3О10 и К2СГ4О13 плавятся соответственно при 243 и 210° с одновременным разложением на К2СГ2О7 и СгОз, при дальнейшем нагревании разлагается Сг03 49. Растворимость КгСг207 в воде при 0° 4,3%, при 20° 11,7%, при 100° 50,2%. Составы эвтони - ческих растворов в системе К2Сг207—K2SO4—Н2050'61: при 20° 6,24% К2Сг207 и 8,23% K2SO4, при 40° 14,40% К2СГ2О7 и 8,20% K2SO4. О растворимости в системе КгСг207—КС1—Н20 см.52. О системах (NH4)2Cr207— (NH4)2S04—Н20 и (NH4)2Cr207—NaCl—Н20 см.53-54.
Бихромат аммония (NH4)2Cr207 кристаллизуется из водного раствора в виде дигидрата и безводной соли. Плотность при 25° .2,15 г/см3. При нагревании до 185° разлагается. Растворимость в воде при 0° 15,16%, при 20° 26,67%, при 100° 60,89% (NH4)2Cr207. Обладает способностью к внутримолекулярному горению. Темпе - .ратура вспышки 240°. В простейшем виде механизм горения представляется совокупностью следующих реакций55:
(NH4)2Cr207 = 2NH3 + Н20 (пар) + 2Сг03 - 64,5 ккал
2Сг03 = Сг203 + 1,502 — 5,6 ккал 2NH3 + 1,502 = N2 + ЗН20 (пар) + 151,3 ккал
Бихромат кальция СаСг207 кристаллизуется из водного раствора от 0 до 10° в виде гексагидрата СаСг207 • 6Н20, при 20—40° в виде СаСг207 • 5Н20, при 50—60° в виде СаСг207 • 4Н20; выше 70° вследствие гидролиза
СаСг207 + н20 СаСг04 + н2Сг04
Кристаллизуется смесь бихромата и монохромата кальция66. Растворимость в воде при 0° 53,47%, при 20° 57,87%, при 60° 65,54%, при 100° 72,7% СаСг207. Бихромат кальция гигроскопичен и на воздухе расплывается. О растворимости в системе СаСг207— К2Сг207-Н20 см.57'58.
Применение
Хром и его соединения широко используются в различных отраслях промышленности59. Металлургической промышленностью Выпускаются специальные хромистые стали, отличающиеся высокой механической прочностью, жаростойкостью и антикоррозионными свойствами. Хром входит также в состав сплавов — алюминиевых, кобальтовых, титановых и др.60. Получаемый восстановлением окиси хрома углем в атмосфере водорода карбид хрома ОзС2 служит для изготовления химически и термически стойких металлокерамических сплавов (керметов), а также режущих и наплавочных твердых сплавов6l-62. Соединения хрома используются для получения хромомагнезитовых и других огнеупоров, применяемых в металлургических печах.
Окись хрома служит сырьем для получения металлического хрома (обычно алюмотермическим путем), карбида хрома, шлифовальных паст и красок, стойких к свету, огню и кислороду воздуха. Ее применяют также для окрашивания стекла и керамики. Окись хрома является компонентом весьма часто применяемых в неорганическом и особенно органическом синтезе хромовых катализаторов (для дегидрогенизации алифатических углеводородов, ароматизации парафиновых углеводородов, гидрирования и крекинга,, конверсии нефтяных газов и проч., а также для реакций изотопного обмена)8-63. Для производства металлического хрома в последнее время все шире стали использовать в качестве полупродукта хлорный хром.
Хромовые квасцы, основной сульфат хрома, хромпики и некоторые другие соединения хрома используются в качестве дубильных веществ в кожевенной промышленности и в качестве протрав и пропитывающих средств при крашении, печатании тканей в текстильной промышленности.
Хромпики служат сырьем для производства хромовых красок—■ желтого крона РЬСг04, красного крона РЬСг04 • РЬ(ОН)2, оранжевого крона (смеси средней и основной солей хромата свинца), желтых хромовых солей цинка и др. Соли хромовых кислот дают желтые, оранжевые, красные и коричневые краски; соли окиси хрома — зеленые; синие и черные краски получаются из соединений хрома и железа.
Хромпики используют также при получении некоторых органи - » ческйх красителей и для приготовления катализаторов. Хромпики применяют в жировой, спичечной, бумажной промышленности, в - электротехнике, в пиротехнике, в фотографии и в других отраслях техники, а также в сельском хозяйстве (для протравливания семян). Из хромпиков в наибольших количествах используют более Дешевый бихромат натрия.
Соединения шестивалентного хрома (хромовый ангидрид,, хоомпики, хлористый хромил) используют в качестве сильных окислителей, в частности во многих процессах органического синтеза— при получении ализарина, сахарина, бензойной кислоты, антрахинона, гидрохинона, в производстве резин, пористых пластиков.
Хромовый ангидрид используют при получении синтетического каучука, органических красителей, для очистки жиров и масел. Его водные растворы применяют для травления и гальванического хромирования металлов, для получения цветных пленок на поверхности сплавов, для электролитической полировки металлов, для электрохимической обработки режущего инструмента. Электролизом растворов хромовой кислоты получают металлический хром высокой степени чистоты.
Хромат натрия является хорошим ингибитором коррозии стали водой, содержащей до 1 % NaClв4.
Технический бихромат натрия выпускают в виде безводного кристаллического или гранулированного, водного гранулированного, а также плавленого продуктов, которые должны удовлетворять требованиям ГОСТ 2651—70 (табл. 39). Технический бихромат калия по ГОСТ 2652—71 и ГОСТ 5.991—71 выпускают высшего и первого сортов, содержащих соответственно (в %): КгСг207 не менее 99,7 и 99,3; сульфатов (S04) не более 0,02 и €,08; хлоридов (С1) не более 0,07 и 0,02; не растворимого в воде остатка не более 0,03 и 0,1; влаги не более 0,05 и 0,1.
|
ТАБЛИЦА 39 Состав технического бихромата натрня (по ГОСТ 2651—70) (содержание компонентов в %)
|
|
* Этот сорт соответствует также регламенту по ГОСТ 5.1493—72 на аттестованный продукт. |
Технический хромовый ангидрит, согласно ГОСТ 2548—62, выпускается в виде чешуек или гранул (не более 3 мм) и должен содержать в высшем, 1- и 2-м сортах, соответственно, не менее 99,5, 99,0, 98,5% Сг03 и не более 0,03, 0,06, 0,10% не растворимых в воде веществ и 0,10, 0,20, 0,40% S04. К качеству аттестованного продукта ГОСТ 5.1599—72 предъявляют следующие требования: содержание не менее 99,6% Сг03 и не более: 0,02% не растворимых в воде веществ, 0,06% S04 и 0,005% натрия.
Требования к качеству технической окиси хрома представлены в табл. 40. Помимо приведенных в ней, ГОСТ предусматривает следующие показатели: содержание цветных металлов
|
ТАБЛИЦА 40 Состав технической окиси хрома (по ГОСТ 2912—66) (содержание компонентов в %)
|
В'ОХМ-1; удельную поверхность и класс чистоты поверхности после полирования для ОХЧ; рН водной вытяжки, красящую способность, цвет и оттенок, укрывистость и крупность зерен для ОХП. В окиси хрома ОХМ-2, получаемой из хромового ангидрида, применяемой в других производствах (не для выплавки металлического хрома), допускается общее содержание серы (S) не более 0,06%.
Тарой для хромпиков, хромового ангидрида и окиси хрома служат стальные барабаны или полиэтиленовые мешки.