Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
Содово-суспензионный способ
Этот способ заключается в использовании для реакции взаимодействия с раствором соды суспензии кремнефторида натрия, что значительно сокращает объемы реакционных растворов289'290. Продукт содержит 70—75% NaF и 20—25% Si02.
Этот способ получения NaF осуществляли в аппаратуре кремне- фтористого отделения Винницкого химического комбинта следующим образом 286-291. В нагретую до 70—80° пульпу Na2SiF6 вводили постепенно при интенсивном перемешивании сухую кальцинированную соду с избытком 1—2% к стехиометрическому количеству. Соотношение Ж:Т в реакционной массе 2—2,5: 1. После получасового нагрева острым паром и проверки завершения реакции (по малиновой окраске фенолфталеина) горячую суспензию центрифугировали. Маточный раствор, содержащий до 3,5% NaF, возвращали в процесс. Продукт после центрифугирования направляли на сушку, которая затруднена его высокой влажностью (20— 25%) и присутствием большого количества гидратированной двуокиси кремния.
В дальнейшем этот процесс был усовершенствован 292_2Э6. Установлена зависимость его скорости и качества продукта от порядка сливания и интенсивности перемешивания реагентов (стр. 1129). Хорошее перемешивание не только выравнивает концентрации реагентов, но и предотвращает в некоторой мере обволакивание кремневой кислотой кристаллов Na2SiF6, что ускоряет их растворение. Оптимальная окружная скорость перемешивания 1,2—1,8 м/сек. При большей скорости масса сильно вспенивается, что осложняет ведение процесса.
При внесении Na2SiF6 в содовый раствор скорость процесса почти в 4 раза больше, чем при введении содового раствора в пульпу. Но при этом происходит интенсивное пенообразование. Поэтому вначале всю пульпу кремнефторида натрия вводят в часть содового раствора, равную одной трети от общего количества, а затем постепенно при перемешивании добавляют в массу остальное количество раствора.
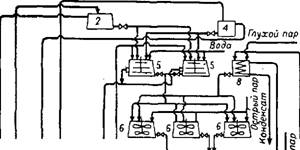
На рис. 334 изображена схема получения фторида натрия из кремнефторида натрия, по которой работал Одесский суперфосфатный завод до замены этого производства производством криолита. Эта схема позволяет вырабатывать каждый из продуктов (NaF и Na2SiF6) в отдельности или совместно. Исходным сырьем является кремнефтористоводородная кислота, полученная водной абсорбцией отходящих фтористых газов. Кремнефторид натрия получают в стальных, футерованных диабазовой плиткой мешалках-реакторах 5 емкостью по 2,7 ж3, куда подают кислоту из стального, футерованного плиткой мерника 2 (емкостью 1,9 ж3) и раствор поваренной соли из стального мерника 4 (емкостью 1,5 ж3). Полученная пульпа кремнефторида натрия может быть непосредственно переработана в товарный продукт, для чего твердую фазу отделяют от жидкости на центрифуге 7 и направляют на сушку, размол и расфасовку. Взаимодействие пульпы Na2SiFe с содовым раствором осуществляют в стальных реакторах 6 с мешалками емкостью по 2,4 ж3, обогреваемых острым или глухим паром; в последнем случае они снабжены паровыми рубашками. Обогрев глухим паром значительно уменьшает объем маточных растворов. В реактор заливают половину требуемого количества насыщенного раствора соды, нагревают его до 60—80° и загружают полную порцию пульпы кремнефторида натрия, а затем постепенно добавляют остальное количество содового раствора. По окончании реакции (через 40— 45 мин) пульпу спускают при перемешивании в центрифуги 7. Маточный раствор направляют через стальной сборник 9 в содорас - творитель 10. Отфугованный продукт высушивают в шнекОвой су
шилке. За один цикл (40—45 мин) в аппаратах указанных объемов получают 300 кг продукта. Производительность шнековой сушилки 6—8 т/сутки. Получаемый продукт содержит 72—75% NaF, 2,5— 3,5% влаги, 16—19% нерастворимого остатка (SiCb); остаток на сите № 05 0,2—0,6%. Капитальные затраты на дооборудование кремнефтористого отделения для выпуска фторида натрия во много раз меньше затрат на организацию производства фторида натрия содово-термическим способом.
|
|
.9 на сушку.
Ю
Пар ±1
В канализацию
Рис. 334. Схема реакторного отделения производства кремнефторида натрия и переработки его иа фторид натрия содово -
|
PS |
|
10 |
||||
|
Ш |
|
U F |
|
£ |
Суспензионным способом: / — сборник кремнефтористоводородной кислоты; 2 —мерник кремнефтористоводородной кислоты; 3 — растворитель поваренной соли; 4 — мерник насыщенного раствора поваренной соли; 5 —реактор для получения Na2SiF6; 6 — реактор для получения NaF; 7 — центрифуга; 8 — мерник насыщенного раствора соды; 9 — сборник маточного раствора NaF; 10 — растворитель соды; И — отстойник для сбросного раствора.
Представляет интерес отделение кремневой кислоты от NaF с помощью гидроциклона2Э6. Разделение в гидроциклоне тем легче, чем больше отличаются по размерам частицы фтористого натрия и кремневой кислоты. Наибольшая разница в размерах этих частиц достигается за счет укрупнения кристаллов NaF в процессе' нейтрализации кремнефтористоводородной кислоты содой, в частности за счет сравнительно медленного перемешивания реакционной массы294. В пульпе, поступающей в гидроциклон, отношение Ж: Т должно быть равно 6—8, для чего концентрация исходной пульпы Na2SiF6 должна быть 100—80 кг/м3. При диаметре гидроциклона 45 мм его производительность 4—4,5 м3/ч пульпы, что
Соответствует 7—10 т/сутки продукта с содержанием до 90% NaF. Потери NaF со сливом меньше 8—10% от количества, поступающего на обогащение. Повторное пропускание слива через гидроциклон позволяет извлечь основную часть NaF.
Описан способ флотационного разделения NaF и БЮг 297.
Освобождение фтористого натрия от Si02 может быть достигнуто при обработке щелочью — образуется раствор жидкого стекла, который отделяется от нерастворяющегося NaF. Получающийся продукт содержит 94—99% NaF. Необходимость утилизации отхода — раствора жидкого стекла осложняет организацию этого процесса80.
Поташный способ
Поташный способ 298,299 производства NaF заключается в конверсии кремнефторида калия оборотным раствором поташа, разделении образовавшегося раствора фторида калия и выделившейся кремневой кислоты, конверсии фторида калия содой с осаждением NaF и отделении от растворимых калиевых соединений осадка NaF.
Исходный кремнефторид калия может быть получен осаждением хлористым калием из раствора кремнефтористоводородной кислоты
TOC o "1-3" h z H2SiF6+2KCl = K2SiF6 + 2HCl (1)
Или абсорбцией газообразного четырехфтористого кремния оборотным раствором поташа:
3SiF4 + 2K2C03 = 2K2SiF6+2C02 + Si02 (2)
Дальнейшие стадии процесса в обоих случаях характеризуются следующими уравнениями:
K2SiF6 + 2К2С03 = 6KF + Si02 + 2СОг (3)
6KF + 3Na2C03 ЗК2С03 + 6NaF (4)
Весь раствор углекислого калия, образующийся в процессе конверсии фтористого калия, полностью возвращается на реакции (2) и (3); если для получения кремнефторида применяется хлористый калий, '/з этого раствора должна быть переработана на товарный поташ.
По обоим вариантам образуется осадок аморфной кремневой кислоты, который после промывки, сушки и разрыхления является 'побочным продуктом — белой сажей 300.
Разложение кремнефторида калия раствором поташа протекает с наибольшей скоростью при температуре кипения смеси (103— 113°). Кремнефторид при этом разлагался практически нацело при небольшом (5%) избытке углекислого калия сверх теоретического количества301. При начальной концентрации в растворе 10—13,5% КгСОз кремнефторид разлагается в течение 1 ч. С увеличением Концентрации раствора поташа продолжительность взаимодействия увеличивается, например, при 21% К2СО3 реакция длится 3 ч, а при 30% К2СО3 — 4 ч.
Осаждаемый в описанных условиях гель кремневой кислоты фильтрует с высокой скоростью и легко промывается. На полуав -
|
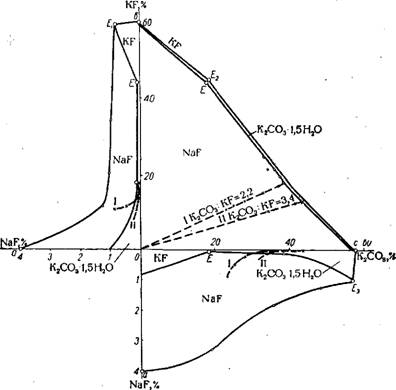
Рис. 335. Диаграмма взаимной водной системы 2KF + Na2C03 ^ ^ 2NaF + К2СО3 при 75° в прямоугольных координатах (разрез по Оси NaF—К2СО3 и области в координатах 2NaF—К2СО3—2KF): /-•разрез через поверхность насыщения NaF прн отношении К2СО3 : KF = 2,2; II - то же прн КгСОз : KF - 3,4. |
Тематической горизонтальной центрифуге достигнута производительность в 470 кг/ч по влажному (44%) осадку. С целью полного осаждения кремневой кислоты из раствора KF Необходимо охлаждение реакционной смеси до 25°. Отфильтрованный после этого раствор содержит лишь 0,05—0,06% БЮг.
На рис. 335 показана часть диаграммы взаимной системы 2KF+Na2C03=Pi:2NaF,+КгС03 при 75°301 ■302. Для рассматриваемого Процесса осаждения NaF имеют значение разрезы диаграммы этой системы через поверхность насыщения NaF при различном соотношении в растворе К2СО3 и KF. Экспериментально определены два таких разреза для 75° при отношениях К2СО3: KF, равных 2,2 и 3,4 (кривые I и II). Они показывают, что по мере увеличения концентрации K2CO3 + KF происходит полное высаливание NaF до начала кристаллизации К.2С03- 1,5Н20. Это позволяет построить технологический процесс так, чтобы путем выпарки раствора поташа в присутствии фтористого калия практически полностью выделялся фтористый натрий.
|
K, S!F,
Рис. 336. Схема производства фторида натрия и поташа нз кремнефторида Калия и соды. |
Один из вариантов схемы производства фторида натрия поташным способом приведен на рис. 336. Конверсия кремнефторида калия осуществляется в обогреваемых паром реакторах с мешалкой взаимодействием с оборотным раствором, содержащим около 39% К2СО3 и 11,5% KF. Этот раствор образуется в процессе первой выпарки смеси, состоящей из фильтрата фторида калия и раствора от промывки поташа. В процессе первой конверсии получается раствор с содержанием до 23% KF и до 0,05% Si02 при практически полном (98,8—99%) разложении кремнефторида. Выделение кристаллов NaF производится в два приема: в процессе второй конверсии и при первой выпарке смеси растворов. Фильтрат, не содержащий NaF, выпаривается вторично для выделения кристаллического поташа К2СО3 • 1,5Н20. По этой схеме на 1 т фтористого натрия получается около 0,5 т поташа (прокаленного). На это количество продукции расходуется 1,04 т кремнефторида калия (свлаж-
ностью 10%) и 1,35 т кальцинированной соды при расходе пара на выпаривание 5,5 т. Получаемый фтористый натрий содержит (на сухое вещество): 98% NaF, 1% KF, 1% К2СО3 и 0,05% Si02.
Запатентован 303 более простой метод. KF получают, из раствора H2SiFe по реакции:
H2SiF6 + ЗК2СО3 =■ 6KF + Si02 + Н20 + ЗС02
Для получения осадка Si02) легкоотделяемого фильтрацией, реакцию ведут при 50—100° с избытком (до 150% от стехиометрического количества) К2СО3. Отфильтрованный и упаренный раствор
|
ПорT>I Воды |
|
SiF4(M3) |
|
Выпорка |
|
Абсорбция |
Со2+ нр
|
Кальцинированная сода
|
|
KaSiF. |
|
{восполнение поТерь^ Кгсо3) |
|
/ Конверсия |
|
Гл |
Фильтрование и / прамыбна ш/мма
|
Раствор К2СОэ |
|
Вода |
Фильтрование пристапяод NaF
|
Промыдная Soda |
|
Вода |
|
Прамыбко кристатв NaF Фторид натрия (товарный) |
|
// праивбка шлома Шлам SiO, |
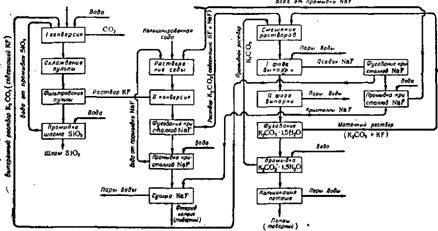
Рис. 337. Схема производства фторида натрия из газообразного четырех - фтористого кремния и соды.
Обрабатывают содой для получения NaF [по реакции (4)]; после Отделения кристаллов NaF раствор К2С03 возвращают в процесс. По другому варианту 304 фтористые газы (SiF4 или смесь SiF4+ + HF) поглощаются в абсорбере оборотным раствором поташа (рис. 337). Суспензия из абсорбера поступает в систему из нескольких обогреваемых паром реакторов, где протекает процесс первой конверсии. После отделения на центрифуге двуокиси кремния раствор фтористого калия (18—20% KF) выпаривают до концентрации около 40% KF. Выпаренный раствор поступает на взаимодействие с содовой суспензией (40% Na2C03) при 85—90й; выделяющийся при этом осадок NaF отфуговывают, а раствор поташа, содержащий 30—35% К2СО3, возвращают иа поглощение фтористых газов. По этой схеме на 1 т фтористого натрия расходуется 1,38 т
Кальцинированной соды, 0,47 т фтора (в виде газов), 0,06 т карбоната калия (потери) и 2,56 г пара. Потери карбоната калия могут восполняться введением в процесс кремнефторида калия.
Поташный способ экономичнее, чем способ производства фтористого натрия из плавикового шпата и серной кислоты. Его достоинством является получение очень чистого продукта.
Фторид кальция [5]
Синтетический фторид кальция 80-304'305 отличается от природного необогащенного плавикового шпата тонкодисперсной структурой. При взаимодействии H2SiF6 с СаСОз или СаО вначале образуется кремнефторид кальция, затем фторид кальция.
H2SiF6 + СаС03 = CaSiF6 + Н20 + С02 CaSiF6 + 2СаС03 = 3CaF2 + Si02 + 2С02 H2SiF6 + ЗСаСОз = 3CaF2 + Si02 + 3C02 + Н20
При использовании карбоната кальция образуется густая пена. Хотя реакция протекает с выделением тепла, но для завершения разложения CaSiF6 требуется подогрев смеси до 70—80° и длительное перемешивание (2—3 ч). При исходной концентрации H2SiF6 8—14% оптимальное весовое отношение СаС03: H2SiF6 рав - hq 2,5. При использовании 12%-ной кремнефтористоводородной кислоты в результате реакции образуется суспензия с весовым отношением Т : Ж, равным 1 : 4. Осадок CaF2 получается тонкодисперсный и трудно отстаивающийся. Фильтруемость осадка зависит от соотношения HF и H2SiF6 в кислоте и вида используемого карбоната кальция, который во всех случаях должен быть тонкоизмельчен - ным. Если в жидкости много HF, для нейтрализации следует применять молотый известняк, так как применение мела в этом случае приводит к образованию очень тонкого, плохо фильтрующегося осадка. Чем больше в смеси H2SiF6, тем легче фильтруется осадок, полученный с применением мела. При отношении HF : SiF4, меньшем 1 : 12, уже возможно использование мела 306, позволяющего достичь полной нейтрализации кислоты.
Для улучшения отстаивания и фильтрации тонкодисперсного CaF2 предложено добавлять в реакционную массу при его осаждении олеиновую кислоту (1—2,5%). Олеиновая кислота может быть использована многократно, так как она не вступает в реакцию и при. перемешивании реакционной массы всплывает наверх 307.
При непосредственном поглощении отбросных фтористых газов меловой суспензией можно нейтрализовать практически весь карбонат, оставляя в суспензии ~0,5 г/л СаСОз с целью предотвращения проскока фтористых газов. Коэффициент абсорбции SiF4 меловой суспензией больше, чем водой, и составляет в башне с хордовой насадкой235 - 10 ООО'г1.
Сгущение осажденного фторида кальция можно осуществить на центрифуге отстойного типа. В отфугованной массе остается до 60% влаги. После высушивания получается тонкодисперсный продукт с величиной частиц около 5 мк и меньше, являющийся смесью кристаллического CaF2 и аморфной Si02. В нем содержится ~63% CaF2, 24—30% S. i02, 10% СаС03 и 3% прочих примесей, количество и состав которых зависят от качества известняка или мела. При использовании для осаждения свежеобожженной извести выход CaF2 составляет по фтору 85—92%, по окиси кальция 74—87%.
Фтористый кальций, содержащий больше 94% CaF2, получается при термической диссоциации CaSiF6 при 380—400°:
CaSiF6 = CaF2 + SiF4
Реакция нейтрализации H2SiF6
H2_SlFe + СаО = CaSiF6 + Н20
Протекает нацело даже на холоду, причем основная масса CaSiF6 выделяется в осадок, а из фильтрата, содержащего 12—15% CaSiF6, можно выделить добавочное количество этой соли выпариванием. Маточный раствор может быть использован для поглощения SiF4.
Можно получать CaF2 из H2SiF6 при помощи СаС12 по схеме: H2SiF6 + СаС12 = CaSiF6 + 2НС1 CaSiF6 + 2СаО = 3CaF2 + Si02 2НС1 + СаО = СаС12 + Н20
В результате нейтрализации соляной кислоты вновь образуется СаС12, который возвращают в процесс.
Предложено получать фтористый кальций поглощением фтористых газов растворами фторидов щелочных металлов и последующей конверсией образовавшихся кремнефторидов едкой щелочью и каустификацией раствора фторида гидроокисью кальция 308:
SiF4+2MF = M2SiF6 M2SiF6 + 4МОН = 6MF + Si(OH)4 4MF + 2Са(0Н)2 = 2CaF2 + 4МОН
В этом процессе щелочь не расходуется (за исключением потерь) ; часть получаемого во второй стадии раствора фторида возвращают на абсорбцию, а часть направляют на каустификацию. Каустификация идет с большой скоростью и практически заканчивается в течение 1 ч. Конверсия кремнефторида также идет с достаточной для практических целей скоростью и полнотой. Получаемые шламы хорошо отстаиваются. Лабораторные испытания показали, что этим способом может быть получен фтористый кальций хорошего качества.
Однако при наличии в газах, кроме SiF4, также HF и H2SiF6 осадок CaFa, образующийся при применении Са(ОН) 2, получается слишком тонкий, трудно отделяемый от жидкости (как при осаждении CaF2 из смеси кислот мелом). В связи с этим этот способ не применим для прямого улавливания фтористых газов суперфосфатных заводов. Считают, что он может быть использован для переработки на CaF2 газов с малым содержанием HF. Впрочем этот способ не имеет преимуществ перед переработкой на CaF2 кремнефтористоводородной кислоты без получения из нее Na2SiF6.
Описана крупная заводская установка в США для улавливания известняком HF из газов, выделяющихся в производстве обесфторенного плавленого фосфата. После очистки от пыли газы с температурой 100—450° пропускают через башню со слоем известняка 2,5—3 ж (размер кусков 6—40 мм). При концентрации HF, соответствующей 0,15—6 г/ж3 фтора, степень поглощения 95—96%. Периодически часть известняка (~40%) заменяют свежим. Фторид кальция накапливается в мелочи, содержащей 80—95% CaF2. Крупные куски, не прошедшие через сито с отверстиями 3,33 жж, содержат лишь 20—40% CaF2 и после отделения от мелочи их возвращают В башню 309-312. Изучена зависимость степени поглощения HF и скорости процесса от свойств известняка, температуры и пр.313.