Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
Разложение фосфатов с образованием загустевающей пульпы
При уменьшении нормы кислоты до стехиометрической величины и увеличении ее концентрации до 50% Р2О5 и-больше весовое отношение между фосфатом и кислотой Т : Ж составляет ~ 1 :2. В этих условиях разложение фосфата в первой стадии (до образования насыщенного раствора) протекает в небольшой степени и в течение очень короткого времени (5—10 мин) 41. В дальнейшем начинается кристаллизация новой твердой фазы и по мере израсходования кислоты количество жидкой фазы уменьшается, а количество твердой фазы увеличивается. В результате этого пульпа постепенно густеет и, наконец, полностью загустевает (схватывается), как и при получении простого суперфосфата. Кристаллизация новой твердой фазы и схватывание пульпы происходит тем быстрее, чем выше концентрация исходной фосфорной кислоты. Выделяющиеся кристаллы продукта реакции тесно соприкасаются с непрореагировавшими зернами фосфата и откладываются на их поверхности. Образующаяся корка по мере ее формирования оказывает все большее сопротивление диффузии ионов водорода. Вследствие этого скорость разложения фосфата определяется все нарастающим сопротивлением твердой фазы4l. Суммарное влияние условий протекания процесса в первой стадии и в период образования корки на зернах фосфата предопределяет скорость разложения в загустевающей пульпе.
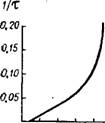
Известно 33,38, что в случае торможения процесса сопротивлением образующейся корки скорость его изменяется по уравнению прямой в координатах '/У—1/х, где у — количество вещества, прореагировавшего к моменту времени т. Как видно на рис. 283, разложение апатита фосфорной кислотой в загустевающей пульпе характеризуется в целом значительно более сложной зависимостью. Однако, если исключить первый период (10—20 мин), когда разложение протекает в ненасыщенных растворах и в незагу - стевающей пульпе, то в дальнейшем процесс описывается указанной зависимостью.
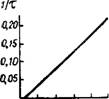
В отличие от апатитового концентрата разложение фосфорита Каратау в течение длительного времени (от 5 до 150 мин) хорошо описывается прямолинейной зависимостью в указанных координатах (рис. 284). Это, очевидно, объясняется тем, что при наличии в растворе соединений магния насыщение раствора и кристаллиза
ция высаливаемой соли — монокальцийфосфата наступает значительно раньше момента отбора пробы для первого определения.
Изменение степени разложения фосфата во времени в загустевающей пульпе определяется совместным влиянием активности ионов водорода раствора и свойств кристаллизующейся твердой фазы. Поэтому в течение некоторого времени, пока корка на зерНах фосфата еще является рыхлой и достаточно проницаемой, про -
|
0,1 0,2 0,3 0,4 а5 I/r'O2 Рис. 283. Зависимость между /у И 1/т при разложении апатита фосфорной кислотой: У — степень разложения (в %) апатита кислотой концентрации 59% P2O5; т-время в мин. |
|
1,2 1,4 1.6 1,8 2,0 2,2 Рис. 284. Зависимость между 1 /(/ и 1/т при разложении фосфорита Каратау фосфорной кислотой концентрации 52,5% Р205: У — степень разложения, %: х — время в мин. |
|
1/у-ю' |
Цесс протекает с заметной скоростью, а в дальнейшем, когда корка увеличивается по своей толщине и становится плотной, сильно замедляется.
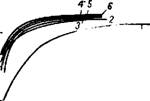
Разложение апатитового концентрата стехиометрической нормой фосфорной кислоты при 20° (рис. 285) ускоряется по мере увеличения концентрации кислоты от 13,6 до 53,6% Р2О5, но замедляется при использовании более концентрированной кислоты40. По - видимому, повышенное значение оптимальной концентрации фосфорной кислоты при разложении фосфата небольшим ее количеством объясняется42 уменьшением концентрации кислоты в начале взаимодействия реагентов до величины, при которой фосфат разлагается насыщенными растворами с наибольшей скоростью (см. выше). При использовании в этом случае менее концентрированной кислоты (например, 40—45% Р2О5) снижение концентрации жидкой фазы в начале процесса произошло бы до величины, прн которой апатит разлагается с меньшей скоростью.
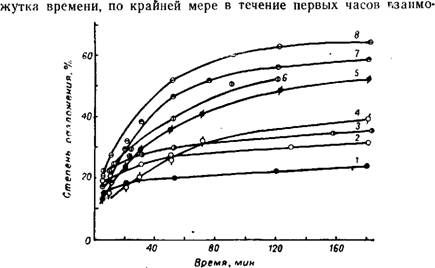
В течение первых 10—20 мин с начала реакции степень разложения мало зависит от нормы кислоты в пределах 50—130% от
стехиометрической, необходимой для образования монокальцийфосфата (рис. 286). Это объясняется тем, что в первый момент реагирует только поверхностный слой зерен, поэтому при всех указанных нормах кислоты имеется большой ее избыток. Некоторое увеличение нормы кислоты позволяет осуществить процесс с несколько большей скоростью в течение более длительного проме -
|
Рис. 285. Изменение коэффициента разложения апатитового концентрата во времени при стехиометрической Норме фосфорной кислоты и температуре 20°. Концентрация кислоты (в % Р2О5): / — 13,6; 2 — 21,0; 3 — 36,4; 4 - 64,8; 5 - 45,6, б - 55.8; 7 - 51,5; S - 53,6. |
Действия (рис. 286). Но увеличение нормы кислоты больше 110% от стехиометрического количества не влияет на степень разложения в продукте после двухнедельного его вылеживания49.
Существенное повышение степени разложения фосфата наблюдается при изменении температуры от 20 до 40° (рис. 287). Дальнейшее повышение температуры до 70—80° приводит к незначительному увеличению[4]'34'50 степени разложения апатита. Это объясняется тем, что при температурах выше 40° уже через очень короткий промежуток времени от начала реакции выделяется значительное количество кристаллов монокальцийфосфата, создающих большое сопротивление диффузии кислоты. В результате этого скорость процесса при температурах выше 40° определяется диффузионным сопротивлением твердой корки продукта реакции, которое мало или вовсе не зависит от температуры. Практически и при растворении апатита в большом количестве насыщенного раствора
(в отсутствие перемешивания твердой фазы) также наблюдается независимость скорости процесса от температуры34. По-видимому, при отсутствии интенсивного отвода образующихся солей в общую массу системы они отлагаются в непосредственной близости от места их возникновения, т. е. у поверхности зерен фосфата. Следует также учесть и резкое уменьшение концентрации ионов водорода с повышением температуры кислоты одной и той же концентрации, вследствие понижения диссоциации кислоты. При этом
|
80 |
|
|
|
£0 |
|
40 |
|
■ ' ' ' 1 |
|
40 80 120 160 Время, мин |
|
|
|
£0 |
|
40 |
|
20 |
|
7 6 5 |
|
40 80 120 ISO Время, мин |
|
Рис. 286. Степень разложения апатита фосфорной кислотой прн 20° в зависимости от нормы кислоты (в % от стехиометрического количества): /-50; 2-75; 3-90; 4-100; 5-110; и - 120, 7-130. |
§
I
*
О
|
8 ч - о «J С 111 А |
|
20 |
|
■ I I I I I I I |
О.
Скорость реакции между ионами водорода и фосфатом с увеличением температуры возрастает в меньшей мере (или в такой же степени), чем уменьшение концентрации ионов34. Таким образом, не только диффузионные, но и кинетические условия осуществления процесса предопределяют незначительное влияние повышения температуры на его скорость.
На скорость разложения фосфата фосфорной кислотой, как и при разложении серной кислотой (см. гл. XXIV), влияют интенсивность перемешивания, гранулометрический состав и общая (внутренняя) поверхность элементарных зерен фосфата.