Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
ПОЛУЧЕНИЕ ФТОРА
Промышленные методы получения фтора основаны на электролизе расплава, состоящего из KF и HF 117-119. При составе электролита KF + 12HF электролиз ведется при температуре от —30 до —50°; при составе электролита KF • HF температура электролиза выше 250°. Она определяется физическими свойствами электролита. По-видимому, наиболее удобным является состав электролита KF • 2HF, который расплавляется ниже 100°, а электролиз ведется при 90—120° при непрерывной подаче фтористоводородного газа в электролизер 75,120.
На аноде выделяется фтор, на катоде — водород. Для корпуса ванны, диафрагмы, катода и других элементов конструкции применяют сталь и красную медь; аноды — угольные или графитовые. Для отвода выделяющегося тепла ванну охлаждают снаружи водяной рубашкой. В анодном газе содержится до 4—8% HF. После отделения HF получается газ примерного состава: 99% F2, 0,12— 0,14% С02, 0,3—0,5% 02 и 0,1—0,4% N2121'122.
Было предложено много конструкций ванн для получения фтора 12s-i27. Одна из них показана на рис. 324. Ванна имеет длину 1,81 м, ширину 0,46 м и высоту 0,61 м работает при нагрузке 750—1500 а, что соответствует плотности тока 1075—2150 а/м2.
Рабочая поверхность анодов около 0,7 м2. Содержание HF в электролите 37—40%; температура электролита 95—115°. Выход по току достигает 95%; он зависит от качества фтористоводородного газа и чистоты бифторида калия, который не должен содержать заметных количеств H20, SO?-, SiFe" и др. При снижении концентрации HF в электролите ниже 37% начинает кристаллизоваться KF, и возрастает сопротивление электролита. Улучшение смачиваемости анода электролитом достигается при добавке к нему 1—1,5% LiF128.
Вследствие большой реакционной способности фтор обычно перерабатывают сразу по выходе его из электролизера. В случае необходимости транспортировать фтор предпочитают сжижать путем глубокого охлаждения жидким азотом или кислородом. Сжижение фтора при более высоких температурах под давлением затруднено сильной коррозией движущихся частей компрессоров. В связи с этим представляет интерес применение для сжатия фтора диафрагменного четырехступенчатого компрессора 129.
|
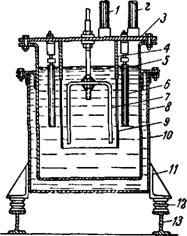
Рис. 324. Схематический разрез электролизера для получения фтора: |
|
/ — выход водорода; 2—.выход фтора; 3 — крышка; 4 — перегородка, к которой прикрепляется диафрагма; 5— уровень электролита; 6 — анод; 7 — катод; 8 — корпус электролизера; 9 — диафрагма из сетки; 10 — водяная рубашка; Л — угловое железо; 12— фарфоровый изолятор; 13 — опоры из швеллерного железа. |
Для транспорта фтора применяют стальные и никелевые баллоны130-132. Образующаяся на внутренней поверхности баллона пленка из фтористой соли препятствует дальнейшей коррозии, признаки которой не обнаруживаются даже после годового хранения фтора 133. Для транспорта под атмосферным давлением применяют стальные трубы, но при этом следует опасаться увлажнения фтора или загрязнения его органическими примесями. При повышенном давлении более пригодны трубы из никеля или монель-металла 134.
Разработана конструкция автоцистерны для перевозки фтора и резервуара для его хранения. Это три горизонтальных стальных цилиндра, находящиеся один в другом. Во внутреннем цилиндре содержится жидкий фтор (—188°) под атмосферным давлением, между стенками внутреннего и среднего цилиндров находится жидкий азот (—196°) также под атмосферным давлением, а кольцевое пространство между средним и наружным цилиндрами заполнено тепловой изоляцией. Жидкий азот предотвращает
11 М. Е. Позин
испарение фтора, наружная изоляция уменьшает потери азота. Перекачку жидкого фтора производят, передавливая его сжатым гелием 135.
Отходящие газы после сжижения или использования фтора перед выбросом в атмосферу необходимо очищать от остатков фтора промывкой раствором щелочи, например по следующей схеме136. Газ отмывают от фтора в поглотительной колонне с насадкой, орошаемой 5—15% раствором NaOH с температурой 40—65°; при такой концентрации NaOH идут только следующие реакции F2 + 2NaOH = 2NaF + '/202 + Н20; F2 + Н20 = 2HF + '/202;
HF + NaOH = NaF + Н20
И чрезвычайно ядовитая окись фтора не образуется. Вытекающий из колонны раствор, содержащий NaF, перекачивают насосом в регенерационный бак, где его обрабатывают известковым молоком. При этом регенерируется едкий натр (по реакции 2NaF + + Ca(OH)2 = CaF2 + 2NaOH) и после отстаивания суспензии CaF2 осветленный раствор через теплообменники возвращается на абсорбцию фтора. При такой схеме расходуется вместо едкого натра более дешевый продукт — известь — и предотвращается накопление в системе NaF, который вследствие малой растворимости мог бы выделяться в осадок и забивать насадку абсорбера и трубы. Расход извести ~4,5 кг на 1 кг улавливаемого фтора.
Необходимый для производства фтора бифторид калия готовят смешением рассчитанных количеств плавиковой кислоты и поташа или едкого кали. К полученному раствору добавляют этиловый спирт для высаливания бифторида, который затем высушивают. Так как с исходными растворами вводится вода, которая также выделяется и при реакции
4HF + 2КОН = 2(KF • HF) + 2Н20
То для более полного использования реагентов необходимо производить выпаривание раствора до начала кристаллизации при 90— 100°, а затем разгонку водно-спиртовой смеси для регенерации спирта и вывода из системы воды. Можно, однако, осуществлять процесс без выпарки раствора и без разгонки водно-спиртовой смеси по следующей схеме 114. В абсорбционной колонне, орошаемой спиртом, поглощают фтористый водород, получая 30—40% раствор HF в спирте. Едкое кали растворяют в оборотном спирте, и после отделения от этого раствора водно-солевого слоя смешивают спиртовые растворы КОН и HF. Выпавший бифторид калия отделяют центрифугированием и высушивают при 100°. Маточный раствор спирта, а также конденсат из паров спирта, уловленных при сушке бифторида, возвращают в цикл для приготовления исходных растворов.