МЕТАЛЛИЧЕСКИЕ РЕШЁТКИ
Все металлы — вещества кристаллические. Что же такое кристаллы?
Слово «кристаллос» у древних греков обозначало лёд. Впоследствии этим словом стали называть все твёрдые тела, имеющие естественную строго определённую геометрическую форму. Кристаллы весьма распространены в природе. Подавляющее большинство твёрдых тел имеет кристаллическое строение.
Железо при затвердевании образует кристаллы в виде кубиков. Но на рисунке 4 мы видим кристаллы железа неправильной формы, кристаллиты, имеющие вид зёрен. Почему это происходит? Как растут кристаллы?
Ответ на эти вопросы впервые дал Д. К. Чернов. Впоследствии справедливость его взглядов была подтверждена работами многих советских учёных.
В расплавленный металл неизбежно попадают пылинки, пузырьки воздуха и другие посторонние включения. Как правило, именно вокруг этих мельчайших частичек начинают группироваться беспорядочно расположенные в остывающем металле атомы. Кроме того, центрами кристаллизации служат и комплексы атомов, самопроизвольно возникающие в охлаждаемом металле. Так образуются зародыши будущих кристаллов (рис. 5, а). По мере охлаждения металла количество зародышей увеличивается. Каждый зародыш вырастает в отдельный кри - сталик (рис. 5, б). Растущие кристаллы в определённый момент начинают теснить друг друга (рис. 5, в), и их правильная форма искажается. Нарушению формы кристаллов способствует и неодинаковая температура в различных местах остывающего металла. Поэтому в расплаве и возникают зёрна (рис. 5, г) и древовидные образования из сросшихся друг с другом отдельных мелких кркстали - ков — дендриты. Кристаллические зёрна и дендриты в застывшем металле могут быть различной формы и ве
Личины. Они отделены друг от друга отдельными прослойками, которые отчётливо видны под микроскопом (см. рис. 4). Эти прослойки состоят из различных неметаллических включений, которые всегда присутствуют в металле.
Получить металл, который состоял бы только из одного кристалла — монокристалла, в обычных условиях
|
Рис. 5. Схема роста кристаллов в застывающем расплаве: а — образуются зародыши, б растут кристаллы, в— кристаллы начинают теснить друг друга, г — отдельные зёрна сращиваются. |
Не удаётся. Объясняется это тем, что в расплаве одновременно зарождается множество кристаллов. Однако для изучения некоторых свойств металлов, как мы увидим дальше, необходимо бывает иметь монокристалл, и в настоящее время разработаны способы искусственного выращивания монокристаллов (осторожное охлаждение расплава и другие способы).
И в зёрнах, и в дендритах, и в монокристалле одного и того же металла атомы располагаются в строго определённом порядке; они образуют ту или другую пространственную решётку.
Атомы нельзя увидеть ни в какой микроскоп. Однако, освещая кристалл рентгеновскими лучами и изучая рентгенограмму, то-есть картину, которая создаётся этими лучами после прохождения их через кристалл на фотопластинке, удаётся глубоко заглянуть в мир кристаллов. Удаётся узнать, как расположены в кристаллической решётке различные атомы и каковы расстояния между этими мельчайшими частицами вещества, частицами, которых мы не можем видеть.
Рентгеновские исследования показали, что среди металлов чаще всего встречаются три типа пространственных решёток.
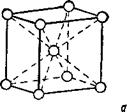
Первый тип — кубическая объёмноцентри - рованная решётка. Атомы в такой решётке находятся в вершинах и в центре куба (поэтому - то решётка и называется объёмноцентрированной). Каждый атом окружён восемью ближайшими соседними атомами (рис. 6, а). Такую решётку имеют литий, хром, ванадий, молибден, вольфрам.
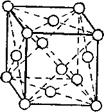
Второй тип решётки — кубическая гранецен- трированная (рис. 6, б). Атомы расположены п о вершинам и центрам граней куба. Такой решёткой обладают, например, алюминий, медь, свинец, никель, золото, серебро, платина.
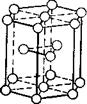
Третий тип — гексагональная (шестиугольная) плотно упакованная решётка (рис. 6, в). Она встречается у магния, цинка, кадмия, бериллия.
Марганец, висмут, белое олово и некоторые другие металлы имеют более сложные решётки.
Изучая рентгенограммы различных кристаллов, учёные пришли к убеждению, что атомы «упаковываются» в пространстве примерно таким же образом, каким можно упаковывать твёрдые шары. Поэтому на рисунке 6 атомы условно изображены в виде шариков (расстояния между ними в левой части рисунка заведомо увеличены, чтобы яснее представить строение кристаллической решётки).
И в кубической гранецентрированной, и в гексагональной решётке каждый атдм металла окружён двенадцатью ближайшими соседними атомами. Чем больше соседей у атома в кристаллической решётке, тем больше места в решётке занято самими атомами. Наиболее плотная «упаковка» атомов — в гранецентрированной и гексагональной решётках. Здесь атомам принадлежит 74% пространства, занимаемого кристаллами. В кубической объёмноцентрированной решётке атомы занимают только 68% пространства.
Нужно сказать, что в металлических кристаллах нет нейтральных атомов; пространственные решётки составлены из положительно заряженных атомов, из ионов.
|
|
|
Рис. 6. Типы кристаллических решёток металлов: а — кубическая объемноцентрированная решётка, б — кубическая гранецентрированная решётка, в — гексагональная решётка (плотная упаковка). |
 Каждый атом металла всегда теряет одну или несколько частиц отрицательного электричества — электронов, и становится ионом. Ионы закреплены в «узлах» пространственной решётки — вершинах и центре куба, в центрах граней и т. д., в зависимости от типа решётки. Электроны же беспорядочно блуждают между ионами.
Каждый атом металла всегда теряет одну или несколько частиц отрицательного электричества — электронов, и становится ионом. Ионы закреплены в «узлах» пространственной решётки — вершинах и центре куба, в центрах граней и т. д., в зависимости от типа решётки. Электроны же беспорядочно блуждают между ионами.
Природа кристаллической решётки и расположение в ней атомов оказывают большое влияние на многие свойства веществ. Об этом мы ещё будем говорить подробно, а сейчас познакомимся с одной интересной особенностью кристаллов, которая называется «анизотропией» и объясняется их строением. Слово «анизотропия» по-гречески означает «неравное свойство». Анизотропия — это неоднородность свойств кристалла в разных направлениях.
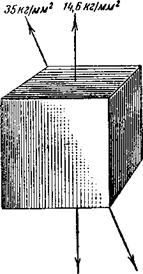 По одним направлениям кристаллы разрушаются легче, чем по другим. Если растягивать монокристалл меди перпендикулярно грани куба, то для того, чтобы его разорвать, требуется напряжение, равное 14,6 кг! мм2 (килограмма на квадратный миллиметр); если же растягивать изготовленный из того же монокри-
По одним направлениям кристаллы разрушаются легче, чем по другим. Если растягивать монокристалл меди перпендикулярно грани куба, то для того, чтобы его разорвать, требуется напряжение, равное 14,6 кг! мм2 (килограмма на квадратный миллиметр); если же растягивать изготовленный из того же монокри-
|
|
Рис. 7. Прочность кристалла Рис. 8. Стекло проводит тепло оди - меди в разных направлениях наково быстро во всех направлениях.
Различна. Олово проводит тепло в одних на
Правлениях хуже, чем в других.
Сталла образец по диагонали куба, то для разрыва требуется напряжение, равное уже 35 кг/мм2 (рис. 7). Это показывает, что кристаллы меди в одном направлении обладают более высокой прочностью, чем в другом.
Неодинакова по разным направлениям и теплопроводность кристаллов. В этом убеждает нас такой опыт (рис. 8). Возьмём кристалл белого олова и для сравнения — кубик, вырезанный из стекла (стекло представляет собой изотропный материал — его свойства одинаковы по всем направлениям). Покроем их грани парафином, а затем поднесём к ним горячую иглу. Расплавленный
слой парафина на стекле будет иметь форму круга, а на олове — овальную форму. Это значит, что олово по одним направлениям проводит тепло хуже, чем по другим, а стекло — по всем направлениям одинаково [48]).