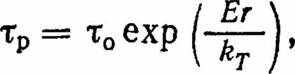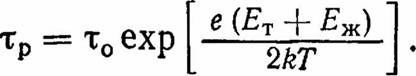МЕХАНИЗМ ВЗАИМОДЕЙСТВИЯ РАЗНОРОДНЫХ МЕТАЛЛОВ ПРИ СВАРКЕ
Экспериментальные и теоретические исследования, проведенные советскими учеными, показывают, что сварку, наплавку и пайку следует отнести к классу реакций, для которых характерным является двухстадийность процесса образования прочных связей между атомами соединяемых веществ. В течение первой стадии происходит образование физического контакта, т. е. осуществляется сближение соединяемых веществ на расстояния, требуемые для межатомного взаимодействия и подготовки поверхности к взаимодействию. На этой стадии из элементарных процессов важную роль играют процессы электростатического взаимодействия поверхностных атомов, В течение второй стадии —
стадии химического взаимодействия — заканчивается процесс образования прочного соединения.
Далее могут протекать процессы релаксационного характера, часто приводящие к снижению достигнутой прочности вследствие рекристаллизации или образования прослоек из хрупких химических соединений или фаз за счет гетерогенной реактивной диффузии. Однако эти процессы могут приводить и к повышению прочности соединения, если вследствие диффузии благоприятно меняется химический состав шва и прилегающих к нему зон.
В случае соединения чистых металлов или твердых растворов процессы взаимодействия сводятся к коллективизации (обобщению) «валентных» электронов положительными ионами, вследствие чего между системой атомов, образующих кристаллическую решетку, возникает прочная «металлическая» связь.
Поверхности твердых тел в атмосферных условиях, как правило, инертны, так как валентности их атомов насыщены связью с атомами окружающей среды и чаще всего кислородом. На окисленной поверхности твердого тела могут протекать процессы физической адсорбции. Для осуществления хемосорбции (химической адсорбции) на реальной поверхности требуется затрата энергии на активацию этой поверхности.
Теплота хемосорбции больше теплоты физической адсорбции и при хемосорбции молекула приближается к поверхности на более близкое расстояние, чем при физической адсорбции. По мере того, как молекула приближается к поверхности, она испытывает вначале влияние физических сил притяжения, которые действуют на больших расстояниях, чем силы химической связи. Для осуществления хемосорбции молекула должна обладать определенной энергией. В приобретении молекулы или атомом этой энергии и заключается акт активации.
Таким образом, протекание процессов взаимодействия различных типов в контакте соединяемых материалов требует определенной величины энергии для активации состояния поверхностей. Эта энергия может сообщаться в виде теплоты (термическая активация), энергии упруго-пластической деформации (механическая активация), электронного, ионного и других видов облучения (радиационная активация) [52].
При сварке в твердом состоянии сближение атомов достигается за счет совместной упруго-пластической деформации соединяемых материалов в контакте, часто в сочетании с дополнительным нагревом.
При сварке плавлением и пайке сближение атомов осуществляется за счет смачивания и активации поверхности твердого материала за счет тепловой энергии.
В каждом из этих случаев для образования соединения требуется определенное время, обусловленное процессами развития физического контакта и химического взаимодействия фаз. Чем ниже температура процесса, тем легче разделить две основные стадии образования соединения друг от друга. При взаимодействии твердого материала с жидким процесс протекает при высокой температуре (по отношению к температуре плавления основного металла) и поэтому скорость его высокая. Обе стадии протекают друг за другом в процессе смачивания, и разделить их практически не удается.
Итак, при сварке плавлением, наплавке и пайке обе стадии процесса и следующая за ними диффузия протекают, как правило, настолько быстро, что в случае соединения разнородных материалов с ограниченной взаимной растворимостью практически трудно получить соединения без хрупких интерметаллических прослоек в контакте. Для разработки технологических процессов сварки необходимо иметь представление о допустимой (при сварке плавлением) длительности этих процессов с тем, чтобы правильно выбирать способ и параметры сварки и обеспечивать получение качественного соединения. В работах [7, 20, 18 и др. ] была дана оценка длительности указанных процессов и сопоставлены
результаты расчета с имеющимися в настоящее время опытными данными. Эти процессы рассмотрены как для сварки плавлением, так и для сварки в твердом состоянии.
Внутри кристалла каждый атом удерживается в своем положении силами связи, симметрично расположенными относительно окружающих его со всех сторон соединений
|
|
|
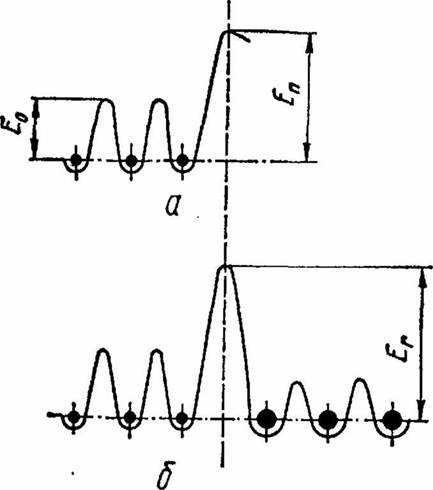
Рис, 7. Схема изменения потенциальной энергии системы атомов: а — у поверхности кристалла; 6 — на границе твердой и жидкой фаз в начальный период их |
атомов. На свободной поверхности кристалла или жидкости атом оказывается неуравновешенным вследствие отсутствия связи с одной стороны (вакуум) или вследствие ослабления связи, обусловленной иными свойствами окружающей среды. Это обстоятельство вызывает повышение энергии поверхностного слоя кристалла. Если для перемещения внутри тела атому необходима энергия Eot то для выхода атома в окружающую среду ему необходима энергия причем
Еп > Е0.
|
контакта» |
При быстром образовании физического контакта, что наблюдается при окунании твердого тела в расплав или при сварке за счет расплавления одного из соединяемых материалов, на границе фаз сначала будет наблюдаться пик межфазной энергии Еп аналогичный Еп (рис. 7), так как переход атомной системы в новое состояние осуществляется не мгновенно, а за некоторый конечный промежуток времени. Поэтому следует ожидать запаздывания химического взаимодействия фаз, а также задержки диффузионных переходов атомов из одного состояния в другое, пока атом не приобретает энергии, необходимой для преодоления меж - фазного барьера, или пока не произойдет релаксация пика
межфазной энергии. Без учета возможных поверхностных явлений период задержки или ретардации диффузии можно рассматривать как время жизни атома перед потенциальным барьером, т. е.
|
|
(1)
тр — период (время) ретардации; Т — температура, К; k ■— коэффициент распределения.
|
|
Определение межфазной энергии представляет большие трудности в нестационарном процессе, так как эта энергия в каждом конкретном случае зависит от особенностей самого процесса, физико-химической природы рассматриваемых фаз и поверхностных явлений. Для ориентировочных оценок периода ретардации можно принять допущение, что величина межфазной энергии в случае взаимодействия двух конденсированных фаз изменяется (уменьшается) по экспоненциальному закону. При таком допущении период релаксации равен времени уменьшения возмущения (исходной величины поверхностного натяжения) до от первоначальной величины. Поэтому в первом приближении и для оценочных расчетов величину межфазной энергии можно определить как
(2)
где ЕгиЕж— энергии активации диффузии соответственно
в твердой и жидкой фазах.
|
|
С учетом уравнения (2) выражение для оценки периода ретардации диффузионных процессов примет вид
(3)
Расчеты по формуле (3) для различных сочетаний показали, что полученные данные достаточно хорошо согласуются с опытными. Это позволяет, несмотря на принятые
допущения, использовать приведенную схему для ориентировочных оценок допустимой длительности контакта твердой и жидкой фаз, а также температуры процесса наплавки, сварки, а в ряде случаев и пайки.
Как уже рассматривалось ранее, важнейшим процессом, протекающим после релаксации пика межфазной поверхностной энергии, является гетерогенная диффузия (прохождение атомами границы раздела фаз: растворение и гетеродиффузия). На основании анализа кинетики процессов, протекающих в зоне контакта, в общем случае длительность тк процесса контактирования твердой и жидкой металлических фаз можно представить 6 Следующем виде:
тк = Тр - f - Тд - J - То. з “I- Тр. х.с» (4)
где тр — время ретардации (релаксации межфазной поверхностной энергии); Тд-—время развития процессов гетеродиффузии до образования пересыщенных твердых растворов; т0<8 — время, необходимое для образования устойчивых зародышей новых химических соединений; тр. х.с — время дальнейшего роста химических соединений*
Период ретардации оценивается уравнением (3). Одним из условий получения качественного соединения является ограничение длительности контактирования таким образом, чтобы не допустить образования интерметаллических соединений, т. е,
*к "Iі" V
Время, вычисляемое по уравнению ретардации (3), всегда меньше времени, необходимого для образования интерметаллидов в зоне контакта. Однако, в связи с невозможностью в настоящее время дать точную оценку релаксации межфазной поверхностной энергии, время, вычисляемое из этого уравнения, по-видимому, существенно превышает истинное время ретардации, т. е. фактически из уравнения (3) определяется время Т = Тр - f Тд, а возможно и т = - f
+ тд + то. з. В связи с этим возникла необходимость попытаться экспериментально определить Тр и тр + Тд - j - т0 3 и оценить энергию активации процессов гетеродиффузии в зоне контакта.
Для изучения вопросов регулирования тепловых и диффузионных процессов на границе раздела твердой и жидкой фаз В. С. Новосадовым, М. X. Шоршоровым и Ю. JI. Красулиным была разработана специальная методика «жидкая клиновая проба» [7], позволяющая за счет регулирования температуры и длительности контактирования фаз гибко регулировать процессы, протекающие в зоне контакта. Жидкий расплав в пробе заливается в клиновое пространство, ограниченное с одной стороны образцом (твердая фаза), а с другой кристаллизатором из меди или другого материала с высокой теплопроводностью (сбоку клиновое пространство с каждой стороны ограничено теплоизоляционными стенками). Регулирование длительности контактирования по длине образца осуществляется за счет разницы в скоростях и времени кристаллизации в верхней и нижней («капилляр») частях клинового пространства. В нижней части клина длительность контактирования минимальная. Определяется она температурой подогрева образца в заливаемой жидкости. Экспериментально определенная величина энергии активации гетеродиффузии для соединений с исчезающе малой величиной гетеродиффузии составляет
Еа = 121 дж/кг • атом. Для соединений стали с алюминием,
стали и никеля с медью Еа ж 93,6 дж/кг ♦ атом. Для получения соединений с минимальным развитием гетеродиффузии длительность контактирования для пары стали с алюминием составляет при 700° С около 4 с, а для пар стали и никеля с медью при 1100° С примерно 0,5 с.