СВАРКА И СВАРИВАЕМЫЕ МАТЕРИАЛЫ
Металлургические реакции при сварке
Большинство процессов взаимодействия на границе металл — защитная среда протекают с наибольшей интенсивностью на высокотемпературных участках зоны плавления, поэтому особо
|
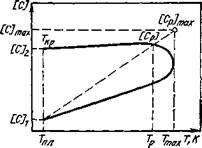
Рис. 3 2 Схема изменения концентрации элемента в наплавляемом металле в результате взаимодействия его со шлаком в сварочной ванне |
благоприятные условия для протекания реакции создаются на стадии каплн.
По мере спада температуры процессы в большинстве случаев начинают протекать в обратном направлении. Однако скорость протекания процессов в обратном направлении в низкотемпературной части сварочной ванны ниже скорости прямых процессов в наиболее горячей части ее. Этим в основном объясняется тот факт, что количество прореагировавшего вещества в процессе нагрева оказывается больше, чем при снижении температуры. Поэтому в затвердевшем металле часто наблюдается прирост или недостаток того или иного элемента по сравнению с исходной его концентрацией в сварочной ванне. Схематически процесс представлен на рнс. 3.2.
Допустим, что между шлаком и жидким металлом при сварке под флюсом идет реакция
(МеЛ)шл + У [Ме']ж (Ме'0)шл + х [Me'], (3.1)
в результате которой в наплавленном металле с увеличением
температуры возрастает концентрация [Me"]. Исходное равно
весное содержание этого элемента в металле было [Сі] (см. рис. 3.2).
Реакция стремится к новому равновесию, причем скорость ее возрастает с повышением температуры. После достижения Гшах температура начинает снижаться, а соответственно в обратном направлении должна изменяться и концентрация [Me"] в наплавленном металле, стремясь к содержанию [Сі]. Однако к моменту достижения Тmax концентрация [Me"] соответствует равновесному содержанию [Ср] для более низкой температуры,
поэтому при начальном снижении температуры [Сі] продолжает расти, стремясь к равновесному состоянию [Ср]тах. Таким образом, температура начинает снижаться, а концентрация [Me"] в наплавленном металле продолжает расти.
Вследствие дальнейшего снижения температуры увеличение содержания [Me"] сначала приостанавливается, а затем, пройдя через максимальную концентрацию [СР], соответствующую равновесной температуре Гр, также начнет снижаться, но опять отставая от изменения температуры. Указанное отставание со снижением температуры должно увеличиваться, так как скорости реакций при более низких температурах уменьшаются. К моменту возвращения объема металла к температуре Гкр концентрация [Me"] не будет иметь значения [Сі] (см. рис. 3.5), а останется на каком-то уровне [Сг], что и создаст прирост элемента в наплавленном металле Л[С].
Подобный ход рассуждений справедлив и применительно к реакциям между газами и металлом в зоне плавления.