«Современные химические источники тока»
Никель-металлгидридный аккумулятор MH ½ KOH½ NiOOH
Никель-металлгидридный (Ni-МН) аккумулятор появился как дальнейшее развитие НК системы в результате замены кадмиевого электрода на водородный электрод. Причины – 1) недостаточно высокая плотность энергии традиционных СА, НК и НЖ систем; 2) экологическая опасность свинца и кадмия. Широко используемые в производстве источников тока Cd, Pb, Hg и их соединения являются высокотоксичными.
Первый герметичный никель-водородный (Ni-Н2) аккумулятор был предложен в СССР в 1964 году:
(–) H2½ KOH½ NiOOH (+)
При заряде такого аккумулятора отрицательный электрод генерирует газообразный водород Н2, накапливающийся под давлением во всем свободном объеме внутри герметичного корпуса. Токообразующая полуреакцая следующая:
(–) 1/2Н2 + OH - « H2O + e
Положительным электродом является оксидно-никелевый электрод, как и в НК и НЖ системах, соответственно электродная полуреакция та же самая:
(+) NiOOH + H2O + e ↔ Ni(OH)2 + OH -
Суммарно
разряд
1/2Н2 + NiOOH ↔ Ni(OH)2
заряд
Давление Н2 в таком ХИТ растет пропорционально заряду и достигает 100 атм при полном заряде. Такие аккумуляторы надежно эксплуатируются в космической технике. Однако использовать их в бытовой электроаппаратуре, конечно, затруднительно.
Начиная с 1970-х годов в научной литературе стали появляться сообщения о металлических сплавах, способных обратимо поглощать большие количества водорода, образуя гидриды металлов. Таких сплавов к настоящему времени предложено несколько десятков. Наиболее известный среди них сплав LaNi5 (поглощает 6 атомов Н на формульную единицу сплава) и его производные LaNi2-xMx, MnNi5, Ti2Ni. Но промышленное использование Ni-МН аккумулятора началось лишь в середине 1980-х годов после создания сплава La-Ni-Co, позволившего электрохимически обратимо абсорбировать водород на протяжении более 100 циклов.
Токообразующая полуреакция на отрицательном электроде
разряд
(–) MH + OH - « M + H2O + e
заряд
И суммарная реакция
разряд
MH + NiOOH ↔ Ni(OH)2 +М
заряд
Здесь символом М обозначен сплав, MH – металлогидрид. Из этих реакций видно, что процесс заключается в переходе атома Н от одного электрода к другому электроду без расхода электролита и образования воды. Поэтому в электролите Ni-МН аккумулятора, в отличие от НК и НЖ систем, изменений не происходит.
Разрядная кривая почти такая же, как у НК аккумулятора, поскольку кадмий и водород очень близки по величине электродного потенциала.
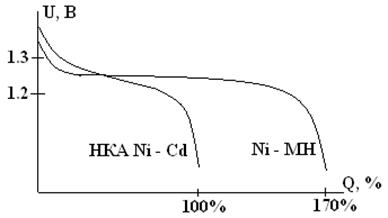
Сравнение никель-кадмиевой и никель-металлогидридной систем
Ni-МН аккумуляторы имеют то же напряжение, что и НК, и выпускаются в таких же корпусах, являясь взаимозаменяемыми. Но замена кадмий на водород позволила в 1.5 – 2 раза увеличить удельные характеристики. Удельная энергия Ni-МН системы составляет 40 – 80 Вт×ч/кг или 100 – 250 Вт×ч/л.
Это система имеет ещё ряд преимуществ:
1) Способность выдерживать высокие скорости разряда: до 5С постоянным током, до 10С импульсным. Отсюда возможность достижения высокой мощности – до 400 Вт/кг.
2) Большой ресурс (типично 400 – 1500 циклов при 100%-ной глубине циклирования), срок службы – 5 лет.
3) Способность МН-электрода к быстрому заряду. Ni-МН аккумуляторы позволяют производить сверхбыстрый заряд током 1С за 1 час или за 1.5 часа. Здесь надо сказать, что стандартным режимом заряда аккумуляторов НК и СА считается заряд током С/10. Из-за идущего параллельно электролиза воды время полного заряда составляет не 10, а 15 часов (в последние годы выпускают НК и СА, допускающие ускоренный заряд за 1 – 3 часа).
4) Переход к более экологически чистым производствам. Отсутствие токсичных материалов.
Наряду с преимуществами есть и недостатки:
1) Более высокая цена из-за применения РЗЭ или других редких металлов.
2) Температурный диапазон не такой широкий, как у никель-кадмиевых ХИТ. Большая часть Ni-МН аккумуляторов неработоспособна ниже –100C и выше +400C.
3) Саморазряд несколько выше, чем у НК (Ni-МН типично теряет 40% емкости за полгода хранения при 200C).
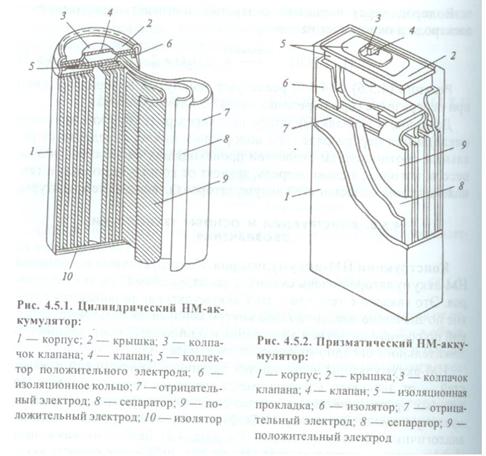
Конструкция никель-металлогидридного аккумулятора
При перезаряде Ni-МН аккумуляторов также реализуется кислородный цикл
перезаряд
2OH - ↔ 1/2O2 + H2O + 2e
Выделяющийся кислород проникает через сепаратор на отрицательный электрод и восстанавливается на нем по обратной реакции.
Применение Ni-МН аккумуляторов самое разнообразное. Прежде всего, для энергопитания современной портативной аппаратуры: переносных компьютеров, ноутбуков, сотовых телефонов, пейджеров, видео - и фотоаппаратуры, переносных электроинструментов (электродрели и т. п.), электробритв, зубных щеток, миксеров, обогревателей одежды и т. п. Но выпускаются также крупные и мощные тяговые аккумуляторы для электромобиля и для космической техники.
Ni-МН аккумуляторы имеют недавнюю историю. Их начали серийно производить за рубежом с 1987 года. Все последующие годы их производство стремительно росло. Сейчас они выпускаются всеми ведущими мировыми электротехническими фирмами, таким как SAFT (Франция), PANASONIC (Япония), SANYO (Япония), SONY (Япония), VARTA (Германия) и др. С начала 1990-х годов они начали вытеснять НК аккумуляторы, производство которых росло весь ХХ век, но с 1991 года начало сокращаться. Как представляется сейчас, со временем Ni-МН должны вытеснить НК аккумуляторы, некоторые фирмы уже объявили о прекращении выпуска НК.
Состояние отечественных разработок. Свинцовые и никель-кадмиевые аккумуляторы выпускаются в широком ассортименте многими российскими фирмами, крупное производство находится в г. Саратове, хотя зачастую ассортимент меньше, а качество ниже, чем у импортных изделий. С Ni-МН аккумуляторами ситуация хуже. Их развитие пришлось на 1990-е годы, когда промышленная наука находилась в России в кризисе. Ni-МН аккумуляторы только начали выпускаться в РФ (по данным на 2000 г. выпускаются двумя заводами в С.- Петербурге: «Мезон» и НИАИ).