СИЛИКАГЕЛЬ, Его получение, свойства и применение
Характеристика пористости
Для измерения пористой структуры адсорбентов пользуются следующими методами: адсорбционным, электрон - номикроскопическим, ртутно-порометрическим и методом рассеивания рентгеновских лучей под малыми углами.
Особенно часто применяются методы адсорбционно- структурного анализа, разработанные Дубининым, Киселевым и их сотрудниками [274—278]. Они являются наиболее простыми и широко распространенными. Их основное преимущество перед другими — возможность расчета главнейших параметров пористой структуры только на основании одной лишь изотермы адсорбции — десорбции. Однако вычисленные по этим методам характеристики структуры являются усредненными [279] и основаны на ряде упрощающих допущений. Тем не менее указанные недостатки существенно не снижают ценности адсорбцион - но-структурных методов, так как получаемые с их помощью результаты согласуются с данными других независимых методов [2801.
Эти методы позволяют определять размер и объем пор, построить кривую распределения объема по их эффективным радиусам и рассчитать удельную поверхность адсорбента.
Представления о пористости адсорбентов можно иметь, определяя их плотности. Различают три разновидности плотностей:
А) кажущаяся — вес единицы объема пористого тела, включая его поры;
Б) истинная — вес единицы объема плотноупакован - ного (не содержащего пор) вещества;
В) насыпной (гравиметрический) вес — вес единицы объема слоя сорбента, включающего объем плотного вещества тела, объема его пор и объема промежутков между зернами.
Согласно классификации Дубинина [274], различают следующие виды пор:
А) макропоры (Кма) с величиной диаметра больше 200—500 А;
Ф переходные поры (Vnep) с диаметром, равным 20— 200А;
В) микропоры (VM„) с диаметром порядка молекулярных размеров.
Названные разновидности пор выполняют различную роль в адсорбционном процессе. Микро - и переходные поры являются адсорбирующими порами. Микропоры [281—283] объемно заполняются сжиженным паром в результате действия адсорбционных сил. В переходных порах протекают два процесса: собственно адсорбция и капиллярная конденсация. Однако такое разделение весьма условно, так как сколько-нибудь резкой границы между ними не существует. Для тонкопористых адсорбентов она зависит от размеров адсорбирующихся молекул [284], а для крупнопористых адсорбирующими порами являются поры переходных размеров [279]. Макропоры не имеют значения для адсорбции в связи с тем, что их удельная поверхность ничтожно мала. Капиллярная конденсация в них не происходит из-за отсутствия мениска, и они заполняются только при пропитке жидкостью.
Объем пористого пространства, или суммарный объем пор, можно выразить
= V МН + Кпер + V маї
Сорбирующих пор
Vs = Ими + Кпер.
Суммарный объем пор определяют, зная кажущуюся и истинную плотности адсорбента
У'-і-т-
Где б — кажущаяся плотность, г/см3; D — истинная плотность, г/см3.
В стекловидных силикагелях макропоры почти отсутствуют, и поэтому суммар ый объем пор принадлежит сорбирующим порам
Их = К,
На основании большого числа экспериментальных дан'-- ных мы пришли к выводу, что величина истинной плотности силикагеля не зависит от его структуры и равна в среднем 2,2 г! см*. Это хорошо согласуется с выводами других исследователей 1285].
Остановимся на методах определения разновидностей плотностей и объемов пор пористых сорбентов. Наиболее распространенный метод измерения кажущейся плотности основан на заполнении ртутью промежутков между зернами адсорбента, помещенного в специальный вакуумный сосуд. На таком принципе основан прибор Хербста [2, 286]. Применение ртути в качестве пикнометрической жидкости обусловлено тем, что она не смачивает поверхность адсорбента и поэтому не проникает в его поры.
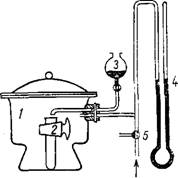
Растрененко [287] и Горош - ко [288] предложили более удобные приборы для определения кажущейся плотности, основанные на том же принципе. Прибор Растрененко состоит (рис. 43) из вакуумного эксикатора 1, в боковое
Отверстие которого вставлена резиновая пробка с двумя отверстиями. В одно из отверстий пропущен ввод от капельной воронки 3, заполненной ртутью, в другое — ввод от вакуумного насоса и ртутного манометра 4. Существенной частью прибора является пробирка 2 с тщательно прошлифованным краном 5. В отверстие болванки крана впаяно донышко с отверстиями диаметром 1 мм.
|
К насосу |
|
Рис. 43. Схема прибора для определения кажущегося удельного веса. |
Измерение кажущейся плотности производят следующим образом. Пробирку взвешивают с точностью до 0,01 г. Затем вынимают болванку крана и насыпают в пробирку около 1 г пористого вещества и вновь взвешивают. По разности весов пробирки с веществом и без него рассчитывают навеску. После этого пробирку помещают в эксикатор. Для того, чтобы воздух, находящийся в пробирке, не препятствовал проникновению в нее ртути, в одно из отверстий донышка крана вставляют капилляр. При помощи насоса создают разряжение в эксикаторе и заполняют из капельной воронки пробирку ртутью до краев крана 2. При помощи трехходового крана 5 впускают воздух в эксикатор, вынимают капилляр из пробки крана и закрывают его. Избыток ртути в воронке крана выливают в эксикатор и пробирку, наполненную ртутью с испытуемым веществом, взвешивают. Затем ртуть вместе с сорбентом удаляют из пробирки и пробирку таким же образом заполняют ртутью в вакууме. Заполненную пробирку со ртутью взвешивают с точностью до 0,01 г.
Кажущаяся плотность б находится по формуле „ _ 13,546 ■ А
(Si-SJ+A '
Где 13,546 — плотность ртути; А — навеска; G1 — вес пробирки со ртутью; G2 — то же с навеской адсорбента.
Истинная плотность также измеряется пикнометриче - ским способом. Наиболее правильные результаты получают, применяя в качестве пикнометрической жидкости бензол, с малым коэффициентом сжимаемости и обладающий способностью наиболее полно проникать во все поры адсорбента (1,289). Более точно рассчитывают истинную плотность, применяя вместо жидкости газ гелий, атомы которого не адсорбируются сорбентом и легко проникают во все его поры.
Определение истинного удельного веса производят следующим образом. Образец адсорбента 1,0—1,5 г измельчают в агатовой ступке, высушивают при 120—150° С в течение 2 ч и помещают в пикнометр, который заливают бензолом так, чтобы над образцом находился небольшой слой бензола, и нагревают на водяной бане при 60° С в течение 2—3 ч. После выдерживания пикнометра с содержимым при комнатной температуре в течение 12—16 ч его доливают до метки бензолом и взвешивают на аналитических весах. Предварительно взвешивают пикнометр с бензолом при той же температуре.
Истинный удельный вес рассчитывают по формуле
Dr И • а ^ _ ______ L»Hfl
(Si — Si) — (G3 — Gi) ' Где DCtn, — плотность бензола; A — навеска адсорбента; Gi, G4—вес пикнометра с бензолом, самого пикномет
Ра, пикном :тра с адсорбентом и бензолом, пикнометра с адсорбентом соответственно.
Существует несколько методов определения объема мик- ропор [279, 276, 285]. Одним методом рассчитывают предельно-сорбированные объемы спиртов и жирных кислот из их растворов в неполярных растворителях (для гидрофильных сорбентов), а вторым — из данных изотерм адсорбции паров метилового спирта или бензола. В последней точка начала гистерезиса капиллярно-конденсационной части изотермы отвечает заполнению тонких пор. Произведение величины адсорбции, соответствующее данной точке, на молярный объем жидкости дает объем микропор. Для большинства сорбентов эта точка при адсорбции метилового спирта отвечает относительному давлению пара 0,53, а для бензола — 0,17.
М. М. Дубинин и его сотрудники [281] разработали теорию объемного заполнения микропор адсорбентов. Согласно [281], для микропористого адсорбента, поры которого соизмеримы с размерами молекул адсорбата, существует вполне определенная величина объема адсорбционного пространства, где адсорбируемое вещество располагается не последовательными слоями, а образует объемную фазу. Это обстоятельство исключает возможность расчета удельной поверхности таких адсорбентов общепринятыми методами. Параметры микропористой структуры этих сорбентов целесообразно характеризовать основными структурными константами теории объемного заполнения.
В соответствии с основным уравнением теории объемного заполнения
А = "ysr [ ехр • В (Lg PJP)
Где W0 — предельный объем адсорбционного пространства; V* — мольный объем адсорбированного вещества; р — коэффициент аффинности характеристической кривой; В — константа, зависящая от размера пор и определяющая форму изотермы. Для расчета констант №0 и В по экспериментальным точкам применяют уравнение Ga = C-D{gPjPf,
W
Где С = lg - у - = lg а0; а0 — предельная величина адсорбции.
Предельный объем адсорбционного пространства является эффективной характеристикой объема микропор тонкопористого адсорбента Кми- В связи с малой сжимаемостью жидкостей плотность вещества в адсорбированном •Состоянии существенно не отличается от плотности жидкости в объемной фазе. В связи с этим для тонкопористых адсорбентов W0 и VMH практически совпадают. Следовательно, параметрами микропористой структуры адсорбентов являются величины W0 и В ИЛИ Vua и В.
Таким образом, для мелкопористых сорбентов, для которых формальный расчет приводит к величинам эффективных радиусов г <С 15 A, S > S', значительная доля объема пор в общем сорбционном объеме представлена микропорами. Удельная поверхность скелета таких сорбентов, вычисленная по методу БЭТ или другому, а также кривая распределения объемов пор по размерам, являющаяся типичной характеристикой переходных пор, теряют физический смысл и совершенно не дают представления об адсорбционных свойствах мелкопористых минеральных адсорбентов. Для характеристики их адсорбционных свойств необходимо знать объемы различных разновидностей пор и константы уравнения теории объемного заполнения.
В теории объемного заполнения предполагается узкое распределение микропор по размерам. Однако некоторые силикагели обладают более сложными микропористыми структурами, в которых имеются микропоры разных размеров. Параметры силикагелей характеризуются константами Wo,, Вх и W0z и Вг двухчленного уравнения Дубинина:
А = W0l/V*[expB1?(gPs/Py} +
Значение Vs дает представление об объеме сорбирующих пор. Научное обоснование физического смысла этой величины как объема всех пор, заполняемых в процессе адсорбции и капиллярной конденсации при упругости насыщенного пара, дано впервые Гурвичем [290]. По Гурвичу величина Vs в пересчете на обычную жидкость не зависит от природы адсорбируемого пара. Объем адсорбционного пространства Vs может быть рассчитан либо по изотерме сорбции, беря величину адсорбции в Ммольїг при P/Ps = = 1 (as), умножив ее на молярный объем адсорбата в жидком состоянии (Кт), либо эксикаторным методом V„ = = а V
US ' т.'
Объем макропор определяется по разности суммарного и сорбционного объемов пор, а переходных — по разности величин предельно-сорбционных пор и микропор.
Для полной характеристики адсорбционных свойств сорбента необходимо иметь представление также о распределении объема пор по величинам их радиусов. Такую структурную кривую можно получить из изотермы адсорбции, воспользовавшись теорией капиллярной конденсации. В основу этого расчета положено уравнение Томсона, связывающее радиус кривизны вогнутого сферического мениска с равновесной упругостью пара над ним
= 2 АУ0 Г RT In PJP '
Где г — радиус кривизны мениска, принимаемый равным радиусу капилляра; V0 — молярный объем адсорбированного вещества в виде жидкости; Ps — давление пара, насыщающего пространство при температуре опыта над плоской поверхностью жидкости; R — газовая постоянная, о — поверхностное натяжение жидкости.
Так как структура реальных пористых тел, в том числе и силикагелей, не может быть образована порами правильной цилиндрической формы, то расчеты по уравнению Томсона дают некоторые эффективные значения радиусов пор. Однако хорошее согласие между результатами расчета размеров пор из представления о капиллярной конденсации и другими независимыми методами [280] (электронная микроскопия, ртутная порометрия и др.) указывает на то, что эффективные радиусы пор, вычисляемые из уравнения Томсона, имеют вполне реальный смысл.
Для получения кривой распределения объема пор по эффективным радиусам поступают следующим образом. На оси ординат откладывают объем адсорбированного пара в жидком состоянии (т. е. величины AV0), а на оси абсцисс — значения г, рассчитанные из формулы при соответствующем данному значению P/Ps. При этом используются данные десорбционной «ветви» изотермы [291]. Таким образом строят интегральную кривую распределения, радиусов пор V = / (г). Наклон отдельных участков этой кривой дает величины AV/Ar. Откладывая их относительно г, получают кривую распределения объема пор по значениям эффективных радиусов (дифференциальная структурная кривая). Максимум этой кривой соответствует величине преобладающего эффективного радиуса пор, к которой прибавляют толщину адсорбционной пленки, рассчитанной по формуле
|
|
Где а — количество адсорбированного вещества (в точке, соответствующей началу гистерезисной петли); V0 — молярный объем адсорбированного вещества в виде жидкости; S — величина удельной поверхности.
Верхним пределом размеров пор, определяемых с достаточной точностью, являются радиусы 100—200 А, ниж-
|
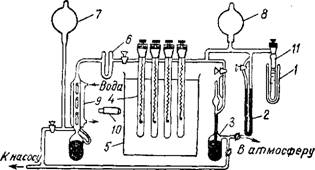
Рис. 44. Схема вакуумной установки для измерения изотерм сорбции. |
Ним пределом (в случае применения маленьких молекул азота, аргона и метанола) — радиусы 10—15 А.
Пытались экспериментально установить распределение объема пор по их радиусам. Так, Дубинин и Киселев предложили метод «молекулярных щупов», дающий возможность судить о размерах тонких пор по их доступности для адсорбции молекул разного размера.
Основные параметры пористой структуры сорбентов получают из изотерм адсорбции паров. Существует два метода экспериментального измерения адсорбции газов и паров: весовой и объемный. При весовом методе определяют увеличение веса адсорбента в результате адсорбции при данном давлении пара и заданной температуре, а при объемном — равновесное давление газа или пара; величина адсорбции в этом случае вычисляется согласно газовым законам по известному объему прибора и температуре.
Для снятия изотерм сорбции паров на пористых сорбентах весовым методом служит высоковакуумная установка
С пружинными кварцевыми весами Мак-Бена-Бакра. Сущность метода заключается в следующем: к кварцевой спирали подвешивают чашечку с адсорбентом и по удлинению спирали после адсорбции судят о количестве адсорбированного' вещества. Установка (рис. 44) состоит из измерительной и форвакуумных частей. К измерительной относятся сорб - ционные трубки 4, спирали из плавленного кварца, чашечки для навесок адсорбента, манометр Мак-Леода — для контроля степени откачки и измерения малых давлений 3, U-об - разный манометр, позволяющий измерять упругость пара до его насыщения 2, пробирки с ад- сорбатом 11, катетометр 10 и термостаты (1 и 5). Форвакуумная часть имеет насос (на рисунке неуказан), ртутный диффузионный трехступенчатый насос Ленгмюра 9, ловушки для жидкого воздуха 6, форвакуум - ные колбы 7, 8.
|
К Закуумндму Насосу |
|
XJ |
|
|
|
■ возОух |
|
Рис. 45. Ртутный затвор. |
При снятии изотерм сорбции по веществам, растворяющим смазку кранов, применяют специальные ртутные затворы. Рассмотрим некоторые наиболее ответственные детали вакуумной установки и принцип их действия. Затворы заменяют вакуумные двухходовые краны. Они представляют собой U-образную трубку, концы которой припаиваются к двум емкостям установки (рис. 45). Емкости сообщаются между собой, пока трубка пуста. Если их необходимо разъединить, то трубку заполняют ртутью, которая поступает снизу из круглого резервуара. Оба конца трубки и нижний круглый резервуар запирают стеклянными клапанами, которые представляют собой поплавки из стекла с овальным шлифом. В концах U-образной трубки и резервуара впаяны шлифы для этих поплавков. Заполнение трубки ртутью и удаление из нее ртути производят впуском воздуха в нижний резервуар и откачиванием его.. Ртуть для затворов должна быть тщательно очищена. Особенно большое внимание нужно обратить на очистку от механических примесей, так как пылинки, всплывая
На поверхность ртути, могут попасть в шлиф клапана^' и он плотно не закроется.
Манометр Мак-Леода состоит из баллончика, снабженного в верхней части капилляром. К отводной трубке, соединяющей манометр с измерительной частью установки, припаян боковой капилляр, предназначенный для сравнения высот столбиков ртути в капиллярах. Опускание и подъем ртути в манометре производят откачиванием воздуха из резервуара и впуском его.
Если известен объем баллончика и радиус капилляра, то можно рассчитать давление в установке по показаниям манометра Мак-Леода
Где Р — давление, мм Hg; Г — радиус капилляра, мм; V — объем баллончика, CmS; H — расстояние от мениска ртути в капилляре до верха капилляра в момент отсчета, когда уровень ртути в параллельном капилляре находится на высоте верха основного капилляра.
Калибровку манометра Мак-Леода производят еще до монтажа установки. Необходимо определить диаметр его капилляра и величину запираемого объема. Диаметр капилляра определяют по длине и весу залитого в него столбика ртути. Капилляры калибруются до их припайки к манометру.
Для измерения всего запираемого объема необходимо запаять конец манометра, ведущий к клапану. Затем манометр перевертывают нижним концом вверх, незапаянный конец капилляра погружают в ртуть, которая засасывается в запираемый объем при помощи вакуума, присоединенного к поднятому нижнему концу. Величина запираемого объема зависит от веса ртути, заполняющей пространство от неза - паянного конца капилляра до конца трубки. При запаивании конца капилляра длина его несколько уменьшается. Поправку на уменьшение объема можно внести, сделав на капилляре метку и измерив расстояние от метки до конца капилляра до и после запайки. Калибровку повторяют несколько раз.
Давления от 1 мм и выше измеряют U-образным манометром. Для избежания поправок на капиллярность оба колена манометра изготовляют из трубки диаметром 20— 25 мм. Манометр заполняют ртутью, поступающей из специального резервуара.
Кварцевая спираль из плавленного кварца отличается тем, что ее растяжение подчиняется закону Гука в весьма большом интервале нагрузок, не давая никаких остаточных деформаций после снятия нагрузки. Благодаря этому имеется возможность непосредственного измерения любой неизвестной нагрузки предварительно прокалиброванной спирали посредством определения линейного удлинения или укорачивания пружины. Техника изготовления кварцевой спирали описана в [292].
Чашечки для навесок адсорбента изготовляют из тонкостенного стекла. На боковой поверхности обычной пробирки выдувают несколько пузырьков, которые при помощи острого пламени делают плоскодонными. Затем пузырьки срезают раскаленной платиновой проволокой и к ним припаивают ручку из стеклянной нити, заканчивающуюся крючком.
Для данного пара и единицы массы адсорбента количество адсорбированного вещества является функцией только равновесного давления и температуры. Количество поглощенных паров выражается обычно в миллимолях на один грамм исследуемого адсорбента.
Для нанесения каждой точки изотермы необходимо знать: относительное давление пара в момент равновесия, общее количество адсорбированного пара к моменту достижения этого равновесия, навеску адсорбента после удаления из нее всех летучих примесей.
Перед тем как приступить к снятию изотермы кварцевые спирали тщательно калибруют. Жидкость, пар которой служит адсорбатом, предварительно очищают, сушат и заливают в пробирку вакуумной установки. Для снижения упругости пара над жидкостью пробирку погружают в охладительную смесь. Температура охлаждающей среды должна быть выше температуры замерзания взятой жидкости. Доводить жидкость до замерзания не рекомендуется, так как изменение удельного объема вещества при замерзании может привести к разрыву ампулы. Когда жидкость охлаждена, откачивают воздух из пробирки.
После подвода определенного количества пара к адсорбенту ампулу с веществом отделяют ртутным затвором и в таком положении навеску выдерживают до наступления равновесия. Зафиксировав равновесие (о чем судят по прекращению растяжения спирали), производят отсчет положения спирали и давления. Далее таким же образом в адсорбционную часть вводят вторую порцию пара, затем третью и т. д., вплоть до насыщения ими адсорбента при данной температуре, т. е. до относительного давления PIPS — 1. Затем производят десорбцию, при которой последовательно небольшими порциями адсорбированный пар из образцов удаляют.
Количество адсорбированного пара в ммоль/г определяют из соотношения
— B" K А~ Mm '
Где K — чувствительность спирали (мг! деление)', B — удлинение спирали (число делений); М — молекулярный вес адсорбируемого вещества; т — навеска адсорбента.
Чувствительность спирали и навеску адсорбента (50— 100 мг) подбирают с учетом предполагаемой адсорбционной активности силикагеля. Растяжение пружины измеряют катетометром.