СИЛИКАГЕЛЬ, Его получение, свойства и применение
Гидротермальное старение гидрогеля
Термодинамически уже давно обосновано явление растворения мелких частиц и рост крупных, находящихся в растворе, насыщенном по отношению к мелким частицам. Процесс повторяется до перехода системы в устойчивое термодинамическое равновесие. Однако в обычных условиях такой процесс протекает очень медленно. Интенсивность его возрастает с увеличением температуры, повышающей растворимость дисперсной фазы. Чем больше растворимость дисперсной фазы, тем процесс идет быстрее. Это явление было положено в основу регулировки пористой структуры
силикагеля методом гидротермального старения (выдерживание гидрогеля в воде при разных температурах в автоклаве).
К числу первых работ в области гидротермального старения гидрогеля кремневой кислоты можно отнести ра
Боты Брунса и Костиной Хармадарьяна и Копеле вича, Вольфа и Бейера [35 45, 164], наблюдавших па дение величины поверхнос ти и расширение пор си ликагеля при промывке геля горячей водой. Такой же эффект наблюдали Ак- шинская и Никитин [169] при обработке гидрогеля водяным паром при высоких температурах и давлении. Однако в указанных работах гидротермальный синтез силикагелей не являлся предметом специального изучения. Систематическое исследование этого вопроса было проведено одним из авторов с сотрудниками [147, 170 — 175].
|
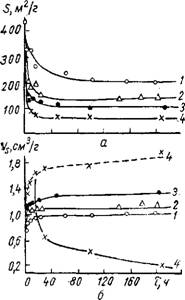
Рис. 21. Влияние условий гидротермальной обработки силикагидроге - ля на удельную поверхность (а) и предельный сорбционный объем пор (б) при 90° (Л; 120° (2); 160' (3) 215° С (4) пунктир — суммарный объем пор. |
В [170] Неймарк, Чертов и Джамбаева изучили Елияниетемпературы и продолжительности гидротермальной обработки сили - кагидрогеля на пористую структуру и свойства ксерогеля. Полученные ими результаты приведены на рис. 21. Как видно из рисунка, по мере увеличения длительности и температуры гидротермального старения гидрогеля удельная поверхность ксерогелей уменьшается, а предельный сорбционный объем пор увеличивается. При этом основные изменения в структуре происходят в первые 20—40 ч, после чего структура ксерогелей изменяется весьма незначительно. Дальнейшие ее изменения достигаются лишь с повышением температуры старения. Гидротермальная об
работка гидрогелей при 215° С в течение первых восьми часов увеличивает предельно-сорбционный объем пор от 0,76 до 1,50 смг! г, более длительное старение резко его снижает до 0,21 см3/г. В то же время суммарный объем пор силикагелей продолжает увеличиваться, что свидетельствует об образовании в них макропор. Для всех же остальных ксерогелей суммарный объем пор совпадает с предельным сорбционным объемом.
Полученные результаты авторы [170] объясняют увеличением первичных глобул исходного гидрогеля и уменьшением плотности их упаковки в процессе гидротермальной обработки. Укрупнение частиц гидрогелей в ходе гидротермальной обработки наблюдали Эшли и Иннес [176] под электронным микроскопом.
Укрупнение глобул при гидротермальном старении является следствием повышения растворимости Si02 с ростом температуры [176, 177, 97]. Это представляется таким образом, что вода расщепляет силоксановую связь на поверхности частиц гидрогеля и диаметр глобул возрастает за счет растворения самых малых из них и переноса кремневой кислоты на поверхгость более крупных. Так же растворяются и большие глобулы гидрогеля, главным образом в местах с наибольшей кривизной поверхности [178], вследствие чего происходит сглаживание ее геометрической неоднородности.
Механизм этих процессов, очевидно, такой же. как и при гидротермальной обработке алюмосиликагеля [179] и аэросила [180, 181]. Таким образом, при гидротермальном старении гидрогеля его глобулы, увеличиваясь в размерах, становятся более однородными по всей величине, более сферическими и менее «шероховатыми», более однородной становится и их упаковка.
Это находит отражение в структуре получаемых ксерогелей: их удельная поверхность уменьшается, объем и диаметр пор увеличиваются, они становятся все более однородно пористыми.
|
65 |
В последующих работах Чертов и др. [171, 172] исследовали кинетику гидротермального старения гидрогеля кремневой кислоты в нейтральной, щелочной и кислой средах в широком диапазоне температур. Авторы установили (см. табл. 16), что наиболее быстро процесс гидротермального старения происходит в щелочной среде. Так, полупериод процесса в щелочной среде (время, в течение которого
Б 3-595
|
Структурио-сорбциоииые характеристики ксерогелей, гидрогели которых (•^исходного образца =796 м2/г V2 =0,33 см3/г)
|
|
' Исследовалось также старение гидрогеля при рН 2 и в 1,0-н. HjS04. При старения несколько ускоряется. |
Удельная поверхность уменьшается вдвое) при 90° со - , ставляет 1 ч, а в нейтральной — 90 ч. При этом гидрогель - переходит в золь. С ростом температуры обработки гидрогеля в щелочной среде удельная поверхность ксерогелей уменьшается. В отличие от нейтральных гелей суммарный объем пор (Vz) ксерогелей уменьшается, становясь практи-
|
Таблица 16
|
|
РН 2 результаты практически такие же, как и при рН 1. В 1,0. и. H, S04 процесс |
|
Подвергались гидротермальной обработке в различных средах |
|
5* |
|
67 |
Чески равным предельному сорбционному объему (Vs). В кислой среде кинетика процесса гидротермального старения сильно замедляется. Так, при 90° С процесс практически не идет и лишь при 170° С происходит уже достаточно интенсивно. Полупериод процесса при 170° С и рН 1 составляет 90 ч, в
То время как при рН 6 — примерно 2 ч, а при рН 11 — меньше 0,25 ч.
Полученные данные о кинетике старения гидрогеля в разных средах согласуются с известными данными о скорости растворения кремнезема в этих средах и позволяют прийти к заключению о важной роли процесса деконден- сации кремневой кислоты (расщепления силоксановой связи) при высокотемпературной обработке гидрогеля в жидкой среде.
Существенное влияние на скорость гидротермального старения гидрогеля кремневой кислоты оказывают минеральные соли [173]. Старение в растворах солей происходит значительно быстрее, чем в воде. Так, если при старении геля в дистиллированной воде для получения ксерогеля с поверхностью — 50 м2/г необходима обработка гидрогеля в автоклаве в течение 50 ч при 300° С, то, например, в 1,0-н. растворе Na2S04 для этого требуется лишь 3 ч при 250° С. При 90° С время, необходимое для уменьшения исходной поверхности вдвое, составляет 90 ч, в 0,1 и 1,0-н. NH4F соответственно только 2 и 1 ч.
Весьма важным является и тот факт, что присутствие солей исключает переход геля в золь, что, как указывалось выше, имеет место в условиях нагрева гидрогеля в слое воды при температуре выше 200°. Таким защитным действием солей можно воспользоваться при получении силикагелей с малой величиной удельной поверхности (50—10 м2/г), Когда приходится применять высокие температуры обработки гидрогеля. С другой стороны, используя каталитическое действие растворов солей, можно существенно снизить температуру обработки гидрогеля.
Связывая кинетику процесса гидротермального старения гидрогеля со скоростью расщепления == Si — О — Si == связей его скелета, Чертов и др. [173] рассматривают расщепление силоксановых связей как реакцию нуклеофиль - ного бимолекулярного замещения, скорость которой должна зависеть от природы аниона соли. Это предположение хорошо согласуется с полученными ими результатами: по каталитическому эффекту анионы располагаются в порядке F_ > S04_>C1-. Такой порядок расположения анионов, в общем, находится в соответствии с их нуклеофильной активностью.
В дальнейшем, анализируя влияние рН среды и анионов на кинетику гидротермального старения гидрогеля, Чертов 1174] рассматривает расщепление силоксановой связи как гетерогенную реакцию, аналогичную протекающим обычно в растворах реакциям нуклеофильного бимолекулярного замещения типа S^,.
Эта реакция представляется следующим образом: ОН~ + =Si — О — Si= -> =Si — ОН + =SiO~.
В нейтральной и кислой средах анион =SiO~ взаимодействуете Н"1", образуя силоксановую группу, которая вступает затем в реакцию конденсации. В щелочной среде, где
|
Таблица 17 Гидротермальное старение гидрогеля в растворах электролитов
|
Возможно существование ионов кремневой кислоты, рекон - денсация может осуществляться также согласно уравнению =SiO~ + НО—Si= -> =Si—О—Si= + ОН-.
Доказательством бимолекулярного расщепления силок- сановых связей в гидрогеле служат результаты опытов (табл. 17), проведенных в 0,1-н. растворах NH4F и HF, свидетельствующие о значительном ускорении процесса в присутствии ионов фтора — активного нуклеофильного агента.
Реакцию с участием F - Чертов представляет следующим образом:
F- + =Si — О — Si= -> =Si — F + =SiO~, одновременно идет гидролиз связи =Si—F
=SiF + Н20 =SiOH + Н+ + F-;
=SiO - + Н+ -> =SiOH.
При обработке геля плавиковой кислотой помимо действия F - разрыв =s Si—О—Si = связи идет также вследствие его гидрофторолиза молекулами HF:
=Si—О—Si= - j - HF ->- =SiOH + =SiF.
Это было подтверждено опытами, в которых гель подвергался воздействию раствора 0,1-н. HF в 1,3-н. NH4C1, где диссоциирована только одна тысячная часть молекул HF. И в таких случаях реакция идет так же быстро, как и при обработке геля 0,1-н HF. Таким образом, F~ и HF являются катализаторами процесса гетеролитического рас-
|
Таб л и ца 18 Содержание внутриглээульных и поверхностных силанольных групп в ксерогелях *
|
Ксерогелей, независимо от величины удельной поверхности (табл. 18), концентрация поверхностных силанольных групп практически постоянна. Средняя величина степени гидратации силикагелей, полученных гидротермальной обработкой гидрогеля в автоклаве, равная ~ 9,5 мкмоль ОН/ж2, хорошо совпадает с концентрацией поверхностных гидро - ксильных групп обычных ксерогелей. Точно так же концентрация внутриглобульных силанольных групп практически постоянна (1,0Мэкв ОН/г) и, в отличие от гидротермально обработанных аэросила и силикаксерогеля, остается такой же, как у исходного образца.
Как показано было в [183], при гидротермальной обработке ксерогелей кремневой кислоты в них образуются ультрапоры, доступные для молекул воды, но недоступные для более крупных молекул криптона, азота, бензола и метанола. У силикагелей, полученных гидротермальной обработкой гидрогеля, ультрапоры не обнаружены [170].
Такое различие в структуре образцов, полученных из ксерогелей и гидрогелей при их гидротермальной обработке (наличие ультрапор у первых и отсутствие вторых), связано, по мнению авторов [175], с некоторыми различиями в условиях переосаждения кремнезема в ходе гидротермальной обработки. При этом важным обстоятельством является разная плотность упаковки скелета гидро - и ксерогелей.
Таким образом, метод гидротермальной обработки гидрогеля дает возможность в широких пределах изменять величину удельной поверхности силикагеля от 800 до 50 м2/г, не влияя на ее химическую природу. При этом получаются однородно крупнопористые адсорбенты, лишенные ультрапор.
Из результатов исследований, описанных в настоящей главе, видно, что, изменяя скорость старения гидрогеля путем изменения среды старения и температуры, можно целенаправленно регулировать пористую структуру силикагеля. На скорость старения гидрогеля влияют факторы, от которых зависит скорость поликонденсации кремневой кислоты или растворимость коллоидного кремнезема; они же определяют изменения в пористой структуре силикагеля.