Процессы и аппараты упаковочного производства
КИНЕТИКА АБСОРБЦИИ
Кинетика физической абсорбции. Скорость процесса абсорбции может быть рассмотрена на основе материала, изложенного в гл. 15. Применительно к абсорбции уравнение массопередачи (15.36), если движущую силу выразить в концентрациях газовой фазы, принимает следующий вид:
![]() , (16.17) 51
, (16.17) 51
Если движущую силу выразить в концентрациях жидкой фазы, то уравнение массопередачи записывается следующим образом:
(16.17а)
![]()
Коэффициенты массопередачи ![]() И
И ![]() В уравнениях (16.17) и (16.17а) определяются в соответствии с уравнениями (15.35) и (15.38) так:
В уравнениях (16.17) и (16.17а) определяются в соответствии с уравнениями (15.35) и (15.38) так:
![]() , (16.18)
, (16.18)
![]() , (16.18а)
, (16.18а)
Где Рг коэффициент массоотдачи от потока газа к поверхности контакта фаз; (Зж - коэффициент массоотдачи от поверхности контакта к потоку абсорбента.
Для хорошо растворимых газов величина Т Незначительна и мало диффузионное сопротивление в жидкой фазе. Тогда ![]() , и можно принять, что
, и можно принять, что ![]() Для плохо растворимых газов можно пренебречь диффузионным сопротивлением в газовой фазе, так как в этом случае значения Т И
Для плохо растворимых газов можно пренебречь диффузионным сопротивлением в газовой фазе, так как в этом случае значения Т И ![]() велики. Toгда
велики. Toгда ![]() и можно считать, что
и можно считать, что ![]()
Для процесса абсорбции в уравнении массопередачи (16.14) молярные концентрации газовой фазы могут быть заменены парциальными давлениями газа, выраженными в долях общего давления. Тогда
![]()
Где ![]()
![]()
![]() средняя движущая сила процесса, выраженная в единицах давления; Кр Коэффициент массопередачи, отнесенный к единице движущей силы, выражаемой через парциальные давления поглощаемого газа.
средняя движущая сила процесса, выраженная в единицах давления; Кр Коэффициент массопередачи, отнесенный к единице движущей силы, выражаемой через парциальные давления поглощаемого газа.
Если линия равновесия является прямой, то средняя движущая сила процесса ![]() по аналогии с уравнением (15.32) выражается так:
по аналогии с уравнением (15.32) выражается так:
(16.19)
![]()
Где ![]() = Рн — р* И
= Рн — р* И ![]() = Рк — р* Движущая сила на концах Абсорбционного Аппарата;
= Рк — р* Движущая сила на концах Абсорбционного Аппарата; ![]() и
и ![]() равновесные парциальные давления газа на входе в аппарат и выходе из него; Рн И Рк Парциальные давления газа на входе в аппарат и выходе из него.
равновесные парциальные давления газа на входе в аппарат и выходе из него; Рн И Рк Парциальные давления газа на входе в аппарат и выходе из него.
Отметим, что если парциальное давление выражено в долях общего давления p то коэффициенты массопередачи ![]() И
И ![]() Численно равны друг другу. Если же парциальные давления выражены в единицах давления, то
Численно равны друг другу. Если же парциальные давления выражены в единицах давления, то ![]()
Между коэффициентами массопередачи и высотой единицы переноса (ВЭП) имеется непосредственная связь (см. гл. 15). Поэтому анализ кинетики абсорбции может быть проведен аналогично на основе ВЭП. Частные зависимости для определения ![]() или
или ![]() для определения коэффициентов массопередачи
для определения коэффициентов массопередачи ![]() И
И ![]() Х Будут рассмотрены ниже (см. разд. 16.7).
Х Будут рассмотрены ниже (см. разд. 16.7).
Кинетика абсорбции, сопровождаемой химической реакцией (хемо-
Сорбция). Химическая реакция, сопровождающая процесс абсорб-ции может оказывать существенное влияние на кинетику процесса. При этом скорость процесса абсорбции определяется не только интенсивностью массопереноса, но также и скоростью протекания химической реакции. Если реакция идет в жидкой фазе, то часть газообразного компонента переходит в связанное состояние. При этом концентрация свободного (т. е. не связанного с поглощенным газом) компонента в жидкости снижается, что приводит к ускорению процесса абсорбции по сравнению с абсорбцией без химического взаимодействия фаз, так как увеличивается движущая сила процесса. В общем случае скорость хемосорбции зависит как от скорости реакции, так и от скорости массопереноса между фазами. В зависимости от того, какая скорость определяет общую скорость процесса переноса массы, различают кинетическую и диффузионную области процессов хемосорбции.
В Кинетической Области скорость собственно химического взаимодействия меньше скорости массопереноса и поэтому лимитирует скорость всего процесса. В Диффузионной Области
Лимитирующей • стадией является скорость диффузии компонентов в зоне реакции, которая зависит от гидродинамических условий в системе и физических свойств и определяется по основному уравнению массопередачи
Если скорости химической реакции и массопередачи соизмеримы, то такие процессы абсорбции относят к Смешанной, Или Диффузионно-кинетической Области.
При определении поверхности контакта фаз для проведения процесса хемосорбции ускорение процесса можно учесть увеличением коэффициента массоотдачи ![]() , если считать движущую силу процесса такой же, как и при физической абсорбции. Тогда коэффициент массоотдачи в жидкой фазе
, если считать движущую силу процесса такой же, как и при физической абсорбции. Тогда коэффициент массоотдачи в жидкой фазе ![]() при протекании химической реакции можно определить следующим образом:
при протекании химической реакции можно определить следующим образом:
![]() (16.20)
(16.20)
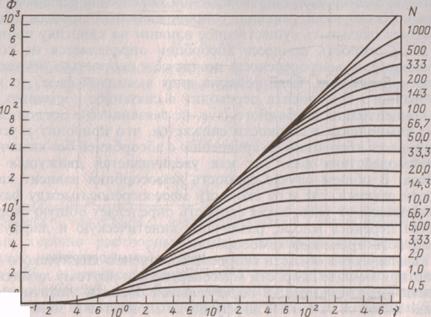
Где Ф фактор ускорения масеообмсна, показывающий, во сколько paз увеличивается скорость абсорбции за счет протекания химической реакции.
Величину Ф можно определить с помощью графика (рис. I(16.5) в зависимости от комплексов величин у и N.
 Ю
Ю
Рис. 16-5. Зависимость фактора ускорения Ф от комплексов у
В кинетической и диффузионной областях выражения для расчёта Ф упрощаются.
5.2.5. УСТРОЙСТВО И ПРИНЦИП ДЕЙСТВИЯ АБСОРБЕРОВ
Абсорбция, как и другие процессы массопередачи, протекает на поверхности раздела фаз. Поэтому абсорбционные аппараты - АбСорберы - должны Обеспечить развитую поверхность контакта между жидкой и газовой фазами. По способу образования этой поверхности, что непосредственно связано с конструктивными особенностями абсорберов, их можно подразделить на четыре основные группы: 1) пленочные; 2) насадочные; 3) тарельчатые; 4) распыливающие.