ПОЛИМЕРНЫЕ ТЕПЛОИЗОЛЯЦИОННЫЕ МАТЕРИАЛЫ
ГАЗО — И ПЕНООБРАЗУЮЩИЕ ВЕЩЕСТВА
Ячеистая или пористая структура при производстве ПТМ создается при помощи газо - или пенообразующих веществ. От правильного их выбора во многом зависит качество получаемого материала: тот или иной вид этих веществ определяет не только технологические параметры, но и способ получения ПТМ.
Газообразователи или, как их еще называют, вспенивающие вещества по агрегатному состоянию разделяют на твердые, жидкие и газообразные. По механизму процесса газовыделения твердые и жидкие газообразователи можно классифицировать следующим образом [4, 6].
1. Газообразователи, выделяющие газообразные вещества вследствие необратимого термического разложения (порофоры).
2. Газообразователи, выделяющие газообразные вещества вследствие обратимого термического разложения.
3. Газообразователи, выделяющие газообразные вещества вследствие химического взаимодействия компонентов.
4. Газообразователи, выделяющие ранее поглощенные газы вследствие термической десорбции (адсорбенты).
5. Газообразователи — легкокипящие жидкости,
Вспенивающие полимер при нагревании их до температуры кипения или при снижении давления.
По химической природе газообразователи можно разделить на органические и неорганические.
Газообразователи должны удовлетворять следующим требованиям [4, 6, 42]:
1) температурный интервал максимального газообразования должен находиться вблизи температуры полного размягчения полимерной композиции;
2) газообразователь должен хорошо распределяться в полимерной композиции;
3) газообразователь и продукты его разложения не должны влиять на скорость отверждения полимера;
4) термическое разложение газообразователя должно протекать не скачкообразно, а постепенно, с выделением газа в количестве, близком к теоретическому;
5) разложение газообразователя не должно сопровождаться выделением такого количества тепла, которое вызовет деструкцию полимера;
6) при температурах, применяемых при производстве пенопластов, газообразователь и газы, образовавшиеся при его разложении, не должны вступать в реакцию с полимером или вызывать коррозию технологического оборудования;
7) газообразователи должны быть доступными, дешевыми и устойчивыми в условиях транспортирования и хранення;
8) газообразователи и продукты их термического разложения ие должны быть токсичными.
Методы определения свойств газообразователей. Судя по требованиям, предъявляемым к газообразовате - лям, их важнейшими показателями являются температурный интервал максимального газообразования (температура разложения), количество выделяемого газа (газовое число) и теплота разложения.
Кроме того, для ряда газообразователей, особенно органических, предъявляются также требования к их влажности и температуре плавления.
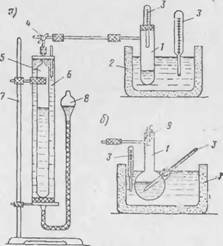
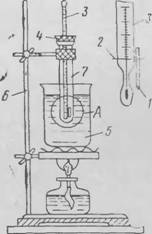
Температура разложения и газовое число газообразователей определяются при помощи прибора, схема которого показана на рис. 1. Прибор состоит из стеклянной реакционной пробирки или колбы 1 емкостью 25— Ж) мл, помещенной и термостат 2. В пробку пробирки вставляются термометр 3 и газоотводная трубка, соединенная через трехходовой кран 4 с газовой бюреткой 5 емкостью 100 мл (с ценой деления не более 0,1 мм). Газовая бюретка имеет водяную рубашку 6 и устанавливается на штативе 7. Нижний конец бюретки соединен каучуковой трубкой с уравнительным сосудом 8, заполнен-
|
Рис. 1. Схема прибора для определения газового числа порофоров А—в воздухе; б — в растворителях |
Ным ртутыо. Навеску газообразователя сбрасывают через устройство 9.
Перед испытанием газообразователь высушивают в эксикаторе под хлористым кальцием в течение суток. Навеску исследуемого газообразователя взвешивают на аналитических весах в реакционной пробирке. Для предупреждения возгонки газообразователя в пробирку помещают 1,5—2 г волокнистого асбеста, предварительно прокаленного в течение 2 ч при 500—600°С. Реакционную пробирку закрывают пробкой и соединяют с трехходовым краном бюретки.
Перед началом определения, поднимая уравнительный сосуд, заполняют газовую бюретку ртутыо. Поворотом крана 4 в реакционной пробирке устанавливают атмосферное давление и затем соединяют ее с газовой бю - рггкпй.
При исследовании газообразователен обычно проводят две серии опытов.
1. Определение газового числа. Реакционную пробирку с исследуемым газообразователем нагревают на масляной бане, обогреваемой электричеством или газовой горелкой. Скорость подъема температуры от 20 до 150—200°С не должна превышать 5 град/мин. После достижения максимальной температуры нагрев прекращают, немного охлаждают реакционную пробирку на воздухе, а затем в воде с температурой, равной температуре воды в рубашке бюретки. Когда температура в реакционной пробирке и в рубашке бюретки сравняется, замеряют объем выделившегося газа, отмечают температуру в приборе и атмосферное давление. Объем газа приводят к нормальным условиям и рассчитывают газовое число (в мл/г) по формуле
|
|
(1)
Где V — объем выделившегося газа в мл при нормальных устовпях; G — навеска газообразователя - в г.
2. Определение кинетики разложения газообразователя при постоянных температурах во времени. Реакционную пробирку тер - мостатируют при определенной температуре. Через определенные промежутки времени замеряют объем газа, приведенного к нормальным условиям.
|
(3) |
Скорости разложения навесок газообразователя при различных температурах сравнивают по относительному объему выделившегося газа, который подсчитывают по формуле
Где т)—относительное количество выделившегося газа; х — количество выделившегося газа в данный момент в мл х0— максимальное количество газа, способное выделиться при разложении данном навески газообразователя,
*„»= G X.
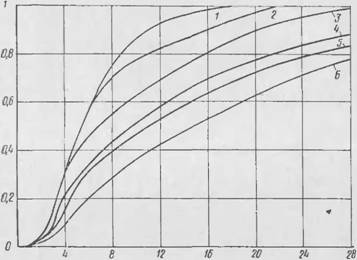
Следует учитывать, что для определения кинетики разложения газообразователя следует пользоваться навес - кон, не превышающей критической. На рис. 2 приведены кривые скоростей разложения наиболее широко применяемого га. чообразопателп порофора 4X3-57 [ П. Как ипдпо
Из рис. 2, скорость разложения, выражаемая производит)
Поп ~ , при / = const не зависит от навески порофо-
Ра, если ее величина не превышает критической. После превышения критической величины (в данном случае 0,07 г) навеска разогревается теплом, выделяющимся при разложении порофора, и. следовательно, кинетика разложения меняется.
|
Время б мин Рис. 2. Зависимость скорости разложения порофора ЧХЗ-57 при /=100°С от величины навески / - 0.1031 г; 2 — 0,0.4-М г; 3 — 0,0702 г; 4 - 0.0578 г, Ч — 0.0)90 г; в - 0,0202 г |
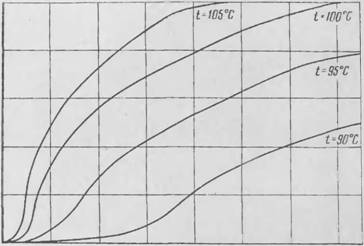
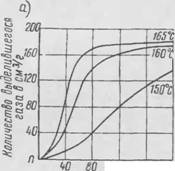
Кинетика разложения газообразователей зависит также и от среды (рис. 3) [4]. Чтобы приблизить опыт к реальным условиям производства ПТМ, кинетику разложения газообразователя определяют в растворителях. Исследования [4] показали, что скорость разложения газообразователей практически ие зависит от вида растворителей. В качестве растворителей можно использовать трнкрезилфосфат, тритолилфосфат, парафин, силиконовые масла и др.
Известен также способ изучения кинетики разложения Rn ioof>|>;i:Uin.Ti4Vi(4"i по .кшпашшщ I ;I.Iohi.I длилеипн ■ и M"Iii('|>;I Гу|и.1 Д.'ш ного и I.I I Op П м с I'P И чгс Кую бомбу
|
|
16 20 Время о мин
|
Рис. 15 Зависимость скорости разложения порофоря MX i ГГ от гемнгратурм К » итдухс; I> » рагнюрии'ля* |
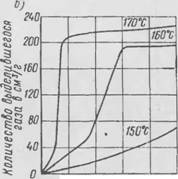
Объемом 20 см3 помещают 10 г газообразователя и нагревают его в течение 2 ч до температуры 170—250°С. По данным опыта строят кривую зависимости давления от температуры (см., например, рис. 10). Этот метод позволяет получать сравнительные характеристики газооб- разователей.
Для определения количества тепла, выделяющегося при разлоо/сении газообразователя, пока еще нет стандартной методики. Эту величину можно определить пользуясь методикой, разработанной авторами в МИСИ им.
|
|
|
61 1? |
|
16 17 |
|
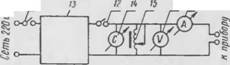
Рис. 4. Схема прибора для определения количества тепла, выделяющегося при |
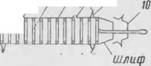
Термическом разложении порофоров О — общий вид; б — камера разложения; в — Электрическая схема; / — термостат; 2—сосуд Дьюара; 3 — мешалка; 4 — камера разложения; 5 — термометр: 6 — токопедущие стержни; 7 —кварцевая трубка; 8 — спираль; 9 — отверстия для выхода газов; 10— крышки; // — крючки; 12 — рубильник; 13 — стабн лнзатор напряжения; Л — электросекундомгр: 15 — автотрансформатор; IR — вольтметр; /7 — амперметр
В. В. Куйбышева на кафедре органических строительных материалов и пластмасс, при помощи прибора, показанного на рис. 4.
Прибор состоит из сосуда Дьюара, который закрывается корковой пробкой. В отверстие в центре пробки устанавливают метастатический термометр (типа Бекма - иа) Па пробке крепится дна токопроиоднщнх стержня,
К которым прикрепляется камера разложения из кварцевого стекла, имеющая внутри нагревательный элемент— проволочку из нихрома. Концы нагревательного элемента при помощи гаек присоединяют к токонесущим стержням. Через отверстие в пробке выводится ручка мешалки. Собранный прибор помещают в термостат для более равномерного теплообмена с окружающей средой. Для точного определения количества тепла, выделяющегося в результате прохождения электрического тока через нагревательный элемент, прибор подключают к электрической схеме.
При серийном определении теплот разложения различных газообразователей в электрическую схему прибора включают тиратронное реле времени со стабилизированным напряжением питания типа ЭЛ-1 [8, 25].
Теплоту разложения газообразователен определяют следующим образом. Вначале определяют эквивалент прибора. Для этого в прибор наливают точно отмеренное количество жидкости, не растворяющей исследуемый газообразователь и имеющей температуру кипения выше температуры ею разложения (например, ксилола, трикре - зилфосфата, четыреххлористого углерода и т. д.), камеру разложения заполняют парафином с ^Пл>70°С и пропускают через прибор электрический ток. Определяют изменение температуры в приборе. По закону Джоуля — Ленца
<2,, = 0,24 IUt, (4)
Где / — сила тока п a; U — напряжение в е; t — время прохождения электрического тока в сек.
Определяют количество выделившегося в приборе тепла при прохождении электрического тока.
Эквивалент прибора вычисляют по формуле
V _________________________________ 0±___________________________ ,5)
К'к + ЛО-Со + Ао) + Д'] Н '
Где QD — количество выделившегося тепла, подсчитанное по формуле Джоуля — Ленца (4); t к—конечная температура главного периода по шкале термометра; hK — поправка на калибр термометра при температуре tK; tQ — начальная температура главного периода по шкале термометра; И — значение градуса при работе с метастатическим термометром; At— поправка на теплообмен прибора с окружающей средой в град.
At подсчитывается по формуле Щукарева ■
At = NV0+ (m + 2r),
Здесь VB — среднее полуминутное изменение тем. пературы прибора и илчплыюм периоде; Кс — среднее полумннугиос изменение тем - тр;1тры прибор I в конечном периоде; п — число полуминутных промежутков главного периода; т — число полуминутных промежутков главного периода с быстрым (^0,3°С за '/г мин) подъемом температуры.
После определения эквивалента прибора К в кварце - вю камеру разложения помещают навеску смеси газообразователя с парафином (для нрш отопления смеси газообразователь и парафин в соотношении I : I тщательно перемешивают до получения однородной массы в фарфоровой ступке при нормальной температуре) Величину навески определяют как разность веса камеры разложения до и после помещения в нее смеси газообразователя с парафином при взвешивании па аналитических весах. Камеру прикрепляют к токонесущим стержням В сосуд Дьюара наливают точно отмеренное количество жидкости (такое же, как при определении эквивалента прибора).
Прибор собирают и подключают к электрической схеме. Теплоту разложения следует определять в тех же условиях, в которых определялся эквивалент прибора. На определенное время (установленное ранее, необходимое для подъема температуры внутри камеры, которое несколько выше температуры полного разложения газообразователя) включается электрический ток. Определяется изменение температуры в приборе таким же образом, как и при установлении эквивалента. Исходя из теплового баланса прибора,
Qp.i.-u, P + Q* = КН [(/Ft - I- Hk) - (f0 + H0) + A /], (7)
Тепло, выделяющееся при термическом разложении газообразователя, определяют по формуле
КН [(Ilk + hk) - (/„ + Ftp) + А /] - Q„
Фразл = ------------------------------------------- Р • (8)
Где Р — навеска газообразователя в г; Q0 — количество тепла, выделившегося при прохождении электрического тока через нагревательный элемент (подсчмтывается по формуле Джоуля — Лтаца), К — эквивалент прибора
Точность метода зависит не столько от качества используемой аппаратуры, сколько от тщательности проведения опыта и измерений Основная ошибка получается при отсчете изменения температуры за счет параллакса. При соблюдении всех условии опыта можно определить теплоту разложения газообразователя с точит гыо До 0,1 0,0Г»%
Температуру плавления определяют в приборе, показанном па рис. 5. Высушенный для испытания газообразователь помещают в два стеклянных капилляра / свнут - ренним диаметром 0,8—I мм и длиной 70—80 мм. Осторожным постукиванием запаянным концом капилляра и стеклянной палочкой уплотняют газообразователь в слой высотой 3—4 мм. Открытые концы капилляров запаивают.
При помощи резинового кольца 2 капилляры крепят к термометру 3 так, чтобы •столбик вещества шаходилсн па середине ртутного резервуара термометра. На верхнюю часть термометра надевают пробку 4 с отверстием для сообщения с атмосферой. Баню 5 Устанавливают на штативе 6, Наполняют чистым глицерином или вазелиновым маслом и в середину ее устанавливают при помощи зажима пробирку 7 диаметром около 20 мм, В которую заливают глицерин на высоту слоя 50 мм. Прибор нагревают до 80°С, после чего в пробирку помещают термометр с прикрепленными капиллярами так, чтобы ртутный резервуар термометра не касался стенок пробирки и был погружен в слои глицерина, а начало шкалы термометра находилось не выше уровня глицерина в бане.
Дальнейшее нагревание ведут так, чтобы температура глицерина повышалась на 2 град/мин. Температуру, при которой газообразователь окончательно переходит в прозрачное жидкое состояние, принимают за температуру плавления.
Влажность газообразователей определяют по методу Дина и Старка в приборе по ГОСТ 1594—42.
|
Узсп А
Рис. 5. Схема прибора определения темпе л плавления порофорои |
К газообразователям, выделяющим газ вследствие необратимого термического разложения, относятся различные органические вещества (порофоры), которые при ионыикчшоп температуре разлагаются с выделением i <i-
|
ТАБЛИЦА 1. ОСНОВНЫЕ ФИЗИКО-ХИМИЧЕСКИЕ СВОПСТВЛ ПОРОФОРОВ
|
|
Продолжение табл. T
|
Дифениламип-р, р' -дисульфо - гидразнд
|
Продолжепие табл. I |
|
Газовое число в см3/г |
|
Торговое наименование |
|
Химическое название н форм>ла |
NH..—NH-SO.,—С„П4- — NH—CeH4—SOj—NH—NHa
|
Дибензил-р, р'-дисульфогидра - зид N112—N11-SOi-QI 14—CI I— —CI I,—Cel I.,—SO,—NH—Nil., |
Порофор ДФ-1 (СССР) |
122 |
145 |
|
Парауретплапфенилсульфоннл - гидразпд CeI I5—0—CO—NH—CeH5— —NH—CO—0—C0H.,—SO»— —NH — NH2 |
Порофор 5 (СССР) |
82—94 |
100—168 |
|
V, л'-оксиди (бензосульфонил- гидразид) NH2—NH—S02—CeH4—О— —C0H4—S02—NH—NH2 |
Genitron OB (Англия); Ge- Iogen (США) |
115—130 |
150—155 |
|
Бензол-1, 3-дисульфонилгидра - зид NHa—NH—S02—CeH4—SO«— —NH—NH2 |
Порофор ДФ-9 (СССР); порофор В-13 (ФРГ) |
183 |
135 |
|
Дифенилсульфон-3,3 - днсульфо - гнразнд H2N—NH—SOi—CeH4— —S02—Ce H4—SOa—NH—NH3 |
Порофор ДФ-10 (СССР); порофор Д-33 (ФРГ) |
103 |
147 |
|
I, 3, 5-тригидразид-2, 4, 6-трн- |
Порофор ДФ-2 |
180 |
2С0—280 |
|
Азпд |
(СССР); Ge |
||
|
Nitron ТИТ |
|||
|
(HaN — NH — )3 — Q — (N11.,)3 |
(Англия) |
|
Продолжение табл. 1
|
|
Продолжение табл. 1
|
Зов N2, СО2, NH3 и др. По химическому строению их можно разделить на следующие классы:
А) азосоединения R—N = N—R';
Б) сульфонилгидразнды R— S02NII — NH2;
В) нитрозосоединения R—N(NO)—R';
Г) азиды кислот R — CON3;
Д) прочие соединения.
Эти вещества с необратимым характером реакции газообразования хорошо измельчаются и совмещаются с полимерами. Недостатками порофоров являются токсичность продуктов разложения, сравнительно высокая стоимость, возможность снижения теплостойкости пено- материала ввиду пластифицирования полимера продуктами разложения.
В табл. 1 приведены основные характеристики применяемых порофоров[1].
В СССР для производства ПТМ наиболее широко применяются порофоры ЧХЗ-57. ЧХЗ-21, 5 и 18. Кроме того, применяют порофоры ДАБ, 254, БСГ, ДФ-4 и т. д.
Порофор ЧХЗ-57 (азоизобутиронитрнл) представляет собой белый кристаллический порошок со следующими свойствами: удельный вес 1,11 г/см3, молекулярный вес 164,22, температура плавления 105—106°С с разложением, легкорастворнм в спирте, эфире; плохо в воде. Промышленность выпускает его в виде технического продукта двух сортов — сухого и влажного, в соответствии с требованиями СТУ-12 № 10.236-62 (табл. 2).
|
ТАБЛИЦА 2. ТЕХНИЧЕСКИЕ ТРЕБОВАНИЯ К ПОРОФОРУ ЧХЭ-57
|
|
1 Показатели определяются на воздушно-сухом продукте. |
Технический порофор ЧХЗ-57 имеет голубоватый оттенок. Его разложение начинается при 75—80°С, значительно ускоряется в интервале 95—100°С, а выше 100°С становится бурным. Кинетика разложения порофора ЧХЗ-57 показана на рис. 3.
Разложение порофора ЧХЗ-57 протекает по схеме: CHg сн3 сн3 сн3
TOC o "1-3" h z II II
Н3с — С — N = N — С — CIГ3 - N2 + СН3 — С — С — СН3
I I II
CN CN CN CN
Реакция протекает через промежуточную стадию образования свободных радикалов. Поэтому порофор ЧХЗ-57 может применяться в качестве инициатора реакции полимеризации. Продукты разложения токсичны. Теплота разложения находится в пределах 80.5— 130,6 ккал/моль и зависит от содержания основного вещества и примесей в порофоре, его газового числа, сроков хранения и т. д.
Порофор ЧХЗ-21 (азодикарбонамнд) прсдстлпляетсобой труднорастворимое кристаллическое вещество желтого цвета с удельным весом 1,66 г/см3. Он разлагается по схеме
|
N Нг |
|
Н2ы |
|
NHr |
|
|
|
Ч / С - с О о |
|
Мг + |
H2N
/
С - N = N - С О О
|
120 Ffpet/я В мим |
|
160 200 |
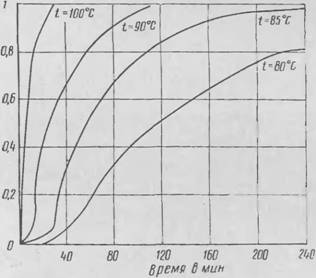
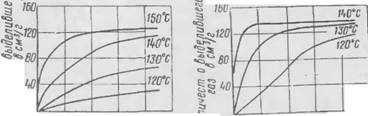
При температуре около 170°С. Последняя может быть снижена до 140°С, если в порофор добавить мочевину. Продукты разложения нетоксичны. Кинетика разложения порофора ЧХЗ-21 показана на рис. 6,а.
|
W ВО 120 160 200 Время 6 мин |
|
«о ез |
|
«Э «а ^ От Э - <з S3 D Со § о |
|
ВО 120 160 Б мин |
|
Время |
U0 80 120 160 200 Время б мин
|
■ по|кк|н1]).| |>ГГ |
Рис. 6. Кинетике разложения
|||||>|)|||<||>.1 ЧЧ i VI. I ||11|нм|и.||.| Ifi, а |||||Ш||||)|>.'| ДЛ1>
Порофор 5 (парауретиланфеннлсульфонилгидразид) представляет собой кристаллический порошок сепо-жсл-
того цвета. Он имеет небольшое газовое число (82— 94 мл/г) и поэтому в полимерную композицию вводится в повышенном количестве (8%).
Порофор 18 (N-, К'-динитрозопентаметнлеитетра - мин) — кристаллическое вещество бледно-желтого цвета с удельным весом 1,4 г/см3, слаборастворимое в органических растворителях. Разлагается при 150—180°С с выделением 220—250 мл/г газа (кинетика разложения показана на рис. 6, б). При повышенных температурах порофор 18 разлагается водой. Температура разложения может быть снижена добавлением органических кислот (салициловой и стеариновой). При разложении выделяется азот, появляются следы формальдегида и метиламина. Последний придает изделию характерный запах, остающийся после вспенивания. При добавлении мочевины (с глицерином) запах исчезает. Порофор 18 чувствителен к механическим воздействиям и недостаточно стоек при хранении. Поэтому его часто стабилизируют маслами, пластификаторами или полимерами.
Порофор ДАБ (диазоаминобензол)—кристаллический продукт оранжево-коричневого цвета с температурой плавления до 96°С, разлагается в интервале 120—150°С (кинетика разложения показана на рис. 6,в) по схеме
Г------ >-N - N - MH-<--------------- > N2 +
Порофор ДАБ хорошо распределяется в смеси и обладает пластифицирующими свойствами. Окрашивает изделия в оранжевый цвет. Недостатком является токсичность (вызывает раздражение кожи).
Порофор 254-1, Г-азо-бис(1-циклогексилцианид) — кристаллическое вещество белого цвета, начинает разлагаться при 100°С, бурно разлагается при 110—120°С. Имеет невысокое газовое число (83—85 мл/г).
Порофор БСГ (бензосульфопилгидразид) ■— кристаллический порошок серо-белого цвета с удельным весом 1,43 г/см3, разлагается при 120—140°С (кинетика разложения показана на рис. 6,г).
В присутствии окислителей температура разложения снижается, и процесс идет очень бурно. Продукты разложения являются активными ускорителями реакции полимеризации.
Порофор ДФ-4 (терефталазид) — кристаллическое вещество бледно-желтого цвета с удельным весом 1,5 г/см3, очень активный газообразователь, разлагается при 85—112°С по схеме
OCNj<ZZ> N3CO^OCNC=>NCO+ 2N2
Продукты разложения ускоряют процесс отверждения композиции, в результате которого образуется однородная мелкоячеистая структура.
К газообразователям, выделяющим газы вследствие обратимого термического разложения, относятся неорганические вещества — карбонаты. Их преимуществом является дешевизна и доступность, а также то, что продукты их разложения, в отличие от органических газообразователей, не оказывают пластифицирующего действия на полимер, что позволяет получать пеиопласты с более высокой теплостойкостью. Но их недостаток—плохое совмещение с полимером — затрудняет их равномерное распределение в смеси. Широкое применение для получения пенопластов из газообразователей этого вида нашли карбонат аммония и бикарбонат натрия.
Карбонат аммония (аммонии углекислый) (ГОСТ 3770—47) получают насыщая аммиачную воду углекислым газом или поглощением водой аммиачно-углекис - лой газовой смеси. Он представляет собой белые твердые куски и кристаллы с запахом аммиака и содержит 28—35% NH3. Технический продукт кроме (NH3)2COs содержит также NH4HCO.1 (бикарбонат аммония) и NH4COONH4 (карбомат аммония), так как углекислый аммоний при действии влаги воздуха частично гидроли - зуется:
3 (NH4)2 СО3 + Н20 2 NH4HC03 + NH4COONH4 + 2 NH4OH.
Увеличение влажности карбоната аммония сдвигает равновесие реакции гидролиза вправо, в сторону образования бикарбоната и карбомата аммония, которые начинают диссоциироваться уже при 30—40°С:
N114НС03 чЛ NH3 + СО-, + Н20;
NH4C00NH4 ^ 2 NH3 + С02.
Бикарбонат аммония начинает распадаться при 60°С: (N114).. СО.-, < * 2 N11»* | СО, | М. Л.
•м
Технический карбонат аммония разлагается очень бурно (рис. 7): быстро образуются значительные количества аммиака и углекислого газа, что приводит к резкому повышению давления, в результате чего образуется коупнопористая структура. Для производства пено- пластов размер его зерен должен быть не более 2 мм.
Бикарбонат натрия (ГОСТ 2156—54), получаемый карбонизацией содовых щелоков, выпускается в виде белого кристаллического порошка. Технический продукт содержит не менее 98,5% NaHC03, 1— 1,2% Na2C03 и другие примеси. Влажность не должна превышать 1%- Процесс разложения бикарбоната натрия обратим и в большой степени зависит от температуры и давления:
2 NaHC03 ^ Na2C03 - f Н20 + СО «
Разложение начинается при 85°С и ускоряется с повышением температуры (рис. 7). Теоретическое количество газообразных продуктов при разложении составляет 267 см3/г. Разложение протекает спокойно, с образованием равномерной структуры без крупных пор. Бикарбонат натрия обладает относительно малым вспенивающим действием, поэтому его часто применяют в сочетании с карбонатом аммония. Размер зерен его должен быть не более 2 мм.
Сообщения о применении газообразователей, выделяющих газы в результате химического взаимодействия компонентов, для получения пено - и поропластов появились сравнительно недавно. В настоящее время эти газообразователи довольно широко применяются в производстве пенорезин. Для вспенивания феполо-формальде - гидных полимеров используют реакции взаимодействия металлов, стоящих в ряду напряжения выше водорода (А1-, Zn, Mg, Fe), с минеральными кислотами H2S04, Н3РО4, НС1, сопровождающиеся выделением газов. Для облегчения диспергирования в полимере применяют тон
кие порошки металлов с определенной пластинчатой формой частиц [132, 133, 135, 138].
Применяют также смеси порошков металлов (Zn, Al, Mg и др.) с органическими кислотами (например, олеиновой), которые при нагревании способны к довольно интенсивному газообразованию. Эти вещества взаимодействуют при 80°С по схеме
П RCOOH + Me (RCOO)„ Me + - у Н2.
Для впенивания этих же полимеров применяют реакцию взаимодействия солей фенилдиазония (например, сульфита или фосфата) [(R') (R")C6H3N=N] с водой при нормальной температуре, в результате чего выделяется азот, фенол н соответствующая кислота [99, 141].
При сравнительно низких температурах (65—80°С) нитрит натрия взаимодействует с хлористым аммонием с выделением большого количества газообразных продуктов:
NH4C1 + NaN02 ^ NaCt - f NH4N02
I
N2 + 2 H,0
Реакция взаимодействия этих веществ экзотермичиа и проходит очень быстро [85].
Для получения пенопластов используют и другие газообразователи например полиэтиленполиамин с ГКЖ-94 при вспеинвании эпоксидных полимеров [88].
Газообразователи, выделяющие ранее поглощенные газы вследствие термической десорбции, представляют собой адсорбенты, которые выделяют при повышенной температуре газы, адсорбированные их активной поверхностью. К их числу относятся активированный уголь, сплпкагель, цеолиты, тьтивнроваппые глины н т. д.
Скорость адсорбции и количество поглощенного газа зависят в первую очередь от химической природы адсорбента и физической структуры его поверхности, а также от давления п температуры, при которой протекает адсорбция. Так как адсорбция газов всегда сопровождается выделением тепла, то при повышении температуры газ будет выделяться (десорбция). Поэтому при прочих равных условиях выгодно насыщать адсорбент при возможно no ire пипкой |гми<-рат ре чем ниже температура адсорбции, тем выше вспенивающая способность газообразователя — адсорбента.
При производстве пенопластов газообразователи этого типа применяются сравнительно редко.