ИНИЦИИРОВАНИЕ
Для технологии производства полиэтилена под высоким давлением практическое значение имеет инициирование органическими пероксида - ми и кислородом. Первое применяется в основном при проведении полимеризации в автоклавных реакторах, второе — в трубчатых.
Как известно, инициирование пероксидами заключается в образовании первичных радикалов при термической диссоциации связи —О—О—
R—О—О—R' кР'СП- R—О + о— R (4.14)
И взаимодействии этих первичных радикалов с мономером по реакции (4.1)*, причем скорость определяет реакция (4.14) как более медленная.
Отсюда:
"и = ''расп=Драсп[І]. (4.15)
Где / - эффективность инициирования — доля первичных радикалов (от общего их количества), участвующая в инициировании полимеризации.
Вопрос о значениях эффективности инициирования при полимеризации этилена и влиянии на эту величину различных факторов практически не изучен. Эффективность инициирования, вероятно, имеет весьма низкие значения, так как температура процесса на 100 °С и более превышает значения, при которых обычно используются соответствующие перок - сиды. Учитывая высокие значения энергии активации (для различных пер[5] оксидов Е= 105-Н50 кДж/моль), скорость распада пероксидов в условиях процесса исключительно велика и побочные реакции радикалов (например, эффект клетки) не могут не играть существенной роли.
В зависимости от строения R и R' скорость распада пероксидов и ее изменение с температурой и давлением для различных пероксидов различны. В табл. 4.1 приведены значения Е и AV* для некоторых пероксидов, применяемых в качестве инициаторов полимеризации этилена, а также данные о температурах, при которых периоды полураспада* составляют 1 мин.
Рассмотрим особенности применения инициаторов в реакторах обоих типов.
Автоклавные реакторы представляют собой, в первом приближении, реакторы идеального смешения (см. гл. 2), имеют во всем объеме одинаковую концентрацию инициатора, которая определяется материальным балансом и выражается уравнением:
[Лр/[Ло = 1/ (1 + ^распт) > (4.16)
Где [Л р и [/] о - равновесная и исходная концентрации пероксида, т - среднее время пребывания реакционной массы в реакторе.
На рис. 4.1 показана зависимость равновесной концентрации ди-грег- бутилпероксида и 7рег-бутилпербензоата от времени пребывания реакционной массы в реакторе. В интервале обычно используемых в промышленных установках времен пребывания (20-50 с) и температур процесса (выше 250 °С) равновесная концентрация составляет менее 5 % от исходной.
Скорость инициирования уи из (4.15) и (4.16) выражается следующим образом:
Таблица 4.1. Влияние температуры и давления на распад некоторых пероксидои [8]
|
ДГ* см3 /моль |
|
Е, КДж/моль |
|
Пероксид |
Температура, С, для туг = 1 мин
Прн0,098 МПапрн 294 МЦа
Дициклогексилперокси - 100 107 116 4,3 дикарбонат
TOC \o "1-3" \h \z Диоктаноилпероксид 127 133 129 5,9
Ірет-Бутилпернеодеканоат 113 119 103 6,1
Ірет-Амилпернеодеканоат 124 133 102 7,0
Ірег-Бутилперпивалат 123 131 110 6,1
Ірег-Амилперпивалат 124 135 113 9,4
Ди-грег-бутилпероксид 191 203 152 13,4
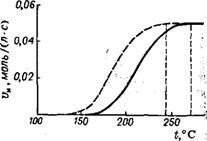
Анализ этого уравнения (рис. 4.2) показывает, что с повышением температуры скорость инициирования возрастает (при постоянной концентрации инициатора) и, достигнув определенного значения, характерного для каждого инициатора, далее остается постоянной. Условием достижения этого постоянства является: красПтР- 1 • Этим условием следует руководствоваться при выборе инициаторов, так как его соблюдение обеспечивает минимальный удельный расход инициатора.
Выбор инициатора влияет также и на стабильность процесса. При
Использовании инициатора в ин - Щр тервале температур, в котором
|
|
|
10 |
|
20 |
|
30 |
|
40 |
[По
0,3
|
|
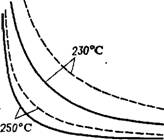
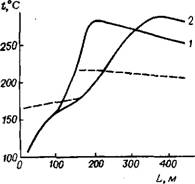
Рис. 4.3. Профиль температуры в трубчатом реакторе при использовании инициаторов с низкой (1) и высокой (2) температурой разложения [411 --------------------------------------------------- температура теплоносителя
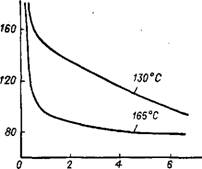
Рис. 4А. Критическая граница полимеризации при инициировании кислородом при температурах 130 и 165 °С [381
Скорость инициирования зависит от температуры, случайное понижение температуры вызовет снижение скорости инициирования, что, в свою очередь, приведет к замедлению полимеризации, уменьшению выделения - теплоты и еще большему снижению температуры вплоть до прекращения реакции. И наоборот, случайной повышение температуры приводит к еще большему ее росту из-за ускорения реакции. Независимость скорости инициирования от температуры, делая невозможным описанное развитие событий, увеличивает стабильность процесса.
Трубчатый реактор, представляющий собой реактор вытеснения, имеет переменные температуру и концентрацию инициатора по длине. Концентрация инициатора в каждом сечении реактора определяется уравнением:
[I]p/[I]o=e~fcpacn*, (4.18)
Іде t — время прохождения реакционной массы от момента ввода в реактор до рассматриваемой точки (при постоянной скорости реакционной массы оно пропорционально длине); £расп ^ const вследствие переменной температуры по длине реактора.
Изменение концентрации инициатора в этом случае определяют совместным решением уравнений теплового и материального баланса (см. гл.5).
|
|
Характеристики применяемого инициатора влияют на протекание процесса в реакторе.. На рис. 4.3 показаны профили температуры в трубчатом
реакторе при использовании низкотемпературных к высокотемпературных пероксидов. В случае низкотемпературного инициатора температура сначала резко возрастает и достигает максимума ні коротком участке реактора, при применении пероксидов с высокой температурой распада рост температуры более плавный и максимальная температура достигается на гораздо большей длине. Эти особенности инициаторов влияют на производительность реактора и качество полимера.
В отличие от инициирования пероксидами, механизм и кинетика которого более или менее ясны, инициирование кислородом более сложно. Согласно существующим представлениям [38, с. 409; 39], процесс протекает через образование промежуточных продуктов реакции кислорода с этиленом или полимером, по-видимому, пероксидного характера, которые в дальнейшем могут давать активные радикалы, инициирующие полимеризацию, или неактивные продукты, а также участвовать в различных побочных реакциях, вплоть до ингибирования:
С2Н4 + 02 - [С2Н4-02], (4.19,а)
[С2Н4-Ог] 2R, (4.19,6)
R - + С2Н4 кр » R—СНг—СН2, (4.19,6)
[С2Н4-02] ----------- Неактивные продукты. (4.19, г)
Побочные реакции;
R—СНг—СНг + Ог—і к, .
^ » Блокирование растущих цепей. (4.19,д) R - + Ог—1
В пользу именно такого механизма свидетельствуют некоторые выявленные особенности процесса, например, наличие индукционного периода и критической границы полимеризации. На рис. 4.4 показаны границы давления и концентрации кислорода, ниже которых полимеризация практически не идет, а выше - протекает с большой скоростью. Такие особенности, характерные для вырожденных разветвленноцепных реакций, к которым относятся процессы окисления углеводородов, являются результатом комплекса реакций (4.19). Скорости каждой из этих ріеакций могут по-разному зависеть от давления, температуры и состава реакционной смеси. В случае, когда fcpacn^i > имеем обычное инициирование:
•'ин=/*ЛСгН4][Ог]. (4.20)
Для относительно узких интервалов варьирования параметров, которые применяются в промышленных установках, кинетика процесса удовлетворительно описывается этим уравнением.
В течение многих лет считалось, что этилен не способен к термической полимеризации под давлением даже при температурах выше 200 °С [38, с. 412]. В работе [40] было показано, что при давлении около •200 МПа может происходить термическая полимеризация этилена с образованием высокомолекулярного (Мп до 105) полимера. Инициирование протекает через образование бирадикала из двух молекул этилена: СН,=СН2+СН2=СН2 СН2-СН2-СН2-СН2 . (4.21)
Общая скорость полимеризации v описывается уравнением:
V = 2,Q3 «lO'e-16465/7^2,5 . (4.22)
Вследствие очень высокой энергии активацииЕ = 136,3 ± бкДж/моль скорость образования полимера сильно изменяется с температурой. Так, при давлении 200 МПа конверсия 3% достигается при 150 °С за 6,7 сут, при 180°С за 12,2 ч, при 250°С за 5,6 мин, при 350°С за 2,2 с.
Эти данные позволяют предположить, что часто обнаруживаемый в работающих при высоком давлении и невысоких температурах частях промышленных установок (подогревателях, фильтрах и др.) высокомолекулярный полиэтилен может образовываться даже в отсутствие инициаторов в результате медленной термической полимеризации зтилена.