С фазовыми переходами рабочего вещества
Естественным является использовать процессы фазовых переходов рабочего вещества с целью получения холода:
• процесс 4 - плавление (переход рабочего вещества из твердого состояния в жидкое). Наиболее ярким примером является использование тепла, необходимого для таяния водного льда или, другими словами, производство холода с помощью процесса таяния льда. Бхтественно, в этом случае можно получить холод на температурном уровне несколько выше, чем Тхол=0°С.
Количество тепла, которое необходимо затратить на плавление некоторого количества рабочего вещества в твердом состоянии (га), является количеством холода, вырабатываемом при плавлении
Q=Am, (4.2)
Где X - удельное тепло плавления рабочего вещества; га - мссгь рабочего вещества;
• процесс 5 - кипение (переход рабочего вещества из жидкого состояния в газообразное).
Количество тепла, необходимое для кипения, является количеством вырабатываемого холода, которое можно получить при кипении
Q=rm, (4.3)
Где г - удельное тепло парообразования рабочего вещества; m масса рабочего вещества.
Абсолютно для всех рабочих веществ повышение температуры и давления влечет за собой уменьшение г. Состояние, при котором г=0 называется критической точкой, при температуре Т > Ткр переход «жидкость —► газ» невозможен (рис.2.5).
На практике для получения холода используют жидкости, кипящие при пониженном давлением.
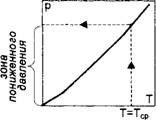
Рис.4.2. Иллюстрация к определению понятия пониженное давление (кривая насыщения)
|
Таблица 4.1
|
Пониженным давлением (для рабочего вещества) называют такое давление, которое меньше давления, соответствующего кипению этого же рабочего вещества при температуре окружающей среды. Зона пониженного давления показана на рис.4.2. Таким образом для любого рабочего вещества можно определить давление, соответствующее температуре кипения равной температуре окружающей среды и, если заставить кипеть это рабочее вещество при более низком давлении, то можно получить холод. Понятие пониженное давление не постоянное и характеризуется физическими свойствами каждого рабочего вещества. В таблице 4.1 приведены значения «пониженного давления» для некоторых рабочих веществ, если принять Тср=20°С (293К).
|
|
• процесс 6 - сублимация (переход рабочего вещества из твердого состояния в газообразное, минуя жидкое). Характерным примером является использование сухого льда (СО2) как автономного источника холода, например, при розничной продаже мороженого. Менее эффективным является использование процесса
Сублимации сухого спирта и нафталина как метода получения холода.
Количество тепла, необходимое для процесса сублимации, является количеством холода, получаемым при сублимации
Q=lm = (X + r)m, (4.4)
Где I - удельное тепло сублимации; т - масса рабочего вещества.
Таким образом видно, что процесс сублимации сопровождается производством большего количества холода, чем процессы кипения или плавления в отдельности.
Для чистых (однокомпонентных) рабочих веществ процесс фазового превращения является изобарно-изотермическим, т. е. на диаграммах состояний в области влажного пара и в области совместного существования смеси рабочего вещества в твердом и газообразном состояниях изотерма совпадает с изобарой. Для смесей рабочих веществ процессы фазового перехода являются только изобарным, так как температура в них изменяется.
Обратим внимание, что процессы 7, 2, 3, 4, 5 и 6 (рис.4.1), идущие слева направо (т. е. с ростом энтропии), протекают естественно. Для возвращения рабочего тела в первоначальное состояние (процессы 7*, 2*, 3* - охлаждение без фазового перехода; процесс 4* - кристаллизация; процесс 5* - конденсация; процесс 6* - десублимация) необходимо затрать энергию, т. е. использовать компенсирующий процесс.
Особое место в методах получения холода занимает процесс испарения жидкости в парогазовую смесь (на рис.4.1 этот процесс отсутствует). Испарение жидкости со свободной поверхности в парогазовую смесь является результатом теплового движения молекул в жидкости, в результате чего при испарении жидкость теряет наиболее быстро движущиеся молекулы. Кинетическая энергия молекул, оставшихся в жидкости, уменьшается и, как следствие этого, температура жидкости понижается. Понижение температуры жидкости будет происходить до тех пор, пока при некоторой температуре не установится динамическое равновесие между подводом тепла к жидкости и отводом его путем испарения этой жидкости. Процесс испарения, при котором все тепло, переданное от парогазовой смеси к жидкости, затрачивается на испарение жидкости и затем возвращается в парогазовую смесь, называют процессом адиабатного испарения. В процессе
адиабатного испарения достигается температура, ниже которой охладить жидкость уже невозможно. Такая температура носит название температуры мокрого термометра.
Процесс испарительного охлаждения применяют в устройствах для охлаждения воды наружным воздухом (градирни, брызгаль - ные бассейны), а также в системах кондиционирования воздуха.
Итак, нами рассмотрены все возможные методы получения холода. Теперь проанализируем методы получения низких температур, т. е. выясним использованием каких природных процессов можно понизить температуру любого рабочего вещества (в любом агрегатном состоянии) ниже температуры окружающей среды, чтобы впоследствии произвести холод.